
 �������ʹ���������������õ���Ҫ�о�����
�������ʹ���������������õ���Ҫ�о�����| m |
| V |
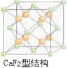 �����þ�̯�����㣮
�����þ�̯�����㣮| 1 |
| 2 |
| 1 |
| 8 |
| 1 |
| 2 |
| m |
| V |
| 52 |
| V��NA |
| 52 |
| V��NA |
 ����������֪���þ�����ͭԭ�Ӹ���=6��
����������֪���þ�����ͭԭ�Ӹ���=6��| 1 |
| 2 |
| 1 |
| 8 |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
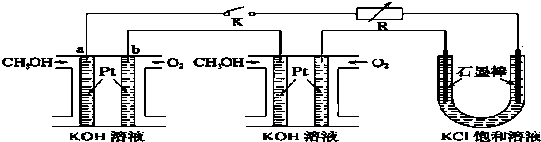
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��Ӧʱ��/min | n��CO��/mol | n��H2O��/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
A����Ӧ��t1 min�ڵ�ƽ������Ϊv��H2��=
| ||
| B�����������������䣬��ʼʱ�������г���0.60 mol CO��1.20 mol H2O���ﵽƽ��ʱn��CO2��=0.30 mol | ||
| C�����������������䣬��ƽ����ϵ����ͨ��0.20 mol H2O����ԭƽ����ȣ��ﵽ��ƽ��ʱCOת��������H2O������������� | ||
| D���¶�������800�棬������Ӧƽ�ⳣ��Ϊ0.64��������ӦΪ���ȷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Yԭ���е�������Xԭ�Ӷ�һ��������Zԭ����һ�� |
| B��Y���ʺ�Z��X�ĵ��ʾ����Է�Ӧ |
| C��Ԫ��ZΪ���õĽ������䵥�ʸ�ˮ��Ӧ�ų��������������ˮ��Һ�Լ��� |
| D��Xԭ�����ⷴӦ���γ�HX |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.1mol |
| B��0.2mol |
| C��0.4mol |
| D��0.8mol 1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ |
| B���۲��Ƿ��� |
| C���Ƚϵ����� |
| D���۲��Ƿ��ж�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A | B | C | D | |
| �� �� Ŀ �� | �̶��ݻ����ܱ������У�ѹǿ�Է�Ӧ�� 2SO2��g��+O2��g��?2SO3��g����Ӱ�� | �̶��ݻ����ܱ������У��¶ȶԷ�Ӧ�� N2��g��+3H2��g��?2NH3��g����H��0��Ӱ�� | �̶��ݻ����ܱ������У�����CO2Ũ�ȣ����Ѵ�ƽ��ķ�Ӧ�� CO��g��+H2O��g��?CO2��g��+H2��g����Ӱ�� | ������Na��K �ֱ�������ˮ��Ӧ |
| ʾ �� ͼ | 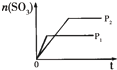 | 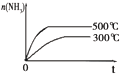 | 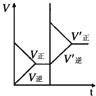 | 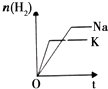 |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com