
【题目】下列说法不正确的是
A.在常温下SiO2(s)+2C(s)=Si(s)+2CO(g)不能自发进行,则该反应的H>0
B.常温下,NH4Cl溶液加水稀释,![]() 不变
不变
C.向硅酸钠溶液中滴加酚酞,溶液变红,证明Na2SiO3发生了水解
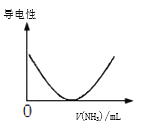
D.如图可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化
 特高级教师点拨系列答案
特高级教师点拨系列答案科目:高中化学 来源: 题型:
【题目】下列关于1.5 mol 氢气的叙述中,正确的是( )
A.质量是 4 g B.体积是 33.6 L C.电子数是3 D.分子数是 1.5×6.02 ×1023 个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列具有特殊性能的材料中,由主族元素和副族元素形成的化合物是( )
A. 半导体材料砷化镓 B. 吸氢材料镧镍合金
C. 透明陶瓷材料硒化锌 D. 超导材料K3C60
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100mL 6molL﹣1H2SO4跟过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量( )
A.碳酸钠(固体)
B.少量硫酸铜溶液
C.Na2SO4溶液
D.加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图1是在金属锌板上贴上一张用某溶液浸湿的滤纸,图2是NaBH4/H2O2燃料电池,则下列说法正确的是

A.图2电池放电过程中,Na+从正极区向负极区迁移
B.图2电池负极区的电极反应为BH4-― 8e- + 8OH-=BO2- + 6H2O
C.若用硫酸钠和酚酞的混合溶液浸湿滤纸,用导线将a、b直接相连,则铅笔芯C点处出现红色
D.若用KI淀粉溶液浸湿滤纸,用导线将a、b与A、B电极相连,铅笔芯C点处出现蓝色,则b接的是A电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于氢键,下列说法中,正确的是 ( )
A. 氢键比范德华力强,所以它属于化学键
B. 分子间形成的氢键使物质的熔点和沸点升高
C. 含氢原子的物质之间均可形成氢键
D. H2O是一种非常稳定的化合物,这是由于氢键所致
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有可逆反应Fe(s)+CO2(g)![]() FeO(s) + CO(g),已知在温度938K时,平衡常数K=1.5,在1173K时,K=2.2 。
FeO(s) + CO(g),已知在温度938K时,平衡常数K=1.5,在1173K时,K=2.2 。
(1)1mol铁粉和1molCO2在2L密闭容器中反应,判断该反应达到平衡状态的依据是 (填序号)。
A.容器内压强不再改变
B.c(CO)不再改变
C.生成1mol的FeO
D.c(CO2)=c(CO)
E.v正(CO2)=v逆(CO)
(2)该反应的正反应是_________(选填“吸热”、“放热”)反应。
(3)若起始时把Fe和CO2放入体积固定的密闭容器中,CO2的起始浓度为2.4 mol/L,某温度时达到平衡,此时容器中CO的浓度为1.0 mol/L,则该温度下上述反应的平衡常数K= (保留二位有效数字)。
(4)一定条件下,该反应在体积固定的密闭容器中进行一段时间后达到平衡状态。使该平衡状态正向移动的措施有(写出两条) 、 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲使明矾[ KAl(SO4)2·12H2O ]溶液中的 Al3+ 完全沉淀,应加入过量的
A.氨水 B.稀硫酸 C.氢氧化钠溶液 D.氯化钠溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com