
【题目】有机物A 分子式为C2H4,可发生以下系列转化,已知B、D是生活中常见的两种有机物,下列说法不正确的是
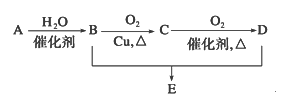
A. 75%的B溶液常用以医疗消毒
B. 由物质A到物质B发生的是加成反应
C. 物质B、D和E可以用饱和Na2CO3溶液鉴别
D. 由物质B、D制备E常用浓硫酸作脱水剂
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:
【题目】苯乙烷(C8H10)可生产塑料单体苯乙烯(C8H8),其反应原理是:C8H10(g)C8H8(g)+H2(g)△H=120kJ·mol-1某温度下,将0.40mol苯乙烷,充入2L真空密闭容器中发生反应,测定不同时间该容器内气体物质的量,得到数据如下表:
时间/min | 0 | 10 | 20 | 30 | 40 |
n(C8H10)/mol | 0.40 | 0.30 | 0.24 | n2 | n3 |
n(C8H8)/mol | 0.00 | 0.10 | n1 | 0.20 | 0.20 |
(1)当反应进行到20min时,该段时间内H2的平均反应速率是_____________。
(2)该温度下,该反应的化学平衡常数是_______________________。
(3)若保持其他条件不变,用0.40 molH2(g)和0.40molC8H8(g)合成C8H10(g),当有30kJ热量放出时,该反应中H2的转化率是__________。此时,该合成反应是否达到了平衡状态?_______(填“是”或“否”)。
(4)工业上以高温水蒸气作为反应体系的稀释剂(不参与反应),C8H10(g)的平衡转化率与水蒸气的用量、体系的温度、压强的关系如图Ⅰ、图Ⅱ所示。

①由图Ⅰ可知,T1________T2(填“大于”、“小于”或“等于”)。
②由图Ⅱ可知,当其他条件不变时,水蒸气的用量越大,C8H10的平衡转化率将________(填“越大”、“越小”或“不变”),原因是______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分离提纯下列物质时选用的试剂或方法不正确的是
分离提纯 | 试剂 | 方法 | |
A | 除去Cl2中的HCl | NaOH溶液 | 洗气 |
B | 提取溴水中的溴单质 | CCl4 | 萃取 |
C | 除去SiO2中的Fe2O3 | 稀盐酸 | 过滤 |
D | 除去乙醇中的水 | 无水CuSO4 | 蒸馏 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在下图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
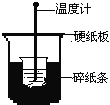
(1)从实验装置上看,图中尚缺少的一种玻璃用品是________。
(2)烧杯间填满碎纸条的作用是_____________。
(3)大烧杯上如不盖硬纸板,求得的中和热数值将_______(填“偏大”、“偏小”或“无影响”)。
(4)实验中改用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比较,所放出的热量________(填“相等”或“不相等”),但中和热应_________(填“相等”或“不相等”),简述理由_________________________________。
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得中和热的数值与57.3kJ/mol相比较会__________;用50mL0.50mol/LNaOH溶液进行上述实验,测得中和热的数值与57.3kJ/mol相比较会__________(均填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2.0mol SO2气体和2.0mol SO3气体混合于固定体积的密闭容器中,在一定条件下发生反应:2SO2(g)+O2(g)![]() 2SO3(g),达到平衡时SO3为n mol.在相同温度下,分别按下列配比在相同密闭容器中放入起始物质,平衡时SO3等于n mol的是( )
2SO3(g),达到平衡时SO3为n mol.在相同温度下,分别按下列配比在相同密闭容器中放入起始物质,平衡时SO3等于n mol的是( )
A. 1.6 mol SO2+0.3 mol O2+0.4 mol SO3
B. 4.0 mol SO2+1.0 mol O2
C. 2.0 mol SO2+1.0 mol O2+2.0 mol SO3
D. 2.0 mol SO2+0.5 mol O2+1.0 mol SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】摩尔盐( (NH4)2Fe(SO4)2·6H2O)广泛用于化学分析。溶于水,不溶于乙醇,在空气中比硫酸亚铁稳定,有还原性。现以废铁屑等为原料制备摩尔盐,并对产品中相关离子进行检测。
(一)制备过程如下:
步骤1:将废铁屑置于热的纯碱溶液中,充分浸泡后过滤、洗涤。
步骤2:向步骤1的滤渣中加入适量稀硫酸,到剩余少量固体为止。过滤。
步骤3:向步骤2的滤液中加入稍过量的(NH4)2SO4饱和溶液。
步骤4:小火蒸发到有晶膜出现,停止加热,冷却后过滤。
步骤5:将步骤4的滤渣洗涤,干燥,得到产品。
回答下列问题:
(1)步骤1中主要是利用纯碱溶液的碱性除去油污。写出纯碱溶液显碱性的主要的离子方程式:__________________________________ 。
(2)步骤1中,也可以用倾析法代替过滤,操作如图所示。下列适合用倾析法分离的是________

a.沉淀颗粒较大 b.沉淀容易沉降
c.沉淀呈胶状 d.沉淀呈絮状
(3)步骤4不直接蒸干的理由是___________________________________________。
(4)步骤5中,洗涤沉淀用的洗涤剂是_____________。
(二)产品中NH4+、Fe2+的检测。
(5)NH4+的定性检测:取少量产品于试管中,加水溶解,_______________________ ,证明样品中含有NH4+(填操作及现象)。
(6)测定产品中Fe2+的含量:称取10.0g产品,溶于水,加入足量NaOH溶液。过滤、洗涤、灼烧、冷却、称量。重复灼烧、冷却、称量,直到_______________为止。称量固体质量为2.0g。产品中Fe2+的质量分数为_______。
(7)己知Li2Ti5O15和Na2O2中都含有过氧键,Ti的化合价为+4,Na2O2中含有一个过氧键,则Li2Ti5O15中过氧键的数目为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)①煤的干馏是____________(填“物理变化”或“化学变化”);
②乙烯分子中官能团的符号____________;
③葡萄糖的结构简式_______________;
④乙醇分子中官能团的电子式_________________;
(2)某反应体系中有反应物和生成物共六种:H2C2O4、CO2、(VO2)2SO4、VOSO4、H2SO4、H2O。完成并配平该反应的化学方程式_____________。
(3)已知铍与铝的化学性质相似,绿柱石是铍、铝的硅酸复盐,其化学式为Be3Al2Si6O18。写出绿柱石溶解于过量NaOH溶液的离子方程式________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在373K时,把0.5molN2O4气体通入体积为5L(恒容)的真空密闭容器中,立即出现红棕色。反应进行到60s时体系达到平衡,此时容器内压强为反应前的1.6倍。下列说法不正确的是
A. 平衡时,N2O4的转化率为60%
B. 平衡时,体系内NO2为0.04mol·L-1
C. 其它条件不变,平衡后再往该密闭容器中通入0.5molN2O4气体,重新达到平衡时N2O4的体积百分数增大
D. 其它条件不变,平衡后再往该密闭容器中通入1molN2O4气体,重新达到平衡时该反应平衡常数不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com