
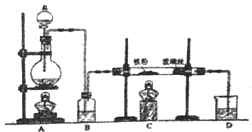
【题目】向炙热的铁屑中通入氯气生产无水氯化铁;向炽热铁屑中通入氯化氢生产无水氯化亚铁。现用如图所示的装置模拟上述过程进行实验。
回答下列问题:
(1)制取无水氯化铁的实验中,A中反应的化学方程式为___,B中加入的试剂是___,D中盛放的试剂____。
(2)制取无水氯化亚铁的实验中,装置A用来制取____,尾气的成分是___,仍用D装置进行尾气处理,存在的问题是____、____。
(3)若操作不当,制得的FeCl2会含有少量FeCl3,原因可能是____,欲制得纯净的FeCl2,在实验操作中应先___,再____。
【答案】MnO2 + 4HCl(浓) ![]() MnCl2 + Cl2↑+ 2H2O 浓硫酸 NaOH溶液 HCl HCl和H2 发生倒吸 可燃性气体H2不能被吸收 氯化亚铁被装置内的氧气氧化 通入HCl气体一段时间(排出装置内空气) 点燃C处酒精灯
MnCl2 + Cl2↑+ 2H2O 浓硫酸 NaOH溶液 HCl HCl和H2 发生倒吸 可燃性气体H2不能被吸收 氯化亚铁被装置内的氧气氧化 通入HCl气体一段时间(排出装置内空气) 点燃C处酒精灯
【解析】
由制备氯化铁的实验装置可以知道,A中浓盐酸与二氧化锰反应生成氯气,B中浓硫酸干燥氯气,C中Fe与氯气反应生成氯化铁,D中NaOH溶液吸收尾气;
若制备无水氯化亚铁,A中浓硫酸与NaCl反应生成HCl,B中浓硫酸干燥HCl,C中炽热铁屑中与HCl反应生成无水氯化亚铁,D为尾气处理,但导管在液面下可发生倒吸。
⑴由制备氯化铁的实验装置可以知道,A中浓盐酸与二氧化锰反应生成氯气,反应为
MnO2 + 4HCl(浓) ![]() MnCl2 + Cl2↑+ 2H2O,装置B主要作用是干燥氯气,因此B中加入的试剂是浓硫酸,D装置主要是处理尾气,因此用NaOH溶液来处理尾气;故答案分别为MnO2 + 4HCl(浓)
MnCl2 + Cl2↑+ 2H2O,装置B主要作用是干燥氯气,因此B中加入的试剂是浓硫酸,D装置主要是处理尾气,因此用NaOH溶液来处理尾气;故答案分别为MnO2 + 4HCl(浓) ![]() MnCl2 + Cl2↑+ 2H2O;浓硫酸;NaOH溶液;
MnCl2 + Cl2↑+ 2H2O;浓硫酸;NaOH溶液;
⑵制取无水氯化亚铁的实验中,装置A用来制取HCl,Fe与HCl反应生成氢气,可以知道尾气的成分是HCl和H2,若仍用D的装置进行尾气处理,存在的问题是发生倒吸、可燃性气体H2不能被吸收,故答案分别是HCl;HCl和H2;发生倒吸;可燃性气体H2不能被吸收;
⑶若操作不当,制得的FeCl2会含有少量FeCl3,主要原因是氯化亚铁被装置内的氧气氧化,欲制得纯净的FeCl2,在实验操作中应先通入HCl气体一段时间(排出装置内空气),再点燃C处酒精灯,故答案分别是氯化亚铁被装置内的氧气氧化;通入HCl气体一段时间(排出装置内空气);点燃C处酒精灯。


科目:高中化学 来源: 题型:
【题目】在2L密闭容器中进行如下反应:N2+3H2![]() 2NH3,5min内氨的物质的量质量增加了0.1mol,则反应速率为
2NH3,5min内氨的物质的量质量增加了0.1mol,则反应速率为
A. v(NH3)=0.02mol/(L·min)
B. v(NH3)=0.01mol/(L·min)
C. v(N2)=0.01mol/(L·min)
D. v(H2)=0.03mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国秦俑彩绘和汉代器物上用的颜料被称为“中国蓝”、“中国紫”,直到近年来人们才研究出来其成分为![]() ,
,![]() 。
。
(1)“中国蓝”、“中国紫”中均具有![]() 离子,
离子,![]() ________,基态时该阳离子的价电子排布式为________。
________,基态时该阳离子的价电子排布式为________。
(2)合成“中国蓝”、“中国紫”的原料有![]() ,孔雀石
,孔雀石![]() 和砂子(
和砂子(![]() )。现代文物分析发现,“中国蓝”中含有微量硫元素。假若硫元素来源于一种阴离子的立体结构型是正四面体的天然钡矿中,则该钡矿主要成分化学式是________。
)。现代文物分析发现,“中国蓝”中含有微量硫元素。假若硫元素来源于一种阴离子的立体结构型是正四面体的天然钡矿中,则该钡矿主要成分化学式是________。
(3)在5500年前,古代埃及人就已经知道如何合成蓝色颜料—“埃及蓝”![]() ,其合成原料中用
,其合成原料中用![]() 代替了
代替了![]() ,其他和“中国蓝”一致。
,其他和“中国蓝”一致。![]() 中键角为________。根据所学,从原料分解的角度判断“埃及蓝”的合成温度比“中国蓝”更________(填“高”或“低”)。
中键角为________。根据所学,从原料分解的角度判断“埃及蓝”的合成温度比“中国蓝”更________(填“高”或“低”)。
(4)硝酸铜溶于氨水形成![]() 的深蓝色溶液。
的深蓝色溶液。
①![]() 中阴离子的立体构型是________。
中阴离子的立体构型是________。![]() 中心原子的轨道杂化类型为________。
中心原子的轨道杂化类型为________。
②氨气在一定的压强下,测得的密度比该压强下理论密度略大,请解释原因________。
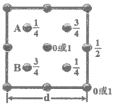
(5)自然界中的![]() 硬度较大,主要原因是________。下图为
硬度较大,主要原因是________。下图为![]() 晶胞中
晶胞中![]() 原子沿
原子沿![]() 轴方向在
轴方向在![]() 平面的投影图(即俯视图),其中
平面的投影图(即俯视图),其中![]() 原子略去,
原子略去,![]() 原子旁标注的数字表示每个
原子旁标注的数字表示每个![]() 原子位于
原子位于![]() 轴的高度,则
轴的高度,则![]() 与
与![]() 的距离是________。
的距离是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化铁和氧化铜的固体混合粉末Xg,高温下用足量的一氧化碳还原,得到金属混合物2.4 g,将生成的二氧化碳气体用足量的澄清石灰水吸收后,产生5 g白色沉淀,则X的值为( )
A.2.45
B.3.20
C.4.00
D.7.40
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物 A、B、C、D、E 的衍变关系如下所示。其中,A 是粮食发酵的产物,D 是高分子化合物,E 具有水果香味。
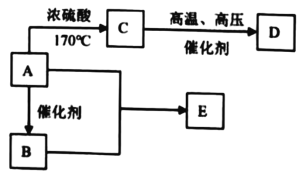
请回答下列问题:
(1)A 的名称是______,含有的官能团名称是______。
(2)写出 A 和 B 反应生成 E 的化学方程式______,该反应的类型为______。
(3)D 的结构简式为______。
(4)写出把 C 通入溴水中的现象______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t℃下,某反应达到平衡,平衡常数K=c(NO)c(SO3)/c(NO2)c(SO2)。恒容时,温度升高,NO浓度减小。下列说法正确的是( )
A.该反应的焓变为正值B.恒温下增大压强,反应体系的颜色加深
C.升高温度,逆反应速率减小D.该反应化学方程式为NO+SO3![]() NO2+SO2
NO2+SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用生活中常见的材料可以进行很多科学实验,甚至制作出一些有实际应用价值的装置来,下图就是一个用废旧材料制作的可用于驱动玩具的电池的示意图。该电池工作时,有关说法正确的是( )

A. 铝罐将逐渐被腐蚀
B. 炭粒和炭棒上发生的反应为O2+4e- = 2O2-
C. 炭棒应与玩具电机的负极相连
D. 该电池工作一段时间后炭棒和炭粒的质量会减轻
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两个恒容的密闭容器中进行下列两个可逆反应:
甲:C(s)+H2O(g)![]() CO(g)+H2(g)
CO(g)+H2(g)
乙:CO(g)+H2O(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
现有下列状态:①混合气体平均相对分子质量不再改变
②恒温时,气体压强不再改变 ③各气体组成浓度相等
④反应体系中温度保持不变 ⑤断裂氢氧键速率是断裂氢氢键速率的2倍 ⑥混合气体密度不变 ⑦单位时间内,消耗水蒸气质量与生成氢气质量比为9∶1
其中能表明甲、乙容器中反应都达到平衡状态的是( )
A. ①②⑤ B. ③④⑥ C. ⑥⑦ D. ④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com