
����Ŀ����50mL0.50mol/L������50mL0.55mol/LNaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȡ��ش��������⣺
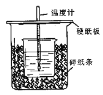
(1)��ϸ�۲�ʵ��װ�ã�ͼ���Ƿ�ȱ��һ�ֲ�����Ʒ�����ȱ�٣�ȱ�ٵ��� (���������ƣ������ȱ�٣��˿ղ��)��ͼ���Ƿ��в���֮�����������ָ�� (���û�У��˿ղ��)
(2)�ձ���������ֽ���������� ��
(3)���ձ����粻��Ӳֽ�壬��õ��к�����ֵ (����ƫ��ƫС����Ӱ����)
(4)����ͬŨ�Ⱥ�����Ĵ������������Һ��������ʵ�飬��õ��к�����H�� ��(����ƫ��������ƫС��������Ӱ����)��
(5)�����60mL0.50mol/L������50mL0.55mol/LNaOH��Һ���з�Ӧ��������ʵ����ȣ����ų������� (������ȡ��������)�������к��� (������ȡ��������)����������
���𰸡�
(1)���β�������� �����ձ���С�ձ��ڲ�ƽ
(2)���� ������ʵ������������ʧ��
(3)ƫС ��(4)ƫ��
(5)����ȡ���ȡ��к�����һ����ֵ����ʵ�������������
��������
���������(1)�������ȼƵĹ����֪��װ�õ�ȱ�������ǻ��β����������װ�õĴ����ǣ�С�ձ�������ձ��ڲ���ƽ����δ������ֽ�����ʴ�Ϊ�����β�����������ڴ�С�ձ���δ������ֽ����С�ձ�������ձ��ڲ���ƽ��
(2)�к��Ȳⶨʵ��ɰܵĹؼ��DZ��¹������ձ���������ֽ���������DZ��¡����ȣ�����ʵ������е�������ʧ���ʴ�Ϊ�����¡����ȣ�����ʵ������е�������ʧ��
(3)���ձ����粻��Ӳֽ�壬���������ʧ����õ��к�����ֵ�����С���ʴ�Ϊ��ƫС��
(4)����Ϊ���ᣬ�������Ϊ���ȹ��̣������ô������ϡ������Һ��Ӧ����Ӧ�ų�������ƫС����õ��к�����ֵ�����С����H��ƫ�ʴ�Ϊ��ƫ��
(5)��Ӧ�ų����������������Լ�������Ķ����йأ���60mL 0.50mol/L������50mL 0.55mol/LNaOH��Һ���з�Ӧ��������ʵ����ȣ�����ˮ�������࣬���ų�������ƫ�ߣ������к��ȵľ���ǿ���ǿ�Ӧ����1molˮʱ�ų����ȣ������������أ��к�����ֵ��ȣ��ʴ�Ϊ������ȣ���ȣ��к�����ָ�������кͷ�Ӧ����1molˮ���ų�������Ϊ���ģ������ᡢ��������ء�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�ظ���Cr������Һ����Ҫ��Cr3+������ɫ����Cr��OH��4������ɫ����Cr2O72�����Ⱥ�ɫ����CrO42������ɫ������ʽ���ڣ�Cr��OH��3Ϊ������ˮ�Ļ���ɫ���壬�ش�
��1��Cr3+��Al3+�Ļ�ѧ�������ƣ���Cr2��SO4��3��Һ�е���NaOH��Һֱ���������ɹ۲쵽�������� ��
��2��CrO42����Cr2O72������Һ�п��ת���������£���ʼŨ��Ϊ1.0molL��1��Na2CrO4��Һ��c��Cr2O72������c��H+���ı仯��ͼ��ʾ��

 �������ӷ���ʽ��ʾNa2CrO4��Һ�е�ת����Ӧ ��
�������ӷ���ʽ��ʾNa2CrO4��Һ�е�ת����Ӧ ��
����ͼ��֪����Һ������ǿ��CrO42����ƽ��ת���� �������С�����䡱��������A�����ݣ��������ת����Ӧ��ƽ�ⳣ��Ϊ ��
��3����K2CrO4Ϊָʾ������AgNO3��Һ�ζ���Һ�е�Cl����Ag+��CrO42������ש��ɫ����ʱ����ζ��յ�������Һ��Cl��ǡ����ȫ������Ũ�ȵ���1.0��10��5molL��1��ʱ����Һ��c ��Ag+��Ϊ molL��1����ʱ��Һ��c��CrO42�������� molL��1����Ksp��Ag2CrO4��=2.0��10��12��Ksp��AgCl��=2.0��10��10����
��4��+6�۸��Ļ����ﶾ�Խϴ���NaHSO3����Һ�е�Cr2O72����ԭ��Cr3+����Ӧ�����ӷ���ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I�����������Fe��ȥ��ˮ���е���������NO3�����ѳ�Ϊ�������о����ȵ�֮һ��
��1��Fe��ԭˮ����NO3���ķ�Ӧԭ����ͼ��ʾ��

�����ĵ缫��Ӧʽ�� ��
��2������������Ͷ��ˮ���У���24Сʱ�ⶨNO3����ȥ���ʺ�pH��������£�
��ʼpH | pH=2.5 | pH=4.5 |
NO3����ȥ���� | �ӽ�100% | ��50% |
24СʱpH | �ӽ����� | �ӽ����� |
��������������̬ |
|
|
pH=4.5ʱ��NO3����ȥ���ʵ͡���ԭ���� ��
��3��ʵ�鷢�֣��ڳ�ʼpH=4.5��ˮ����Ͷ���������۵�ͬʱ������һ������Fe2+�����������NO3����ȥ���ʡ���Fe2+������������ּ��裺
����Fe2+ֱ�ӻ�ԭNO3��������Fe2+�ƻ�FeO��OH�������㡣
�� �Ա�ʵ�飬�����ͼ��ʾ���ɵõ��Ľ����� ��
��ͬλ��ʾ�ٷ�֤ʵFe2+����FeO��OH����Ӧ����Fe3O4����ϸ÷�Ӧ�����ӷ���ʽ�����ͼ���Fe2+���NO3��ȥ���ʵ�ԭ�� ��
II.��������Na2FeO4 ��һ�����;�ˮ����
��4������������Ҫͨ�����·�Ӧ��ȡ:2Fe��OH��3+3NaClO+4NaOH= 2Na2FeO4+3X+5H2O,��X�Ļ�ѧʽΪ__________��
��5���������ƾ���ǿ�����ԣ���ˮ��Ӧ����Fe��OH��3�����ܹ�����ˮ���������ʣ���д������������ˮ��Ӧ�����ӷ���ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����г�ȥ���ʵķ�����ȷ���ǣ� ��
�� ��ȥ��������������ϩ������������ͨ��Cl2����Һ���룻
�� ��������ˮ�ĵ����Ҵ���ȡ��
�� ��ȥCO2��������SO2������ͨ��ʢ����̼��������Һ��ϴ��ƿ��
�� ��ȥ�Ҵ��������������������ʯ�ң�����
A���� �� B���� �� C���� �� D���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������M���C�����������ͼ������ԭ���á������ܶȸߵ��ŵ㣬������Ϊ����Դ�������ƶ��豸�ĵ�Դ�������طŵ���ܷ�Ӧ����ʽΪ��4M+nO2+2nH2O=4M��OH�� n����֪����ص������۱�������ָ��λ�����ĵ缫�������������ͷų��������ܡ�����˵������ȷ������ ��

A�����ö�缫��Ŀ������ߵ缫��������Һ�ĽӴ��������������������ɢ���缫����
B���Ƚ�Mg��Al��Zn���ֽ����C������أ�Al�C������ص����۱��������
C����M�C��������У�Ϊ��ֹ����������Mg��OH��2���˲������Ե���ʼ������ӽ���Ĥ
D��M�C������طŵ���̵�������Ӧʽ��4Mn++nO2+2nH2O+4ne�C=4M��OH��n
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й����е绯ѧװ��˵����ȷ������ ��

A��װ������,�����е�K+����ZnSO4��Һ
B��װ��������һ��ʱ���,a��������Һ��pH����
C����װ��������ͭʱ,c��Ϊ��ͭ
D��װ������ظ����ĵ缫��ӦʽΪO2+4e-+2H2O=4OH-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ͬ��Ba(OH)2��Һ�У��ֱ�������ʵ���Ũ����ȵ�H2SO4��NaHSO4��Һ���䵼�������������Һ����仯��������ͼ��ʾ��
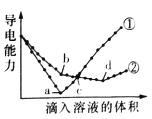
���з�������ȷ����( )
A���������μ�H2SO4��Һ�ı仯����
B��b�㣬��Һ�д������ڵ�������Na+��OH-
C��c�㣬����Һ�к�����ͬ����OH-
D��a��d�����Ӧ����Һ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ɫ��Һ�п��ܺ�����Na+ ����Ba2 +�� ��Clһ�� ��Brһ����SO32һ����SO42һ �����е������֣����ν�������ʵ�飬��ÿ�������Լ����������۲쵽���������¡�

���н��۲���ȷ���ǣ� ��
A���϶�û�е��������� B������ȷ�����������ۢ�
C���϶����е��������٢ۢܢ� D���϶����е��������٢ܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ����д�����ۣ������������� ��
ѡ�� | ���ӷ���ʽ | ���� |
A | ��������Fe3O4�ܽ��ڹ�����ϡHNO3��Fe3O4+8H+=Fe2++2Fe3++4H2O | ��ȷ��Fe2+��Fe3+���ʵ���֮��Ϊ1:2 |
B | Ba(HCO3)2��Һ��������NaOH��Һ��Ӧ Ba2����HCO3-��OH��=BaCO3����H2O | ��ȷ����ʽ����Ӧ�������κ�ˮ |
C | ����SO2ͨ�뵽NaClO��Һ�У� SO2��H2O��ClO��=HClO��HSO3- | ��ȷ��˵�����ԣ�H2SO3ǿ��HClO |
D | 1mol/L��NaAlO2��Һ��2.5mol/L��HCl��Һ�����������Ȼ�ϣ� 2AlO2-��5H��=Al3����Al(OH)3����H2O | ��ȷ��AlO2-��Al(OH)3���ĵ�H�������ʵ���֮��Ϊ2��3 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com