
【题目】25℃时,由醋酸和醋酸钠按一定比例混合形成的溶液始终保持c(CH3COOH) +c(CH3COO-)= 0.1mol/L,该溶液中c(CH3COOH)、c(CH3COO-)与pH的关系如下图所示,下列有关该溶液的叙述中正确的是
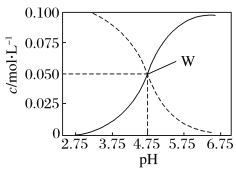
A.pH=5的溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-)
B.W点所表示的溶液中:c(Na+)=c(CH3COOH)
C.pH=3的溶液中:c(H+)+c(Na+)+c(CH3COOH)=0.1mol/L
D.据图像可求得该温度下CH3COOH的电离常数Ka=10-4.75
【答案】D
【解析】
A、由图可知,pH=4.75时,c(CH3COO-)=c(CH3COOH),故当pH=5时,有c(CH3COO-)>c(CH3COOH),且溶液显酸性,则c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-),故A错误;
B、溶液存在电荷守恒,应为c(Na+)+c(H+)=c(CH3COO-)+c(OH-),W点时c(CH3COOH)=c(CH3COO-),故c(Na+)+c(H+)=c(CH3COOH)+c(OH-),若c(Na+)=c(CH3COOH),则c(H+)=c(OH-),与图像不符,故B错误;
C、由电荷守恒及c(CH3COOH)+c(CH3COO-)=0.1molL-1可知,c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=c(CH3COO-)+c(CH3COOH)=0.1mol/L,c(H+)+c(Na+)+c(CH3COOH)=0.1mol/L+c(OH-),故C错误;
D、W点c(CH3COOH)=c(CH3COO-),平衡常数K=![]() =10-4.75molL-1,故D正确;
=10-4.75molL-1,故D正确;
故选D。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.乙烯、氯乙烯、聚乙烯均可使酸性高锰酸钾溶液褪色
B.分子式为C4H7ClO2,可与NaHCO3产生CO2的有机物可能结构有3种
C.![]() 分子中至少有11个碳原子处于同一平面上
分子中至少有11个碳原子处于同一平面上
D.1mol有机物 一定条件下能和7molNaOH反应
一定条件下能和7molNaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是![]()
A.棉花、麻、羊毛、蚕丝的主要化学成分都是蛋白质
B.淀粉、纤维素、氨基酸、蛋白质在一定条件下都能水解
C.皂化反应完全后,向反应液中加入热的饱和食盐水,容器底部有固体析出
D.可用水鉴别乙醇、苯和四氯化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,某浓度H3PO4溶液中逐滴加入NaOH溶液,滴加过程中各种含磷微粒的物质的量分数![]() 随溶液pH的变化曲线如下图所示。下列说法正确的是( )
随溶液pH的变化曲线如下图所示。下列说法正确的是( )
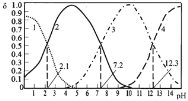
A.曲线1和曲线2分别表示![]() (H3PO4)和
(H3PO4)和![]() (HPO42-)的变化
(HPO42-)的变化
B.25℃时,H3PO4的电离常数K1=10-2.1
C.pH=7.2时,溶液中c(H2PO4-)+c(HPO42-)+c(OH-)=c(Na+)+c(H+)
D.pH=12.3时,溶液中由水电离出的c(H+)=10-12.3 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在10 mL0.1 mol/L Na2CO3溶液中逐滴加入0.1 mol/LHCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示(CO2因逸出未两出,忽略因气体逸出引起的溶液体积变化),下列说法不正确的是( )
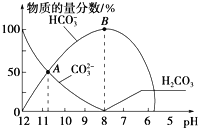
A.在0.1 mol/L Na2CO3溶液中:c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-)
B.在B点所示的溶液中,浓度最大的离子是Na+
C.在A点所示的溶液中:c(CO32-)=c(HCO3-)>c(H+)>c(OH-)
D.当溶液的pH为7时,溶液的总体积为20mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)冬季是雾霾的高发季节,天气预报会及时发布PM2.5的污染警报。
①下列行为不会增加城市大气中PM2.5浓度的是______(填字母)。
a.燃放烟花爆竹 b.为城市主干道洒水保洁 c.露天焚烧落叶
②雾霾会刺激呼吸道,使人易患流行性感冒。感冒发烧病人可服用______(填字母)药品进行治疗。
a.补血剂 b.抗酸药 c.阿司匹林
③维生素C可增强人体的免疫力。维生素C具有的性质是______(填字母)。
a.还原性 b.常温下不溶于水 c.溶液显碱性
(2)著名物理化学家张存浩院士在氟化氢(氘)激光器和水煤气合成液体燃料研究等方面做出了重要贡献。
①氟化氢(HF)的水溶液能腐蚀玻璃。该反应的化学方程式为______,制备普通玻璃的主要原料有SiO2、CaCO3、______(填化学式)。
②水煤气的主要成分是CO和H2,在40 MPa、380 ℃、锌铬氧化物作催化剂的条件下,用CO和H2合成液体燃料CH3OH,该反应的化学方程式为______。
(3)海底考察、水底打捞中均需要进行潜水作业。
①一种简易潜水器是潜水钟,由钢铁制成,在海水中会发生______腐蚀,反应中得到电子的物质是______。
②潜水员需要均衡的膳食结构。糖类、油脂、蛋白质都能为人体提供能量。油脂在人体中发生水解生成甘油和______;蛋白质在酶的作用下水解生成______,而被人体吸收。
③考察活动中会产生大量废水和垃圾。含汞离子废水需要处理后再排放,加入适量的硫化钠溶液能使汞离子变成______(填化学式)沉淀而除去;随便丢弃聚乙烯塑料膜会造成白色污染,聚乙烯的结构简式是______;如图是贴在某垃圾桶上的标志,该标志的含义是______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,往水中不断加入NaHC2O4固体,部分微粒浓度随加入的c(HC2O4-)的变化趋势如图所示。下列说法正确的是( )
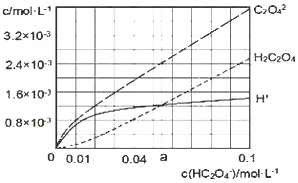
A.当c(HC2O4-)=0.1 mol/L时,c(H+)>c(C2O42-)-c(H2C2O4)
B.当c(HC2O4-)>a mol/L时,c(H+)<c(H2C2O4),HC2O4-的水解程度大于电离程度
C.HC2O4-![]() C2O42-+H+,Ka(HC2O4-)=a
C2O42-+H+,Ka(HC2O4-)=a
D.将0.08 mol/LH2C2O4溶液与等浓度NaOH溶液等体积混合后(忽略体积变化),c(Na+)>c(HC2O4-)>c(C2O42-)>c(H2C2O4)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食盐是日常生活的必需品,也是重要的化工原料。
(1)粗食盐中常含有少量K+、Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaCl的流程如下:

提供的试剂:饱和Na2CO3溶液 饱和K2CO3溶液 NaOH溶液 BaCl2溶液 Ba(NO3)2溶液 75%乙醇 四氯化碳
①欲除去溶液Ⅰ中的Ca2+、Mg2+、Fe3+、SO42-,选出a所代表的试剂,按滴加顺序依次为________(只填化学式)。
②分离操作①中所用到的玻璃仪器有____________。
③洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为________。
(2)用提纯的NaCl配制450 mL 4.00 mol·L-1NaCl溶液,所用仪器除药匙、烧杯、玻璃棒外还有________(填仪器名称)。
(3)在实验中多次用到玻璃棒,其作用有三个,分别是______________、______________、______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量纯净的氨基甲酸铵置于密闭真空恒容容器中(固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)![]() 2NH3(g)+CO2(g)。判断该分解反应已经达到化学平衡状态的是( )
2NH3(g)+CO2(g)。判断该分解反应已经达到化学平衡状态的是( )
A. 2v(NH3)=v(CO2) B. 密闭容器中c(NH3)∶c(CO2)=2∶1
C. 密闭容器中混合气体的密度不变 D. 密闭容器中氨气的体积分数不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com