
【题目】25℃时,某浓度H3PO4溶液中逐滴加入NaOH溶液,滴加过程中各种含磷微粒的物质的量分数![]() 随溶液pH的变化曲线如下图所示。下列说法正确的是( )
随溶液pH的变化曲线如下图所示。下列说法正确的是( )
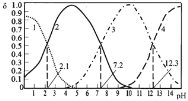
A.曲线1和曲线2分别表示![]() (H3PO4)和
(H3PO4)和![]() (HPO42-)的变化
(HPO42-)的变化
B.25℃时,H3PO4的电离常数K1=10-2.1
C.pH=7.2时,溶液中c(H2PO4-)+c(HPO42-)+c(OH-)=c(Na+)+c(H+)
D.pH=12.3时,溶液中由水电离出的c(H+)=10-12.3 mol/L
【答案】B
【解析】
A.起始时段附近浓度较高的为H3PO4,随着pH缓慢增大,溶液中H3PO4浓度降低,H2PO4-浓度增大,然后H2PO4-浓度降低,HPO42-浓度增大,然后HPO42-浓度降低,PO43-浓度增大,所以曲线1表示δ(H3PO4),曲线2表示δ(H2PO4-),曲线3表示δ(HPO42-),曲线4表示δ(PO43-),A错误;
B.根据图象,溶液中c(H3PO4)=c(H2PO4-)时,即δ(H3PO4)=δ(H2PO4-),溶液的pH=2.1,则H3PO4的电离常数K1=c(H+)=10-2.1,B正确;
C.pH=7.2时,溶液中溶液中δ(H2PO4-)=δ(HPO42-),则c(H2PO4-)=c(HPO42-),溶液中存在电荷守恒:c(Na+)+c(H+)=c(H2PO4-)+2c(HPO42-)+3c(PO43-)+c(OH-),C错误;
D.pH=12.3时,溶液中δ(HPO42-)=δ(PO43-),则c(HPO42-)=c(PO43-),溶液中c(H+)=10-12.3mol/L,H+由HPO42-及H2O共同电离产生而来,D错误;
故合理选项是B。


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案科目:高中化学 来源: 题型:
【题目】N2O5是一种新型硝化剂,在一定温度下可发生如下反应:2N2O5(g)4NO2(g)+O2(g)△H>0.T1温度时,向密闭容器中通入N2O5气体,部分实验数据见下表:
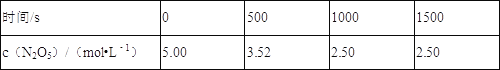
下列说法正确的是( )
A.500_s内NO2的生成速率为2.96×10﹣3_molL﹣1s﹣1
B.T1温度下该反应平衡时N2O5的转化率为29.6%
C.达到平衡其他条件不变,将容器的体积压缩到原来1/2,则c(N2O5)<5.00molL﹣
D.T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1>K2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:
①H2(g)+![]() O2(g)=H2O(l) △H=-285.8 kJ·mol-1
O2(g)=H2O(l) △H=-285.8 kJ·mol-1
②H2O(g)=H2(g)+![]() O2(g) △H=+241.8 kJ·mol-1
O2(g) △H=+241.8 kJ·mol-1
③C(s)+![]() O2(g)= CO(g) △H=-110.5 kJ·mol-1
O2(g)= CO(g) △H=-110.5 kJ·mol-1
④CO2(g)=C(s)+O2(g) △H=+393.5 kJ·mol-1
回答下列问题:
(1)上述反应中属于放热反应的是_________________________。
(2)H2的燃烧热为____________,C的燃烧热为_____________。
(3)CO燃烧时的热化学反应方程式为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下将NaOH溶液滴入二元弱酸H2X溶液中,混合溶液中的离子浓度与溶液pH的变化关系如图所示。下列叙述正确的是( )
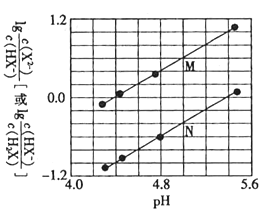
A.Ka1(H2X)的数量级为![]()
B.曲线N表示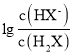 与pH的变化关系
与pH的变化关系
C.NaHX溶液中:c(H+)<c(OH-)
D.当混合物呈中性时,c(Na+)>c(X2-)>c(HX-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】多晶硅是制作光伏电池的关键材料。将SiCl4氢化为SiHCl3的热化学方程式为:3SiCl4+2H2(g)+Si(s)![]() 4SiHCl3(g) △H2<0
4SiHCl3(g) △H2<0
(1)该反应是____________反应(填吸热、放热)
(2)在相同条件,相同时间t时,不同温度下该反应中SiCl4转化率如图所示。下列叙述正确的是________________(填序号)。
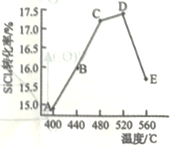
a.相同时间t内,A点的平均反应速率大于B点
b.相同时间t时,B点:v正>v逆
c.相同时间t时,v逆:C点大于A点
d.工业生产中采用了适宜温度:480~520°C
(3)为了增大化学反应速率,除加入催化剂、升高温度外还可以采用哪些方法和措施:___。(只写出一条)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,c(CH3COOH)+c(CH3COO-)=0.1mol·L-1的醋酸、醋酸钠混合溶液中,c(CH3COOH)、c(CH3COO-)与pH的关系如图所示。下列有关该溶液的叙述不正确的是( )
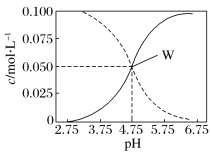
A. pH=5的溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-)
B. 溶液中:c(H+)+c(Na+)=c(CH3COO-)+c(OH-)
C. 由W点可以求出25℃时CH3COOH的电离常数
D. pH=4的溶液中:c(H+)+c(Na+)+c(CH3COOH)-c(OH-)=0.1mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,由醋酸和醋酸钠按一定比例混合形成的溶液始终保持c(CH3COOH) +c(CH3COO-)= 0.1mol/L,该溶液中c(CH3COOH)、c(CH3COO-)与pH的关系如下图所示,下列有关该溶液的叙述中正确的是
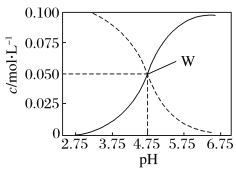
A.pH=5的溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-)
B.W点所表示的溶液中:c(Na+)=c(CH3COOH)
C.pH=3的溶液中:c(H+)+c(Na+)+c(CH3COOH)=0.1mol/L
D.据图像可求得该温度下CH3COOH的电离常数Ka=10-4.75
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三硫化磷(P4S3)是黄绿色针状晶体,易燃、有毒,分子结构之一如图所示,已知其燃烧时P被氧化为P4O10,下列有关P4S3的说法中不正确的是( )
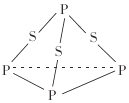
A.P4S3属于共价化合物
B.1mol P4S3分子中含有9mol共价键
C.P4S3充分燃烧的化学方程式为P4S3+8O2![]() P4O10+3SO2
P4O10+3SO2
D.P4S3中磷元素为+3价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2O5是一种新型硝化剂,在一定温度下可发生以下反应:
2N2O5(g)![]() 4NO2(g)+ O2(g) ΔH>0
4NO2(g)+ O2(g) ΔH>0
T1温度时,向密闭容器中通入N2O5,部分实验数据见下表:
时间/s | 0 | 500 | 100 0 | 150 0 |
c(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.50 | 2.50 |
下列说法中不正确的是
A.500 s内N2O5分解速率为2.96╳10-3mol·L-1·s-1
B.T1温度下的平衡常数为K1=125,平衡时N2O5的转化率为50%
C.T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1<K2
D.达平衡后其他条件不变,将容器的体积压缩到原来的1/2,则c(N2O5)> 5.00 mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com