
【题目】2019年国际非政府组织“全球计划”12月4日发布报告:研究显示,全球二氧化碳排放量增速趋缓。CO2的综合利用是解决温室问题的有效途径。
(1)CO2催化加氢制甲醇的有关反应及其在不同温度下的化学平衡常数如下表所示。
化学反应 | 平衡常数 | ||
500℃ | 700℃ | 800℃ | |
Ⅰ.H2(g)+CO2(g) H2O(g)+CO(g) | 1.0 | 1.70 | 2.52 |
Ⅱ.2H2(g)+CO(g) CH3OH(g) | 2.5 | 0.34 | 0.15 |
Ⅲ.3H2(g)+CO2(g) CH3OH(g)+H2O(g) ΔH | |||
①ΔH___0(填“>”、“<”或“=”)。
②已知反应Ⅲ的速率方程式:υ正=k正·c3(H2)·c(CO2),υ逆=k逆·c(CH3OH)·c(H2O),k正、k逆为速率常数。反应达到平衡后,仅升高温度,k正增大的倍数___k逆增大的倍数(填“大于”、“小于”或“等于”)。
③500℃时,向恒容的密闭容器中加入1molCO2和1molH2,控制反应条件只发生反应Ⅰ。达到平衡后,只改变下列条件,能使CO的平衡体积分数增大的是___(填选项字母)。
A.增大压强 B.降低温度 C.再通入等物质的量CO2和H2 D.分离出部分水
(2)在200℃时,向5L带气压计的恒容密闭容器中通入2molCO2和2molCH4发生反应CH4(g)+CO2(g)2H2(g)+2CO(g),测得初始压强为P0kPa,反应过程中容器内总压强(P)随时间(t)变化(反应达到平衡时的温度与起始温度相同)如图所示。
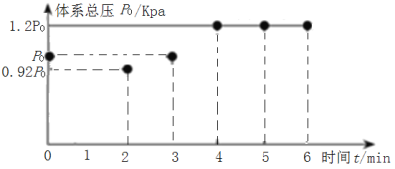
①该反应过程中从0min到2min压强变化原因是___。
②0~4min内,反应的平均反应速率υ(CO2)=___。
③用平衡分压代替平衡浓度表示的化学平衡常数Kp=___。[气体分压(p分)=气体总压(p总)×气体体积分数]
(3)科学家提出利用CO2与CH4制备“合成气”(CO、H2)可能的反应历程如图所示。
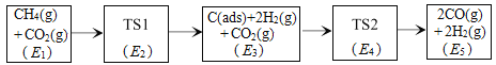
注:C(ads)为吸附性活性炭,方框内包含微粒种类及数目、微粒的相对总能量[如第一个方框中1个CH4(g)+1个CO2(g)的相对总能量为E1eV,单位:eV]。其中,TS表示过渡态。
①CH4(g)+CO2(g) 2H2(g)+2CO(g)ΔH=___kJ·mol-1(已知:1eV=1.6×10-22kJ)
②若E4+E1<E3+E2,则决定制备“合成气”反应速率的反应方程式为___。
【答案】< 小于 D 反应为吸热反应,温度降低使体系压强减小 0.02mol·L-1·min-1 0.01P02(kPa)2 96.32(E5-E1)或1.6×10-22NA(E5-E1) CH4(g)=C(ads)+2H2(g)或CH4(g)+CO2(g)=C(ads)+2H2(g)+CO2(g)
【解析】
根据平衡常数表达式和温度对平衡常数的影响判断,根据温度对化学平衡的影响判断反应Ⅲ的移动方向,选择使反应Ⅰ正向移动方向的措施。列出“三段式”计算反应速率和平衡常数。利用盖斯定律计算出焓变的大小。计算出活化能较高的反应是决速反应。
①Ⅰ.H2(g)+CO2(g)H2O(g)+CO(g),K1=![]() ;
;
Ⅱ.2H2(g)+CO(g) CH3OH(g),K2=![]() ;
;
Ⅲ=Ⅰ+Ⅱ,3H2(g)+CO2(g) CH3OH(g)+H2O(g) K3=![]() =K1×K2,根据表中数据依次计算出500℃、700℃、800℃的K3依次为2.5、0.578、0.378,温度越高,K3越小,故ΔH<0;
=K1×K2,根据表中数据依次计算出500℃、700℃、800℃的K3依次为2.5、0.578、0.378,温度越高,K3越小,故ΔH<0;
②已知反应Ⅲ:3H2(g)+CO2(g) CH3OH(g)+H2O(g) ΔH<0 ,反应达到平衡后,仅升高温度,正逆反应速率都增大,平衡逆向移动,正反应速率增大的倍数比逆反应速率增大的倍数小,υ正=k正·c3(H2)·c(CO2)<υ逆=k逆·c(CH3OH)·c(H2O),即k正增大的倍数小于k逆增大的倍数;
③反应Ⅰ.H2(g)+CO2(g) H2O(g)+CO(g) ,升高温度平衡常数增大,则反应I的ΔH>0,
A.增大压强,平衡不移动,CO的平衡体积分数不变,故A不符合题意;
B.降低温度,平衡逆向移动,CO的平衡体积分数减小,故B不符合题意;
C.再通入等物质的量CO2和H2,相当于增大压强,平衡不移动,CO的平衡体积分数不变,故C不符合题意;
D.分离出部分水,平衡正向移动,能使CO的平衡体积分数增大,故D符合题意;
答案选D。
(2)在200℃时,向5L带气压计的恒容密闭容器中通入2molCO2和2molCH4发生反应CH4(g)+CO2(g)2H2(g)+2CO(g),测得初始压强为P0kPa,
①图中可以看出,该反应过程中从0min到2min压强减小,原因是该反应为吸热反应,温度降低使体系压强减小;
②4min后压强不再变化,说明4min时已经达到平衡,设从起始到平衡转化CH4物质的量为xmol,用三段式
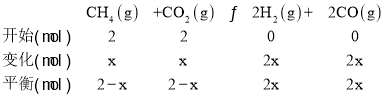
由图中数据可以看出平衡时的总压强为1.2P0kPa,起始总压强为P0kPa,气体的压强之比等于物质的量之比,![]() ,解得x=0.4,平衡时气体的总物质的量等于4mol+2xmol=4mol+2×0.4mol=4.8mol,0~4min内,反应的平均反应速率υ(CO2)=
,解得x=0.4,平衡时气体的总物质的量等于4mol+2xmol=4mol+2×0.4mol=4.8mol,0~4min内,反应的平均反应速率υ(CO2)=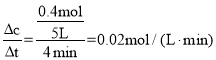 ;
;
③用平衡分压代替平衡浓度表示的化学平衡常数Kp=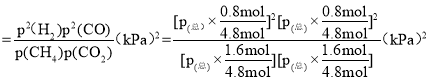
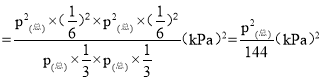 =
=![]() ;
;
(3) ①根据流程图可知,第一步:CH4(g) 2H2(g)+ C(ads) ΔH1= (E3- E1span>)NAeV;
第二步:CO2(g)+C(ads)2CO(g) ΔH2= (E5 - E3) NAeV;
第一步加第二步得到:CH4(g)+CO2(g)2H2(g)+2CO(g)ΔH=(E5-E1) NAeV=1.6×10-22NA (E5-E1) kJ或96.32 (E5-E1) kJ;
②决速步骤,指反应历程中反应速率最慢的反应;速率快慢则由反应的活化能决定,活化能越大,反应速率越慢;若E4+E1<E3+E2,则E2-E1>E4-E3,则决定制备“合成气”反应速率的反应方程式为:CH4(g)=C(ads)+2H2(g)或CH4(g)+CO2(g)=C(ads)+2H2(g)+CO2(g)。


科目:高中化学 来源: 题型:
【题目】某微生物电池在运行时可同时实现净化有机物污水、净化含![]() 废水(pH约为6)和淡化食盐水,其装置示意图如图所示。图中,D和E为离子交换膜,Z为待淡化食盐水。(已知Cr3+完全沉淀所需的pH为5.6)下列说法不正确的是
废水(pH约为6)和淡化食盐水,其装置示意图如图所示。图中,D和E为离子交换膜,Z为待淡化食盐水。(已知Cr3+完全沉淀所需的pH为5.6)下列说法不正确的是
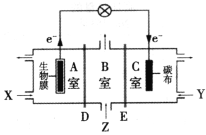
A.E为阴离子交换膜
B.X为有机物污水,Y为含![]() 废水
废水
C.理论上处理1 mol的![]() 的同时可脱除3 mol的NaC1
的同时可脱除3 mol的NaC1
D.C室的电极反应式为![]() +6e-+8H+==2Cr(OH)3↓+H2O
+6e-+8H+==2Cr(OH)3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物A、B是中学常见的物质,其阴阳离子可从表中选择.
阳离子 | K+、Na+、NH4+、Fe2+、Ba2+、Cu2+ |
阴离子 | OH﹣、I﹣、NO3﹣、AlO2﹣、HCO3﹣、HSO4﹣ |
(1)若A的水溶液为无色,B的水溶液呈碱性,A、B的水溶液混合后,只产生不溶于稀硝酸的白色沉淀及能使湿润的红色石蕊试纸变蓝的气体,则:
①A中的化学键类型为_________(填“离子键”、“共价键”).
②A、B溶液混合后加热呈中性,该反应的离子方程__________________________ .
(2)若A的水溶液为浅绿色,B的焰色反应呈黄色.向A的水溶液中加入稀盐酸无明显现象,再加入B后溶液变黄,但A、B的水溶液混合后无明显变化.则:
①A的化学式为__________________________ .
②经分析上述过程中溶液变黄的原因可能有两种(请用文字叙述)
Ⅰ._______________________.Ⅱ._________________________.
③请用一简易方法证明上述溶液变黄的原因_________________________.
④利用上述过程中溶液变黄原理,将其设计成原电池,若电子由a流向b,则b极的电极反应式为_.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用除去表面氧化膜的细铝条紧紧缠绕在温度计上(如图),将少许硝酸汞溶液滴到铝条表面,置于空气中,很快铝条表面产生“白毛”,且温度明显上升。下列分析错误的是

A.Al和O2化合放出热量B.硝酸汞是催化剂
C.涉及了:2Al+3Hg2+→2Al3++3HgD.“白毛”是氧化铝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知3CuO+2NH3![]() 3Cu+N2+3H2O。下列判断正确的是
3Cu+N2+3H2O。下列判断正确的是
A.N元素的化合价降低B.NH3被还原
C.消耗0.3 mol CuO转移0.6 NA个电子D.CuO是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下面两种方法可以制得白色的Fe(OH)2沉淀。
方法一:用不含Fe3+的FeSO4溶液与用不含O2的蒸馏水配制的NaOH溶液反应制备。
(1)用硫酸亚铁晶体配制上述FeSO4溶液时还需加入__。
(2)除去蒸馏水中溶解的O2常采用___的方法。
(3)生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,这样操作的理由是__。
方法二:在如图装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备。
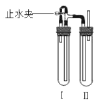
(1)在试管I里加入的试剂是___。
(2)在试管II里加入的试剂是___。
(3)为了制得白色Fe(OH)2沉淀,在试管I和II中加入试剂,打开止水夹,塞紧塞子后的实验步骤是:先___,后__。
(4)这样生成的Fe(OH)2沉淀能较长时间保持白色,其理由是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上已经实现CO2与H2反应合成甲醇。在一恒温、恒容密闭容器中充入2molCO2和6molH2,一定条件下发生反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。请回答:

(1)该密闭容器的容积是___。
(2)达到未平衡状态的时刻是___min(填“3”或“10”)。
(3)在前3min内,用H2浓度的变化表示的反应速率v(H2)=___mol/(L·min)。
(4)10min时体系的压强与开始时压强之比为__。
(5)达平衡后H2O(g)的物质的量分数是___。
(6)已知:①CO(g)+2H2(g)=CH3OH(g) △H=-90.1kJ/mol,②CO(g)+H2O(g)=CO2(g)+H2(g)△H=-41.1kJ/mol,则CO2与H2反应合成CH3OH(g)的热化学方程式__,反应在10min内所放出的热量为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
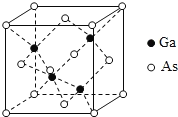
【题目】2019年1月3日上午,嫦娥四号探测器翩然落月,首次实现人类飞行器在月球背面的软着陆。所搭载的“玉兔二号”月球车,通过砷化镓(GaAs)太阳能电池提供能量进行工作。回答下列问题:
(1)基态As原子的价电子排布图为____________,基态Ga原子核外有________个未成对电子。
(2)镓失去电子的逐级电离能(单位:kJmol-1)的数值依次为577、1985、2962、6192,由此可推知镓的主要化合价为____和+3,砷的电负性比镓____(填“大”或“小”)。
(3)1918年美国人通过反应:HC≡CH+AsCl3![]() CHCl=CHAsCl2制造出路易斯毒气。在HC≡CH分子中σ键与π键数目之比为________;AsCl3分子的空间构型为___________。
CHCl=CHAsCl2制造出路易斯毒气。在HC≡CH分子中σ键与π键数目之比为________;AsCl3分子的空间构型为___________。
(4)砷化镓可由(CH3)3Ga和AsH3在700℃制得,(CH3)3Ga中碳原子的杂化方式为_______
(5)GaAs为原子晶体,密度为ρgcm-3,其晶胞结构如图所示, Ga与As以_______键键合。Ga和As的原子半径分别为a pm和b pm,设阿伏伽德罗常数的值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为_______________(列出计算式,可不化简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胡椒酚是植物挥发油中的一种成分。关于胡椒酚的下列说法其中正确的是( )
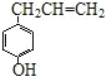
①该化合物属于芳香烃;②分子中至少有7个碳原子处于同一平面;③它存在能发生银镜反应的同分异构体;④1mol该化合物最多可与4mol H2发生加成反应
A.①③B.①②④C.②③D.②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com