
| 1 |
| 5 |

| 1 |
| 5 |
| 0.028g |
| 14g/mol |
| 200ml |
| 500ml |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 2 |
| A��ͨH2��һ����������ͨO2��һ���Ǹ��� |
| B��ͨO2��һ����������ͨH2��һ���Ǹ��� |
| C������һ��ʱ���������ҺpH���� |
| D���˵���ܷ�������ɫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A�������ӵĽṹʾ��ͼ�� | ||
B����Ϊ���ԭ�������ⶨ����̼���أ�
| ||
C���Ȼ�þ�ĵ���ʽ�� | ||
D���õ���ʽ��ʾ�Ȼ�����ӵ��γɹ��̣� + + �� ��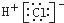 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��lH��2H��3HΪͬ�������� |
| B��lH��2H��3H����������ͬ |
| C��lH��2H��3H��Ϊͬλ�� |
| D��lH��2H��3H����������ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ݳ��������ü�ʯ�����գ�����b�ˣ���xƫС |
| B����������Һ�������ɲ����������أ���c�˹��壬������ʱ�й���ɽ���ȥ��xƫ�� |
| C��ijNaOH����Һ¶���ڿ�����һ��ʱ����Լ���Ϊָʾ���ζ�������Ӧ�����Һ����xƫС |
| D��������������ȴ�����º����ⶨ�����ʱδ��ƽ�����ܺ�ˮ����Һ�棬��xƫС |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ||
| ������ | Fe ��OH��3 | Zn��OH��2 |
| pH | 1.5��3.2 | 6.4��8.0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ��Ӧ���� | |
| ʵ����� | |
| �Թ��з�����Ӧ�����ӷ���ʽ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com