
| A、蛋白质溶液中加入饱和(NH4)2SO4溶液,蛋白质析出,再加水也不溶解 |
| B、人工合成的具有生命活性的蛋白质-结晶牛胰岛素是1965年我国科学家最先合成的 |
| C、重金属盐能使蛋白质变性,所以误食重金属盐会中毒 |
| D、浓HNO3溅在皮肤上,使皮肤呈黄色,是由于浓HNO3和蛋白质发生颜色反应 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 L 0.1 mol?L-1 (NH4)2Fe(SO4)2?6H2O溶液中:c(NH4+)+c(Fe2+)+c(H+)=c(OH-)+c(SO42-) |
| B、0.1 mol?L-1的NH4Cl与0.1 mol?L-1的NH3?H2O等体积混合:c(NH4+)+2c(H+)=c(NH3?H2O)+2c(OH-) |
| C、pH=9.4、浓度均为0.1 mol?L-1的HCN与NaCN的混合溶液中:c(Na+)>c(CN-)>c(HCN)>c(OH-) |
| D、0.1 mol?L-1 CH3COONa 溶液与0.05 mol?L-1盐酸等体积混合后的酸性溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v(A)=0.01 mol/(L?s) |
| B、v(B)=0.04 mol/(L?s) |
| C、v(B)=0.60mol/(L?min) |
| D、v(C)=1.0mol/(L?min) |
查看答案和解析>>
科目:高中化学 来源: 题型:
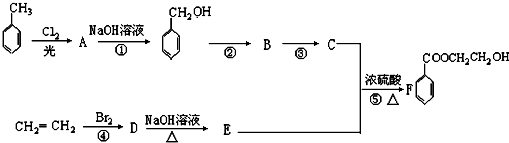
 煤是重要的能源,也是生产化工产品的重要原料.试用所学知识,解答下列问题:
煤是重要的能源,也是生产化工产品的重要原料.试用所学知识,解答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.01mol/L NH4Al(SO4)2溶液与0.02mol/L Ba(OH)2溶液等体积混合NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3?H2O | ||||
| B、Na2O2加入H218O中:2Na2O2+2H218O=4Na++4OH-+18O2↑ | ||||
C、NH4HCO3溶液与过量NaOH溶液共热:NH4++OH-
| ||||
D、浓硝酸中加入过量铁粉并加热:Fe+3NO3-+6H+
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、相同浓度的两溶液中由水电离出的c(H+)相同 |
| B、pH=12与pH=2的两溶液稀释100倍,pH都变化2个单位 |
| C、用20mL0.1mol/L的氢氧化钠滴定未知浓度的醋酸,选用酚酞作指示剂 |
| D、两溶液相互反应生成1molH2O的中和热为57.3kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.08mol?L-1 |
| B、0.12 mol?L-1 |
| C、0.05 mol?L-1 |
| D、0.14mol?L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com