
【题目】下表是某加碘盐包装袋上的部分文字说明:根据这一说明某学生作出如下判断,其中正确的是
配料 | 氯化钠 |
含碘量 |
|
使用方法 | 勿长时间炖炒,食品熟后加入 |
A.此食盐是纯净物
B.“勿长时间炖炒”的原因可能是碘酸钾受热不稳定
C.仅用淀粉溶液就可以检验此食盐中是否含碘
D.1kg此食盐中含碘酸钾![]()
科目:高中化学 来源: 题型:
【题目】(1)写出有机物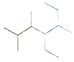 的名称____________________。
的名称____________________。
(2)分子式为C8H10属于芳香烃的同分异构体共有________种,其中________(结构简式)在苯环上的一氯代物有两种。
(3)有机物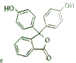 中含氧官能团的名称是____________________。
中含氧官能团的名称是____________________。
(4)分子式为C6H10的某烃是含有双键的链状结构,分子中无支链或侧链,且分子中不存在![]() 基团,则其可能的结构简式为____________________(任写一种)
基团,则其可能的结构简式为____________________(任写一种)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于热化学反应的描述中正确的是()
A.已知H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3kJ·mol-1,则H2SO4和Ba(OH)2反应的ΔH=2×(-57.3)kJ·mol-1
B.将甲醇蒸气转化为氢气的热化学方程式是CH3OH(g)+![]() O2(g)=CO2(g)+2H2(g)ΔH=-192.9kJ·mol-1,则CH3OH(g)的燃烧热为192.9kJ·mol-1
O2(g)=CO2(g)+2H2(g)ΔH=-192.9kJ·mol-1,则CH3OH(g)的燃烧热为192.9kJ·mol-1
C.H2(g)的燃烧热为285.8kJ·mol-1,则2H2O(g)=2H2(g)+O2(g) ΔH=+571.6kJ·mol-1
D.葡萄糖的燃烧热是2800kJ·mol-1,则![]() C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l) ΔH=-1400kJ·mol-1
C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l) ΔH=-1400kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有①、②、③、④四种元素的基态原子的电子排布式如下:①![]() ;②
;②![]() ;③
;③![]() ;④
;④![]() 。则下列有关比较中不正确的是
。则下列有关比较中不正确的是
A.电负性:④>③>②>①
B.最高正化合价:③>②>①>④
C.原子半径:①>②>③>④
D.第一电离能:④>③>②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验操作、现象和解释或结论都正确的是
选项 | 实验操作 | 现象 | 解释或结论 |
A | 向 | 出现白色沉淀,最终沉淀没溶解 | Y可能是 |
B | 常温下,将铁片浸入足量浓硫酸中 | 铁片不溶解 | 常温下,铁与浓硫酸一定没有发生化学反应 |
C | 向某食盐溶液中滴加淀粉溶液 | 溶液颜色不变 | 该食盐为非加碘食盐 |
D | 将 | 有白色沉淀 |
|
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】异丁烯与氯化氢可能发生的两种加成反应及相应的能量变化与反应过程如下图所示,下列说法错误的是( )


A.活化能:反应①大于反应②
B.中间产物的稳定性:中间体1小于中间体2
C.产物的能量:产物1大于产物2
D.△H大小:反应①小于反应②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
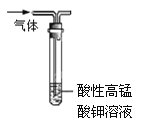
A.用如图装置除去乙烷中混有的乙烯
B.配制一定物质的量浓度的溶液,定容时仰视刻度,溶液浓度偏大
C.制备乙酸乙酯时,将乙醇和乙酸依次加入浓硫酸中
D.玻璃仪器洗涤干净的标准是:附着在仪器内壁上的水既不聚集成滴,也不成股流下
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列图示的说法中正确的是( )
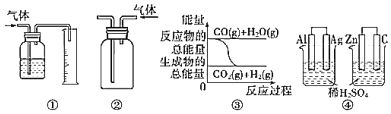
A.用图①所示装置测量气体的体积
B.用图②所示实验装置排空气法收集CO2气体
C.图③表示可逆反应CO(g)+H2O(g)![]() CO2(g)+H2(g)是放热反应
CO2(g)+H2(g)是放热反应
D.图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量也相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】稀氨水中存在电离平衡NH3·H2O ![]() NH4++OH-,下列叙述正确的是
NH4++OH-,下列叙述正确的是
A.加水稀释后,溶液中c (H+)减小
B.通入少量HCl(g)后,溶液中c(NH4+)减小
C.加入少量浓氨水,电离平衡逆向移动
D.加入少量NH4Cl固体,溶液的pH减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com