
(6分)一定量氢气在氯气中燃烧,所得混合气体用100 mL 2.00 moL·L-1NaOH溶液恰好完全吸收,测得溶液中含有NaClO的物质的量为0.05mol。试计算下列问题:
(1)所得溶液中Cl-的物质的量为 ;
(2)所用氯气和参加反应的氢气的物质的量之比n(C12):n(H2)为 ;
科目:高中化学 来源:2016届江苏省无锡市高三上学期10月月考化学试卷(解析版) 题型:填空题
(12分)利用铝灰(主要成分为Al、Al2O3、AlN、FeO等)制备铝鞣剂[主要成分为Al(OH)2Cl]的一种工艺如下:
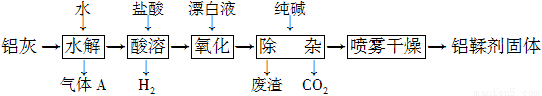
(1)气体A能使湿润的红色石蕊试纸变蓝。铝灰在90 ℃水解生成A的化学方程式为____________。“水解”采用90 ℃而不在室温下进行的原因是________________。
(2)“酸溶”时,Al2O3发生反应的离子方程式为 。
(3)“氧化”时,发生反应的离子方程式为 。
(4)“废渣”成分为______________(填化学式)。
(5)采用喷雾干燥而不用蒸发的原因是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高一上学期9月月考化学试卷(解析版) 题型:选择题
下列物质中,含原子数最多的是
A. 0.1mol氯化氢 B. 0.4g甲烷
C. 3.4gH2S D. 6.02×1022个氢分子
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省高二上学期第一次联考化学试卷(解析版) 题型:选择题
下列各组热化学方程式中,△H1>△H2的是
①C(s)+O2(g)===CO2(g) △H1 C(s)+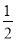 O2(g)===CO(g) △H2
O2(g)===CO(g) △H2
②S(s)+O2(g)===SO2(g) △H1 S(g)+O2(g)===SO2(g) △H2
③H2(g)+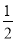 O2(g)===H2O(l) △H1 2H2(g)+O2(g)===2H2O(l) △H2
O2(g)===H2O(l) △H1 2H2(g)+O2(g)===2H2O(l) △H2
④CaCO3(s)===CaO(s)+CO2(g) △H1 CaO(s)+H2O(l)===Ca(OH)2(s) △H2
A.① B.②③④ C.④ D.①②③
查看答案和解析>>
科目:高中化学 来源:2016届江西省红色七校高三上学期第一次联考化学试卷(解析版) 题型:实验题
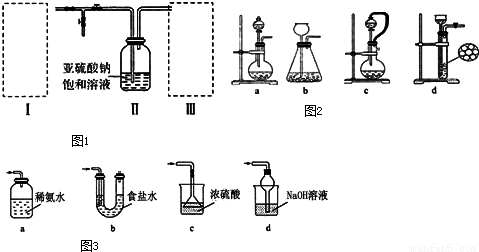
(10分)焦亚硫酸钠(Na2S2O5)为白色或黄色结晶粉末或小结晶。其性质活泼,具有强还原性,在食品加工中作防腐剂、漂白剂、疏松剂。某实验小组拟采用如图1装置(实验前已除尽装置内的空气)来制取焦亚硫酸钠(Na2S2O5).
(1)装置I是用亚硫酸钠固体和浓硫酸制备二氧化硫气体,该装置中反应的化学方程式为 .如果想控制反应速度,如图2中可选用的发生装置是 (填写字母).
(2)装置Ⅱ中发生反应的化学方程式为:2 NaHSO3=Na2S2O5 + H2O,当有Na2S2O5晶体析出,要获得已析出的晶体可采取的分离方法是 ;某同学需要420mL0.1mol/L焦亚硫酸钠溶液来研究其性质,配制时需称量焦亚硫酸钠的质量为 ;配制时除用到托盘天平、药匙、烧杯、玻璃棒等仪器外,还必须用到的玻璃仪器是 .
(3)装置Ⅲ用于处理尾气,可选用如图3的最合理装置(夹持仪器已略去)为 (填序号).
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高一上学期第一次月考化学试卷(解析版) 题型:实验题
(8分)为证明Na2O2可作为潜水艇的供氧剂,某化学小组在实验室模拟CO2与Na2O2反应产生氧气的实验。
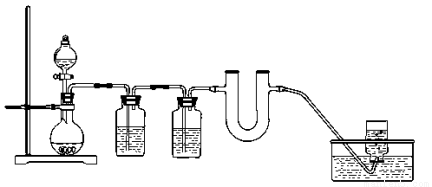
(1)生成CO2的化学反应方程式:
(2)饱和碳酸氢钠溶液的作用是除去CO2中混有的HCl气体,浓H2SO4的作用是
(3)u形管中的现象是 ,反应方程式为
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省临沂市高二上10月月考化学试卷(解析版) 题型:填空题
(1)在2L的密闭容器中,由CO2和H2合成甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g),在其他条件不变的情况下,探究温度对反应的影响,
CH3OH(g)+H2O(g),在其他条件不变的情况下,探究温度对反应的影响,
实验结果如图1所示(注:T2>T1,均大于300℃).
①温度为T2时,从反应开始到平衡,生成甲醇的平均反应速率为 .
②通过分析图1,温度对反应CO2(g)+3H2(g) CH3OH(g)+H2O(g)的影响可以概括为 .
CH3OH(g)+H2O(g)的影响可以概括为 .

③下列情形能说明上述反应已达到平衡状态的是 (填字母).
A.体系压强保持不变
B.密闭容器中CO2、H2、CH3OH(g)、H2O(g)4种气体共存
C.CH3OH与H2物质的量之比为1:3
D.每消耗1mol CO2的同时生成3mol H2
④已知H2(g)和CH3OH(l)的燃烧热△H分别为﹣285.8kJ·mol﹣1和﹣726.5kJ·mol﹣1,写出由CO2和H2生成液态甲醇和液态水的热化学方程式: .
(2)在容积可变的密闭容器中,由CO和H2合成甲醇CO(g)+2H2(g) CH3OH(g),CO在不同温度下的平衡转化率与压强的关系如图2所示.
CH3OH(g),CO在不同温度下的平衡转化率与压强的关系如图2所示.
①该反应的平衡常数表达式K=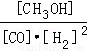 ,250℃、0.5×104 kPa下的平衡常数 (填“>”、“<”或“=”)300℃、1.5×104 kPa下的平衡常数.
,250℃、0.5×104 kPa下的平衡常数 (填“>”、“<”或“=”)300℃、1.5×104 kPa下的平衡常数.
②实际生产中,该反应条件控制在250℃、1.3×104 kPa左右,选择此压强而不选择更高压强的理由是 .
查看答案和解析>>
科目:高中化学 来源:2016届湖南省浏阳市高三上学期第二次月考化学试卷(解析版) 题型:推断题
(13分)尼龙是目前世界上产量最大、应用范围最广、性能比较优异的一种合成纤维。以X为原料合成高分子化合物尼龙-66的流程如下:

已知部分信息如下:
I.Z的化学式为C6H10O4。
Ⅱ.X和浓溴水反应产生白色沉淀。
Ⅲ.某些醛与醛之间能发生羟醛缩合反应,例如:
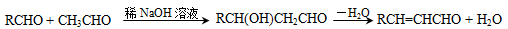
请回答下列问题:
(1)X的化学名称为____ __,W的结构简式为__________,T的分子式为 _____________。
(2)反应②的条件为______________________。
(3)上述反应中属于加成反应的有 。
(4)写出反应④的化学方程式________________________。
(5)满足下列条件的S的同分异构体的结构共有________种(不考虑立体异构),①单环芳香族化合物 ②既能发生银镜反应,又能发生水解反应其中,苯环上核磁共振氢谱上有2个峰的结构简式为_________________。
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三上学期第二次月考化学试卷(解析版) 题型:选择题
下列离子方程式错误的是
A.向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++SO42-===BaSO4↓+2H2O
B.酸性介质中KMnO4氧化H2O2:2MnO4-+5H2O2+6H+===2Mn2++5O2↑+8H2O
C.等物质的量的MgCl2、Ba(OH)2和HCl溶液混合:Mg2++2OH-===Mg(OH)2↓
D.铅酸蓄电池充电时的阳极反应:PbSO4+2H2O-2e-===PbO2+4H++SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com