
【题目】下列属于同位素的是
A.1H与2HB.14 C与14NC.O2与O3D.H2O和H2O2
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:
【题目】某学习小组拟探究CO2和锌粒反应是否生成CO,已知CO能与银氨溶液反应产生黑色固体。实验装置如图所示:
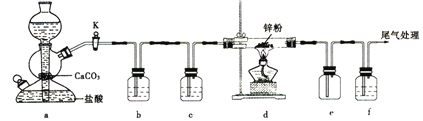
下列叙述正确的是
A. 装置e的作用是防倒吸
B. 如图所示装置的活塞K处于关闭状态
C. 实验结束时,先关闭活塞K,再熄灭酒精灯
D. b、c、f中的试剂依次为饱和碳酸钠溶液、浓硫酸、银氨溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关人体细胞组成元素的叙述,正确的是
A.人体不同细胞的元素种类和含量都大致相同
B.构成细胞的微量元素的含量少,生理作用也小
C.组成人体的元素在非生物界中都能找到
D.C是最基本元素,也是细胞鲜重中含量最多的元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酰氯(SO2Cl2)对眼和上呼吸道黏膜有强烈的刺激性,但其在工业上有重要作用。其与硫酸的部分性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 其他性质 |
SO2Cl2 | -54.1 | 69.1 | ①遇水易水解,产生大量白雾,生成两种强酸 ②易分解:SO2Cl2 |
H2SO4 | 10.4 | 338 | 强吸水性、稳定不易分解 |
实验室用干燥纯净的氯气和过量的二氧化硫在活性炭的催化作用下合成硫酰氯,反应方程式为:SO2(g)+Cl2(g)=SO2Cl2(1)H<0,其实验装置如图所示(夹持仪器已省略):

(1)仪器A的名称为____________,冷却水应该从______(填“a”或“b”)口进入。
(2)仪器B中盛放的药品是__________。
(3)实验时,装置戊中发生反应的化学方程式为____________。
(4)若缺少装置乙和丁,则硫酰氯会水解,硫酰氯水解的化学方程式为___________。
(5)反应一段时间后,需在丙装置的三颈瓶外面加上冷水浴装置,其原因是__________。
(6)实验开始时,戊中开始加入12.25gKC1O3,假设KC1O3在过量盐酸作用下完全转化为Cl2,实验结束后得到32.4g纯净的硫酰氯,则硫酰氯的产率为______。
(7)少量硫酰氯也可用氙磺酸(ClSO2OH)直接分解获得,反应方程式为:2ClSO2OH=H2SO4+SO2Cl2。
①在分解产物中分离出硫酰氯的实验操作名称是_____,现实验室提供的玻璃仪器有漏斗、烧杯、蒸发皿、酒精灯、接液管、锥形瓶,该分离操作中还需要补充的玻璃仪器是_____、_____、_____。
②分离出的产品中往往含有少量的H2SO4,请设计实验方案检验产品中有硫酸(可选试剂:稀盐酸、稀硝酸、BaCl2溶液、蒸馏水、紫色石蕊试液):___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于胶体和溶液的说法中,正确的是
A.许多胶体能进行电泳是因为这些胶体带电
B.在溶有 1mol 氢氧化铁的胶体中,含有 NA 个氢氧化铁胶粒
C.光线通过时,胶体产生丁达尔效应,溶液则无丁达尔效应
D.将饱和氯化铁溶液滴入稀氢氧化钠溶液中加热,可得氢氧化铁胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光催化技术是一种在能源和环境领域有着重要应用前景的绿色技术。Ti的某种晶型的氧化物M可用作光催化材料。
(1)基态Ti原子的价层电子排布图为________。
(2)在第四周期d区元素中,与Ti 原子未成对电子数相同的元素名称是________。
(3)金属钛的原子堆积方式如图1所示,则金属钛晶胞俯视图为_____。

(4)生活环境中的臭气源有氨气、甲硫醇(CH3-SH) 等,M 可以作为高效除臭剂。与氨气互为等电子体的阳离子为_____,甲硫醇中硫原子采取的杂化方式为_____,与S位于同一周期,且第一电离能小于S 的非金属元素符号为______,已知甲硫醇熔沸点小于甲醇(CH3OH),试解释此差异的主要原因___________。
(5)M 的晶胞结构如图2,M 化学式为______。
(6)石墨烯是单个原子厚度的二维碳纳米材料( 如图3),其比表面积大( 比表面积指单位质量物料所具有的总面积)。石墨烯与M 的结合使用,极大地提高了M 的光催化效果。在石墨烯晶体中,每个最小的六元环占有____个C 原子。已知石墨烯中C-C 键长为a pm,则单层石墨烯的比表面积为_____m2/g(NA表示阿伏伽德罗常数的数值,忽略碳原子的厚度)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一处于平衡状态的反应:X(s)+3Y(g) ![]() 2Z (g),ΔH<0。为了使平衡向生成Z的方向移动,应选择的条件是( )
2Z (g),ΔH<0。为了使平衡向生成Z的方向移动,应选择的条件是( )
①高温 ②低温 ③高压 ④低压 ⑤加催化剂 ⑥分离出Z
A.①③⑤
B.②③⑤
C.②③⑥
D.②④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列装置不能达到有关实验目的是( )

A. 用甲图装置证明ρ(煤油)< ρ(钠)< ρ(水)
B. 用乙图装置可以吸收氨气防止倒吸
C. 用丙图装置制取金属锰
D. 用丁装置比较NaHCO3和Na2CO3的热稳定性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是地壳中含量最多的金属元素,其单质和化合物广泛应用于日常生活中。
(1)铝粉和铁的氧化物(FeO-Fe2O3)可配成铝热剂用于焊接钢轨,反应的化学方程式是____。
(2)以铝土矿(主要成分为Al2O3.含SiO2和Fe2O3等杂质)为原料生产铝和铵明矾晶体[NH4Al(SO4)2·12H2O]的一种工艺流程如下(已知:SiO2在“碱溶”时转化为铝硅酸钠(NaAlSiO4·nH2O)沉淀)。

①实验前,要将铝土矿粉粹的目的是_______。
②用氧化物的形式表示铝硅酸钠的化学式________。
③步骤②涉及到的离子方程式是: _______。
④写出利用Al2O3制备金属Al的化学方程式: _______。
⑤若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的物质的量之比为1:1,则投料时铝土矿中的Al2O3和H2SO4的物质的量之比为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com