
【题目】下列有关人体细胞组成元素的叙述,正确的是
A.人体不同细胞的元素种类和含量都大致相同
B.构成细胞的微量元素的含量少,生理作用也小
C.组成人体的元素在非生物界中都能找到
D.C是最基本元素,也是细胞鲜重中含量最多的元素
 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
【题目】阿斯巴甜(Aspartame,结构简式如图所示)具有清爽的甜味,甜度约为蔗糖的200倍。下列有关说法不正确的是
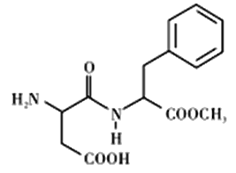
A. 阿斯巴甜在一定条件下既能与酸反应、又能与碱反应
B. 分子式为C14H18N2O3,阿斯巴甜属于蛋白质
C. 1mol阿斯巴甜分子可消耗3molNaOH
D. 一定条件下阿斯巴甜的水解产物中有两种氨基酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示物质结构的化学用语或模型正确的是
A. HF的电子式:![]() B. 用核素符号表示中子:
B. 用核素符号表示中子:![]()
C. HClO的结构式:H-Cl-O D. 用电子式表示CO2的形成过程: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钨是熔点最高的金属,是重要的战略物资。自然界中钨主要以钨酸盐( 钨元素的化合价为+6)形式存在于黑钨矿中。黑钨矿的主要成分是铁和锰的钨酸盐(FeWO4、MnWO4 ),还含有少量Si、As的化合物。由黑钨矿石冶冻金属钨的工艺流程如图所示:
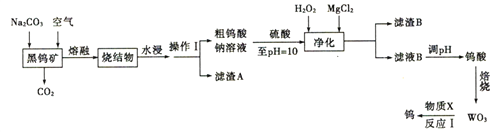
已知:①烧结物的成分为Fe2O3、MnO2、Na2SO3、Na2WO4、Na3AsO3、Na3AsO4;
②上述流程中,钨的化合价只在反应Ⅰ中发生改变;
③常温下钨酸难溶于水。
请回答下列问题:
(l)操作Ⅰ用到的玻璃仪器为______________。
(2)写出FeWO4在熔融条件下与Na2CO3、空气反应生成Fe2O3 的化学方程式________________。
(3)pH=10的溶液中的杂质阴离子为SiO32-、HAsO32-、HAsO42-等,则“净化”过程中,MgCl2 的作用是______________,加入H2O2 时发生反应的离子方程式为____________________。
(4)已知:室温时Ksp[Mg(OH)2]=5.6×10-12,在“净化”阶段,常温时保持溶液pH=10,为防止产生Mg(OH)2 沉淀,溶液中c(Mg2+)应不超过_________mol/L。
(5)反应Ⅰ中,物质X 可为H2、CO。
①已知:C(s)+H2O(g)![]() CO(g)+H2(g) △H1=a kJ/mol
CO(g)+H2(g) △H1=a kJ/mol
W3(s)+3H2(g)![]() W(s)+3H2O (g) △H2=bkJ/mol
W(s)+3H2O (g) △H2=bkJ/mol
WO3(s)+3CO(g)![]() W(s)+3CO2(g) △H3=c kJ/mol
W(s)+3CO2(g) △H3=c kJ/mol
根据上述信息,2WO3(s)+3C(s)![]() 2W(s)+3CO2(g)的△H=____________kJ/mol(用含a、b、c的式子表示)。
2W(s)+3CO2(g)的△H=____________kJ/mol(用含a、b、c的式子表示)。
②若黑钨矿中钨的质量分数为ω,提炼过程中利用率为b,欲用akg 黑钨矿制得化学纯金属钨,则产品中杂质允许含量的最大值为_____________kg(化工产品等级标准:优级纯≥99.8%,分析纯≥99.7%,化学纯≥99.5%)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H 是一种免疫调节剂,其合成流程如下:

问答下列问题:
(1)H所含官能团有氨基、羟基和______________。
(2)X的化学式为_______________,③的反应类型是_____________。
(3)设计反应①和⑤的目的是__________________。
(4)反应①为取代反应,其化学方程式为________________。
(5)R的同分异构体M同时满足下列条件:
①M 能与氯化铁溶液发生显色反应
②1molM 最多能和4molNaOH 发生反应
③在核磁共振氢谱上有四组峰且峰的面积之为3:3:2:2
M 的结构简式可能为________________。
(6)已知: ,结合上述相关信息,以
,结合上述相关信息,以 为原料设计合成路线合成
为原料设计合成路线合成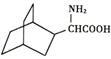 _________(其他试剂自选)。
_________(其他试剂自选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视。目前工业上有一种方法是用CO2来生产燃料甲醇。为探究该反应原理,进行如下实验:在容积为1L的密闭容器中,充入1molCO2和3molH2 , 在500℃下发生发应,CO2(g)+3H2(g) ![]() CH3OH(g)+ H2O(g)。实验测得CO2和CH3OH(g)的物质的量(n)随时间变化如下图1所示:
CH3OH(g)+ H2O(g)。实验测得CO2和CH3OH(g)的物质的量(n)随时间变化如下图1所示:
(1)从反应开始到平衡,氢气的平均反应速率v(H2)=。
(2)500℃该反应的平衡常数为(结果保留一位小数),图2是改变温度时化学反应速率随时间变化的示意图,若提高温度到800℃进行,达平衡时,K值(填“增大”“减小”或“不变”)。
(3)下列措施中不能使CO2的转化率增大的是________________。
A.在原容器中再充入1mol H2
B.在原容器中再充入1molCO2
C.缩小容器的容积
D.使用更有效的催化剂
E.将水蒸气从体系中分离出
(4)500℃条件下,测得某时刻,CO2(g)、H2(g)、CH3OH(g)和H2O(g)的浓度均为0.5mol/L,则此时v(正) v(逆)(填“>”“<”或“=”)。
Ⅱ、一定条件下,可逆反应A2(g)+B2(g) ![]() 2C(g)达到平衡时,各物质的平衡浓度为c(A2)=0.5mol/L;c(B2)=0.1mol/L;c(C)=1.6mol/L。若用a、b、c分别表示A2、B2、C的初始浓度(mol/L),则:
2C(g)达到平衡时,各物质的平衡浓度为c(A2)=0.5mol/L;c(B2)=0.1mol/L;c(C)=1.6mol/L。若用a、b、c分别表示A2、B2、C的初始浓度(mol/L),则:
①a、b应满足的关系是; ②a的取值范围是。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com