
【题目】Ⅰ、如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视。目前工业上有一种方法是用CO2来生产燃料甲醇。为探究该反应原理,进行如下实验:在容积为1L的密闭容器中,充入1molCO2和3molH2 , 在500℃下发生发应,CO2(g)+3H2(g) ![]() CH3OH(g)+ H2O(g)。实验测得CO2和CH3OH(g)的物质的量(n)随时间变化如下图1所示:
CH3OH(g)+ H2O(g)。实验测得CO2和CH3OH(g)的物质的量(n)随时间变化如下图1所示:
(1)从反应开始到平衡,氢气的平均反应速率v(H2)=。
(2)500℃该反应的平衡常数为(结果保留一位小数),图2是改变温度时化学反应速率随时间变化的示意图,若提高温度到800℃进行,达平衡时,K值(填“增大”“减小”或“不变”)。
(3)下列措施中不能使CO2的转化率增大的是________________。
A.在原容器中再充入1mol H2
B.在原容器中再充入1molCO2
C.缩小容器的容积
D.使用更有效的催化剂
E.将水蒸气从体系中分离出
(4)500℃条件下,测得某时刻,CO2(g)、H2(g)、CH3OH(g)和H2O(g)的浓度均为0.5mol/L,则此时v(正) v(逆)(填“>”“<”或“=”)。
Ⅱ、一定条件下,可逆反应A2(g)+B2(g) ![]() 2C(g)达到平衡时,各物质的平衡浓度为c(A2)=0.5mol/L;c(B2)=0.1mol/L;c(C)=1.6mol/L。若用a、b、c分别表示A2、B2、C的初始浓度(mol/L),则:
2C(g)达到平衡时,各物质的平衡浓度为c(A2)=0.5mol/L;c(B2)=0.1mol/L;c(C)=1.6mol/L。若用a、b、c分别表示A2、B2、C的初始浓度(mol/L),则:
①a、b应满足的关系是; ②a的取值范围是。
【答案】
(1)0.225mol/(L·min)
(2)5.3,减小
(3)B,D
(4)>,a=b+0.4,0.4≤b≤1.3
【解析】(1)根据图1,开始时CO2的浓度是1mol/L,平衡时CO2的浓度是0.25mol/L,CO2的浓度变化量是0.75 mol/L,则氢气的浓度变化量是2.25 mol/L,v= ![]() ,所以氢气的平均反应速率v(H2)=
,所以氢气的平均反应速率v(H2)= ![]() =0.225mol/(L·min);
=0.225mol/(L·min);
(2)根据“三段式”
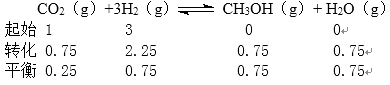 k=
k= ![]() =5.3;
=5.3;
根据图2可知,升高温度平衡逆向移动,K减小;
(3)A.在原容器中再充入1mol H2,平衡正向移动,CO2的转化率增大; B.在原容器中再充入1molCO2,平衡正向移动,但CO2的转化率减小;C.缩小容器的容积,平衡正向移动,CO2的转化率增大; D.使用更有效的催化剂,平衡不移动, CO2的转化率不变; E.将水蒸气从体系中分离出,平衡正向移动,CO2的转化率增大;故选BD;
(4)CO2(g)、H2(g)、CH3OH(g)和H2O(g)的浓度均为0.5mol/L, ![]() , Q<K,所以反应正向进行, v(正)> v(逆);
, Q<K,所以反应正向进行, v(正)> v(逆);
Ⅱ、①设转化过程中A2(g)转化浓度为x mol·L-1,B2(g)的转化浓度也为x mol·L-1。平衡时:a-x=0.5,b-x=0.1。所以,a=b+0.4。
②根据一边倒的方法,把C完全分解为A、B,则c(A2)=1.3mol/L;c(B2)=0.9mol/L;把B完全变为C,则c(A2)=0.4mol/L;c(B2)=0mol/L;c(C)=1.8mol/L;利用极值法,故a的取值范围为0.4<a<1.3;
【考点精析】解答此题的关键在于理解反应速率的定量表示方法的相关知识,掌握反应速率的单位:mol/(L·min)或mol/(L·s) v=△c-△t,以及对化学平衡状态本质及特征的理解,了解化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效).


科目:高中化学 来源: 题型:
【题目】下列有关人体细胞组成元素的叙述,正确的是
A.人体不同细胞的元素种类和含量都大致相同
B.构成细胞的微量元素的含量少,生理作用也小
C.组成人体的元素在非生物界中都能找到
D.C是最基本元素,也是细胞鲜重中含量最多的元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一处于平衡状态的反应:X(s)+3Y(g) ![]() 2Z (g),ΔH<0。为了使平衡向生成Z的方向移动,应选择的条件是( )
2Z (g),ΔH<0。为了使平衡向生成Z的方向移动,应选择的条件是( )
①高温 ②低温 ③高压 ④低压 ⑤加催化剂 ⑥分离出Z
A.①③⑤
B.②③⑤
C.②③⑥
D.②④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列装置不能达到有关实验目的是( )

A. 用甲图装置证明ρ(煤油)< ρ(钠)< ρ(水)
B. 用乙图装置可以吸收氨气防止倒吸
C. 用丙图装置制取金属锰
D. 用丁装置比较NaHCO3和Na2CO3的热稳定性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列选项不正确的是( )
A.已知A-+H2B(过量)= HA+HB- , 则结合H+的能力:HB-<A-<B2-
B.在0.1 mol/L氨水中滴加0.1 mol/L盐酸,恰好完全中和时溶液pH=a , 则由水电离产生的c(OH-)=10-a mol/L
C.将c molL-1的醋酸溶液与0.02 molL-1NaOH溶液等体积混合后溶液恰好呈中性,用含c的代数式表示CH3COOH的电离常数Ka= ![]()
D.欲除去CuCl2溶液中混有少量的FeCl3 , 可加入CuO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用工业炼铅产生的锌灰(主要成分为ZnO、PbO、FeO、MnO2、CuO)可回收制备ZnCl2,工艺流程如下:
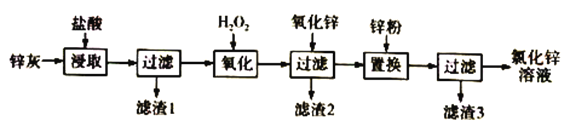
回答下列问题
(1)“浸取”实验中,反应体系的温度、反应时间对锰脱除效果的影响如下表,则适合的温度和反应时间分别是________________、____________________。

(2)“滤渣1”的主要成分是_____________。
(3)H2O2溶液的作用是____________________________________,已知“滤渣2”的主要成分是Fe(OH)3,则氧化锌的作用是_______________________________。“置换”实验中发生的反应的离子方程式有Zn+Pb2+=Ph+Zn2+、___________________________________。
(4)由锌灰制取金属锌可采用碱溶解,然后电解浸取液,已知:ZnO溶于NaOH溶液中生成[Zn(OH)4]2-,则阴极的电极反应为___________________________________。
(5)ZnCl2晶体溶解于饱和Na2CO3溶液中,得到6.46g的碱式碳酸锌[Znx(CO3)y(OH)z,为了测定其组成,充分加热分解,产生的气体依次通入浓硫酸和碱石灰,质量分别增重了0.72g和0.88g,则该碱式碳酸锌的化学式为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机化合物M的结构简式如图所示,有关该化合物的叙述不正确的是
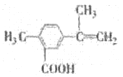
A. 该有机物的分子式为C11H12O2
B. 该有机物的所有碳原子可能处于同一平面上
C. 仅考虑取代基在苯环上的位置变化,M的同分异构体(不包括自身)有9种
D. 该有机物一定条件下只能发生加成反应和酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是地壳中含量最多的金属元素,其单质和化合物广泛应用于日常生活中。
(1)铝粉和铁的氧化物(FeO-Fe2O3)可配成铝热剂用于焊接钢轨,反应的化学方程式是____。
(2)以铝土矿(主要成分为Al2O3.含SiO2和Fe2O3等杂质)为原料生产铝和铵明矾晶体[NH4Al(SO4)2·12H2O]的一种工艺流程如下(已知:SiO2在“碱溶”时转化为铝硅酸钠(NaAlSiO4·nH2O)沉淀)。

①实验前,要将铝土矿粉粹的目的是_______。
②用氧化物的形式表示铝硅酸钠的化学式________。
③步骤②涉及到的离子方程式是: _______。
④写出利用Al2O3制备金属Al的化学方程式: _______。
⑤若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的物质的量之比为1:1,则投料时铝土矿中的Al2O3和H2SO4的物质的量之比为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列反应的热化学方程式:
(1)N2和H2反应生成34g NH3 , 放出92kJ热量。
(2)1molCH4(g)在O2中完全燃烧生成CO2和H2O(g),放出890.3kJ热量。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com