
【题目】下列说法中正确的是( )
A. 溶液成中性就是pH=7 B. 溶液成中性指的是C(![]() )=C(
)=C(![]() )
)
C. 酸中一定无OH- D. 盐溶液一定成中性
科目:高中化学 来源: 题型:
【题目】下列是部分短周期中第二、第三周期元素的原子半径及主要化合价.
元素代号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
原子半径(nm) | 0.186 | 0.160 | 0.152 | 0.143 | 0.110 | 0.099 | 0.075 | 0.074 |
主要化合价 | +1 | +2 | +1 | +3 | +5、﹣3 | +7、﹣1 | +5、﹣3 | ﹣2 |
回答下列问题:
(1)⑧在元素周期表中的位置是(周期、族);
(2)8个元素的最高价氧化物的水化物中,酸性最强的是(填化学式);
(3)元素⑤、⑦、⑧分别形成的简单气态氢化物中,⑦的电子式为 , 稳定性最强的氢化物的结构式为;
(4)写出①、④的最高价氧化物对应的水化物之间发生反应的离子方程式;
(5)用电子式表示元素①与⑥形成化合物的过程 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用纯净的锌粒与稀盐酸反应制取氢气气体,请回答:
(1)实验过程如下图所示,分析判断段化学反应速率最快,段收集的氢气最多. 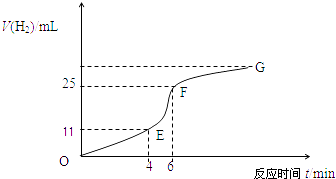
(2)将锌粒投入盛有稀盐酸的烧杯中,刚开始时产生H2的速率逐渐加快,其影响因素是 , 一定时间后反应速率逐渐减慢,其原因是 .
(3)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的是
A.蒸馏水
B.氯化钠固体
C.氯化钠溶液
D.浓盐酸
E.降低温度
(4)EF段产生H2的反应速率为mLmin﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关硫酸工业综合经济效益的说法中正确的是( )
A.甲地有丰富的硫资源,水源能源充足,交通便利,是风景秀丽的旅游胜地,虽当地使用硫酸的工业不多,但为提高当地经济效益宜建硫酸厂
B.为减少SO2对空气的污染,可以建筑高烟囱,使含SO2的尾气在高空扩散稀释,到达地面时达到安全浓度
C.硫酸生产过程排放的污染物主要是含SO2的尾气、固体烧渣、废酸和废水等
D.选择硫酸厂厂址时,当经济利益与环保问题有冲突时,为提高人们的物质生活水平,应先考虑经济利益的问题
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列反应的热化学方程式:
(1)N2和H2反应生成34g NH3,放出92kJ热量____________________。
(2)1molCH4(g)在O2中完全燃烧生成CO2和H2O(g),放出890.3kJ热量________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂。其中没食子儿茶素(EGC)的结构如图所示。关于EGC的下列说法中正确的是
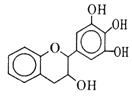
A. 遇FeCl3溶液不发生显色反应
B. 1 mol EGC与4 mol NaOH恰好完全反应
C. 易发生氧化反应和取代反应,难发生加成反应
D. 分子中所有的原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知:CH3CH2OH+NaBr+H2SO4(浓) ![]() CH3CH2Br+NaHSO4 +H2O。实验室制备溴乙烷(沸点为38.4℃) 的装置如图: 圆底烧瓶中加入10mL 95%乙醇、28mL浓硫酸,然后加入研细的10.3g溴化钠和几粒碎瓷片,小火加热,使NaBr充分反应。
CH3CH2Br+NaHSO4 +H2O。实验室制备溴乙烷(沸点为38.4℃) 的装置如图: 圆底烧瓶中加入10mL 95%乙醇、28mL浓硫酸,然后加入研细的10.3g溴化钠和几粒碎瓷片,小火加热,使NaBr充分反应。
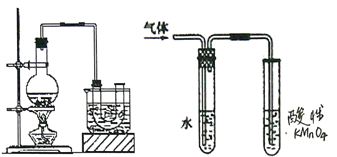
(1)反应时若温度过高会降低溴乙烷的产率,原因是______;也可看到有红棕色气体产生,该气体的化学式为_________。为避免温度过高,宜采用_________加热。
(2)反应结束后,U形管中粗制的溴乙烷呈棕黄色。为了除去其中的杂质,最好选用下列试剂中的_______(填序号)。
A.Na2SO3溶液B.H2OC.NaOH溶液D.CCl4
(3)溴乙烷在NaOH水溶液和NaOH乙醇溶液发生不同类型的反应,生成不同的产物,用上面右图所示装置进行实验:该实验的目的是________。盛水的试管(装置)的作用是____。
(4)为检验溴乙烷中的溴元素,正确的操作顺序是:取少量溴乙烷,然后______(填序号)。
①加热 ②加入AgNO3溶液 ③加入稀HNO3酸化 ④加入NaOH溶液 ⑤冷却
(5)经提纯最终得到纯净的溴乙烷为7.63g,则溴乙烷的产率为______ (保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在无色透明的酸性溶液中,能大量共存的离子组是
A. Mg2+、NH4+、NO3-、Cl-
B. Al3+、Ag+、NO3-、Fe2+
C. K+、CO32-、Cl-、Ba2+
D. Na+、OH-、SO42-、Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.合成硫酸的工业尾气可以直接排入大气
B.进入接触室的气体,必须先经净化、干燥
C.从沸腾炉中排出的炉渣可以作为肥料
D.在高温、高压下由SO2和O2合成SO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com