
如图为10 mL一定物质的量浓度的盐酸X,用一定浓度的NaOH溶液Y滴定的图示。依据图示,推出X和Y的物质的量浓度是( )
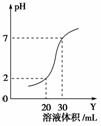
| A | B | C | D | |
| X浓度/mol·L-1 | 0.12 | 0.04 | 0.03 | 0.09 |
| Y浓度/mol·L-1 | 0.04 | 0.12 | 0.09 | 0.03 |
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案科目:高中化学 来源: 题型:
下列化学反应能用离子反应Ca2++ 2HCO3-+ 2OH-® CaCO3↓+ CO32- + 2H2O表示的是( )
A. Ca(OH) 2与少量的NaHCO3 B. Ca(OH) 2与少量的Ca(HCO3) 2
C. Ca(HCO3) 2与足量的NaOH D. Ca(OH) 2与足量的Ca(HCO3) 2
查看答案和解析>>
科目:高中化学 来源: 题型:
已知卤代烃可以和钠发生反应。例如溴乙烷与钠发生反应为2CH3CH2Br+2Na―→CH3CH2CH2CH3+2NaBr,下列所给化合物中与钠反应不可能生成环丁烷的是
A.CH3CH2CH2CH2Br B.CH2BrCH2Br
C.CH2Br2 D.CH2BrCH2CH2CH2Br
查看答案和解析>>
科目:高中化学 来源: 题型:
要组装一套实验室利用液体和液体反应制备气体的装置,现设计了如下的五步操作,正确的程序是( )
①将蒸馏烧瓶固定在铁架台上
②将酒精灯放在铁架台上,根据酒精灯确定铁圈高度,固定铁圈,放好石棉网
③用漏斗向蒸馏烧瓶中加入一种液体反应物,再向分液漏斗中加入另一种液体反应物,并将导气管放入气体收集装置中
④检查装置的气密性(利用固定装置微热的方法检查气密性)
⑤在蒸馏烧瓶中装好分液漏斗,连接好导气管
A.②①⑤④③ B.④①②⑤③
C.①②⑤④③ D.①⑤④②③
查看答案和解析>>
科目:高中化学 来源: 题型:
某课外活动小组将下图所示装置按一定顺序连接,在实验室里制取一定量的FeCl3(所通气体过量并充分反应)。

请回答下列问题:
(1)A中发生反应的化学方程式为__________________________________。
(2)各装置的正确连接顺序为(填写装置序号)A→________→________→________→D。
(3)装置C的作用是_____________________________________________________,
写出装置D中反应的离子方程式________________________________________。
(4)反应开始后,B中硬质玻璃管内的现象为____________________________________;可以检验生成物中含有Fe3+的试剂是______________(填写试剂名称)。
(5) 该小组欲用右图所示装置收集尾气,并测量多余气体的体积。
该小组欲用右图所示装置收集尾气,并测量多余气体的体积。
①若右图所示量气装置由干燥管、乳胶管和50 mL滴定管改造后组装而成,此处所用滴定管是________(填“酸式”或“碱式”)滴定管。
②为提高测量的准确性,右图装置中的液体可用__________,收集完气体后,读数前应进行的操作是________________________。
③如果开始读数时操作正确,最后读数时俯视右边滴定管液面,会导致所测气体的体积________(填“偏大”“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列是某学生自己总结的一些规律,其中正确的是:( )
(A)氧化物不可能是还原产物,只可能是氧化产物
(B)有些化学反应不属于化合、分解、置换、复分解中的任何一种反应
(C)一种元素可能有多种氧化物,但同种化合价只对应一种氧化物
(D)将Mg(HCO3)2溶液加热,最终得到Mg(OH)2沉淀,由此可知溶解度Mg(OH)2> Mg(HCO3)2
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,其中B是地壳中含量最多的元素.已知A、C及B、E分别是同主族元素,且B、E两元素原子核内质子数之和是A、C两元素原子核内质子数之和的2倍.处于同周期的C、D、E元素中,D是该周期金属元素中金属性最弱的元素.
(1)试比较C、D两元素最高价氧化物对应水化物碱性的强弱(填化学式)
> ;
(2)A、B、C形成的化合物的晶体类型为 ;电子式为 ;
(3) 写出D单质与C元素最高价氧化物对应水化物反应的离子方程式 ;
(4)写出两种均含A、B、C、E四种元素的化合物在溶液中相互反应、且生成气体的离子方程式 ;
(5)A单质和B单质能构成电池,该电池用多孔惰性电极浸入浓KOH溶液,两极分别通入A单质和B单质,写出该电池负极电极反应方程式 ;
(6)通常条件下, C的最高价氧化物对应水化物2mol与E最高价氧化物对应水化物1mol的稀溶液间反应放出的热量为114.6KJ,试写出表示该热量变化的离子方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
某课外学习小组设计实验测定Na2CO3样品(含NaC l杂质)的纯度。请根据实验方案回答下列问题:
l杂质)的纯度。请根据实验方案回答下列问题:
方案一:沉淀法。
(1)将w g样品在烧杯中溶解,加入过量的BaCl2溶液,并用玻璃棒搅拌。
(2)________(填操作名称) 、洗涤、干燥,称量沉淀的质量为m g。
(3) 根据以上数据得出Na2CO3的质量分数为________。
根据以上数据得出Na2CO3的质量分数为________。
方案二:气体法。
实验小组利用如图装置完成实验。
(4)根据上述实验装置可知,乙中所盛试剂为________,其作用是________。丁的作用是________。
(5)学习小组通过测量丙装置实验前后的质量,确定Na2CO3的含量,但计算结果总是比实验值偏低,试分析可能的原因(装置气密性良好):
A:________;B:________。
(6)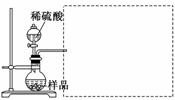 在此方案基础上,有同学提出测量气体体积的方法确定Na2CO3的含量。请依据此设想,补充完整实验装置。(画出实验装置图并注明所用试剂)。
在此方案基础上,有同学提出测量气体体积的方法确定Na2CO3的含量。请依据此设想,补充完整实验装置。(画出实验装置图并注明所用试剂)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com