
【题目】某Na2CO3、NaAlO2的混合溶液中逐滴加入1molL-1的盐酸,测得溶液中的CO32-、HCO3-、AlO2-、Al3+离子的物质的量与加入盐酸溶液的体积变化关系如图所示,则下列说法正确的是( )

A.原混合溶液中的CO2-3与AlO-2的物质的量之比为1:2
B.V1:V2=1:5
C.M点时生成的CO2为0.05mol
D.a曲线表示的离子方程式为:AlO-2+H++H2O=Al(OH)3↓
【答案】D
【解析】
试题分析:Na2CO3、NaAlO2的混合溶液中逐滴加入1molL-1的盐酸。首先,发生反应AlO2-+H++H2O═Al(OH)3↓,a线表示AlO2-,由图可知AlO2-反应完毕,加入盐酸50mL,根据方程式可知n(AlO2-)=n(H+)=0.05L×1mol/L=0.05mol。第二阶段,AlO2-反应完毕,发生反应CO32-+H+═HCO3-,b线表示CO32-,c线表示HCO3-,由图可知CO32-反应完毕,该阶段加入盐酸100mL-50mL=50mL,根据方程式可知n(CO32-)=n(H+)=0.05L×1mol/L=0.05mol。第三阶段,CO32-反应完毕,发生反应HCO3-+H+═CO2↑+H2O,d线表示HCO3-,由图可知HCO3-反应完毕,该阶段加入盐酸150mL-100mL=50mL,根据方程式可知n(HCO3-)=n(H+)。第四阶段,发生反应Al(OH)3+3H+═Al3++3H2O,e线表示Al3+,由图可知Al(OH)3反应完毕,根据方程式可知n(H+)=3n[Al(OH)3]=3×0.05mol=0.15mol,该阶段加入盐酸体积为![]() =0.15L=150mL。A、由上述分析可知,原混合溶液中的CO32-与AlO-2的物质的量之比为0.05mol:0.05mol=1:1,故A错误;B、原溶液中n(CO32-)=0.05mol,V1时溶液中碳酸氢根离子等于碳酸根离子为0.025ml,由反应CO32-+H+═HCO3-可知,需要盐酸为0.025mol,盐酸的体积为
=0.15L=150mL。A、由上述分析可知,原混合溶液中的CO32-与AlO-2的物质的量之比为0.05mol:0.05mol=1:1,故A错误;B、原溶液中n(CO32-)=0.05mol,V1时溶液中碳酸氢根离子等于碳酸根离子为0.025ml,由反应CO32-+H+═HCO3-可知,需要盐酸为0.025mol,盐酸的体积为![]() =0.025L=25mL,故V1=50mL+25mL=75mL,由上述分析可知,V2=150mL+150mL=300mL,故V1:V2=75mL:300mL=l:4,故B错误;C、由上述分析可知M点时溶液中CO32-完全转化为HCO3-,没有CO2生成,故C错误;D、由上述分析可知,a曲线表示的离子方程式为:AlO-2+H++H2O=Al(OH)3↓,故D正确;故选D。
=0.025L=25mL,故V1=50mL+25mL=75mL,由上述分析可知,V2=150mL+150mL=300mL,故V1:V2=75mL:300mL=l:4,故B错误;C、由上述分析可知M点时溶液中CO32-完全转化为HCO3-,没有CO2生成,故C错误;D、由上述分析可知,a曲线表示的离子方程式为:AlO-2+H++H2O=Al(OH)3↓,故D正确;故选D。


科目:高中化学 来源: 题型:
【题目】反应aA(g)+bB(g)![]() cC(g)(△H<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示:
cC(g)(△H<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示:
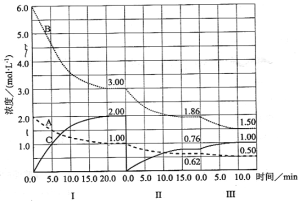
回答问题:
(1)反应的化学方程式中a∶b∶c为 ;
(2)由第一次平衡到第二次平衡,平衡移动的方向是_____,采取的措施是____________。
(3)比较第Ⅱ阶段反应温度(T2)和第Ⅲ阶段反应温度(T3)的高低;T2 T3(填“<”“>”“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把下列四种X溶液分别加入四个盛有10 mL 2 mol/L盐酸的烧杯中,均加水稀释到50 mL,此时,X和盐酸缓慢地进行反应,其中反应最快的是( )
A.10 ℃ 20 mL 3 mol/L的X溶液
B.10 ℃ 10 mL 2 mol/L的X溶液
C.20 ℃ 10 mL 4 mol/L的X溶液
D.20 ℃ 30 mL 2 mol/L的X溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40~50℃时反应可生成它。CuH不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;Cu+在酸性条件下发生反应是2Cu+===Cu2++Cu 。
根据以上信息,结合自己所掌握的化学知识,回答下列问题:
(1)在CuSO4溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中所起的作用是 (填“氧化剂”或“还原剂”)。
(2)写出CuH在氯气中燃烧的化学反应方程式 。
(3)CuH溶液在稀盐酸中生成的气体是 (填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、W为五种短周期元素。X原子的质子数与电子层数相同,W原子核外电子数是M原子最外层电子数的2倍,Y、Z、M、W在周期表中的相对位置如图所示。下列说法不正确的是
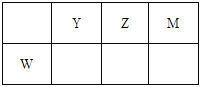
A. 原子半径:W>Y>Z>M>X
B. 热稳定性:XM>X2Z,沸点:X2Z>YX3
C. X、Y、Z三种元素形成的化合物中不可能含离子键
D. ZM2、YM3、WM4分子中每个原子最外层均满足8电子结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】咖啡酸苯乙酯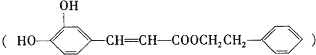 是一种天然抗癌药物,在一定条件下能发生如下转化
是一种天然抗癌药物,在一定条件下能发生如下转化
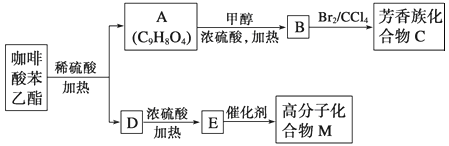
请回答下列问题:
(1)D分子中的官能团是__________;
(2)高分子化合物M的结构简式是__________;
(3)写出A→B反应的化学方程式:__________;
(4)B→C的反应类型为__________;
(5)1molA最多可消耗__________molNaOH;
(6)一定条件下1molA最多与__________mol氢气加成
(7)A的同分异构体有很多种,其中,同时符合下列条件的同分异构体的结构简式:__________
①苯环上只有两个取代基 ②能发生银镜反应 ③能与碳酸氢钠溶液反应 ④能与氯化铁溶液发生显色反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有机物A能发生以下转化,并且A可以作为水果的催熟剂,在一定条件下A可以发生自身加成反应,形成高分子化合物E。
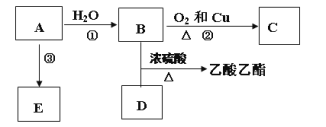
(1)写出E的结构简式______________,E______(填“能”或“不能”)使酸性KMnO4溶液褪色。
(2)请写出C的名称是______________,D分子中的官能团名称是___________。
(3)请写出反应②以及B与D发生反应的化学方程式,并注明反应类型:
② ________________________________,反应类型_____________;
B+D ______________________________,反应类型_____________。
(4)若完全燃烧0.1mol某烃,燃烧产物依次通过浓硫酸、浓碱液,实验结束后,称得浓硫酸增重9g,浓碱液增重17.6g。该烃的化学式 ,并写出其所有可能的结构简式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,不满足组内任意两种物质在一定条件下均能发生反应的是( )
物质 组别 | 甲 | 乙 | 丙 |
A | FeCl2 | Cl2 | NaOH |
B | SiO2 | NaOH | HF |
C | AlCl3 | KOH | H2SO4 |
D | SO2 | NaOH | NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
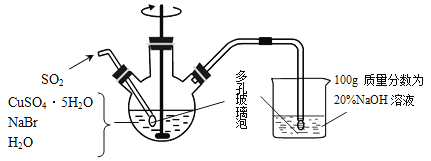
【题目】溴化亚铜是一种白色粉末,不溶于冷水,在热水中或见光都会分解,在空气中会慢慢氧化成绿色粉末。制备CuBr的实验步骤如下:
步骤1.在如图所示的三颈烧瓶中加入45gCuSO4·5H2O、19gNaBr、150mL煮沸过的蒸馏水,60℃时不断搅拌,以适当流速通入SO2 2小时。
步骤2.溶液冷却后倾去上层清液,在避光的条件下过滤。
步骤3.依次用溶有少量SO2的水、溶有少量SO2的乙醇、纯乙醚洗涤。
步骤4.在双层干燥器(分别装有浓硫酸和氢氧化钠)中干燥3~4h,再经氢气流干燥,最后进行真空干燥。
(1)实验所用蒸馏水需经煮沸,煮沸目的是除去其中水中的 (写化学式)。
(2)步骤1中:①三颈烧瓶中反应生成CuBr的离子方程式为 ;
②控制反应在60℃进行,实验中可采取的措施是 ;
(3)步骤2过滤需要避光的原因是 。
(4)步骤3中洗涤剂需“溶有SO2”的原因是 ;最后溶剂改用乙醚的目的是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com