
【题目】将质量为6.3g的Na2SO3暴露在空气中一段时间后溶于水配成100mL溶液.取出50mL,加入过量的稀硫酸溶液得到气体在标准状况下的体积为0.448L;另取该溶液50mL加入足量的氯化钡溶液,求生成的白色沉淀的成分及其质量.
【答案】解:6.3g亚硫酸钠的物质的量为:n(Na2SO3)= ![]() =0.05 mol,
=0.05 mol,
取出一半与稀硫酸反应,生成二氧化硫的物质的量为:n(SO2)= ![]() =0.02 mol,根据S原子守恒可知溶液中含有亚硫酸钠的物质的量为:n(Na2SO3)=n(SO2)=0.02 mol,
=0.02 mol,根据S原子守恒可知溶液中含有亚硫酸钠的物质的量为:n(Na2SO3)=n(SO2)=0.02 mol,
溶液具有均一性,则另一份加入氯化钡的溶液中含有亚硫酸钠的物质的量也是0.02mol,结合S原子守恒看含有硫酸钠的物质的量为:n(Na2SO4)=0.05mol× ![]() ﹣0.02mol=0.005 mol,
﹣0.02mol=0.005 mol,
加入氯化钡溶液后生成的白色沉淀为BaSO4、BaSO3 , 其中生成亚硫酸钡的物质的量为:n(BaSO3)=0.02 mol,质量为:m(BaSO3)=217g/mol×0.02mol=4.34g,
生成硫酸钡的物质的量为:n (BaSO4)=0.005 mol,质量为:m(BaSO4)=233g/mol×0.005mol=1.165g,
答:生成的白色沉淀为亚硫酸钡和硫酸钡的混合物,含有4.34g亚硫酸钡,含有1.165g硫酸钡.
【解析】亚硫酸钠易被氧化成硫酸钠,取出50mL溶液加入稀硫酸后生成的气体为二氧化硫,根据n= ![]() 计算出二氧化硫的物质的量,从而可知每份溶液中没有被氧化的亚硫酸钠的物质的量及被氧化的物质的量;另一份溶液中加入氯化钡溶液后生成硫酸钡和亚硫酸钡沉淀,根据亚硫酸钠、硫酸钠的物质的量可知硫酸钡、亚硫酸钡的物质的量,再根据m=nM计算出沉淀的质量.
计算出二氧化硫的物质的量,从而可知每份溶液中没有被氧化的亚硫酸钠的物质的量及被氧化的物质的量;另一份溶液中加入氯化钡溶液后生成硫酸钡和亚硫酸钡沉淀,根据亚硫酸钠、硫酸钠的物质的量可知硫酸钡、亚硫酸钡的物质的量,再根据m=nM计算出沉淀的质量.


 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:高中化学 来源: 题型:
【题目】呼吸面具中Na2O2可吸收CO2放出O2,若用超氧化钾(KO2)代替Na2O2也可起到同样的作用。
(1)写出KO2与CO2的反应方程式________________________________.
(2)lkgNa2O2和lkgKO2,分别和CO2反应,生成的O2体积比(同温同压下)为__________。
(3)等物质的量的CO2分别与足量的Na2O2,KO2反应生成的O2体积比(同温同压下)为__________。
(4)你认为选用_______________作补氧剂更为合适,理由是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化属于加成反应的是( )
A. 乙烯使酸性高锰酸钾溶液的紫色褪去
B. 乙烯与水在一定条件下反应生成乙醇
C. 苯与浓硫酸和浓硝酸的混合液反应生成油状物
D. 乙醇在催化剂存在的条件下与氧气反应生成乙醛
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1200℃时,天然气脱硫工艺中会发生下列反应:
H2S(g)+![]() O2(g)===SO2(g)+H2O(g) ΔH1
O2(g)===SO2(g)+H2O(g) ΔH1
2H2S(g)+SO2(g)===![]() S2(g)+2H2O(g) ΔH2
S2(g)+2H2O(g) ΔH2
H2S(g)+![]() O2(g)===S(g)+H2O(g) ΔH3
O2(g)===S(g)+H2O(g) ΔH3
2S(g)===S2(g) ΔH4
则ΔH4的正确表达式为
A. ΔH4=![]() (ΔH1+ΔH2-3ΔH3) B. ΔH4=
(ΔH1+ΔH2-3ΔH3) B. ΔH4=![]() (3ΔH3-ΔH1-ΔH2)
(3ΔH3-ΔH1-ΔH2)
C. ΔH4=![]() (ΔH1+ΔH2-3ΔH3) D. ΔH4=
(ΔH1+ΔH2-3ΔH3) D. ΔH4=![]() (ΔH1-ΔH2-3ΔH3)
(ΔH1-ΔH2-3ΔH3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,浓度均为1.0 mol·L-1的NH3·H2O和NH4Cl混合溶液10 mL,测得其pH为9.3。下列有关叙述正确的是
A.加入适量的NaCl,可使c(NH4+) = c(Cl-)
B.滴加几滴浓氨水,c(NH4+)减小
C.滴加几滴浓盐酸,![]() 的值减小
的值减小
D.1.0 mol·L-1的NH4Cl溶液中c(NH4+)比该混合溶液大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有五种操作方法,在油脂皂化后,使肥皂和甘油从混合物中充分分离,可以采用的方法是( )
①分液 ②蒸馏 ③过滤 ④盐析 ⑤渗析
A.①②
B.③④
C.②③④
D.②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向10mlbmol·L-1的CH3COOH溶液中滴加等体积的0.01mol·L-1的NaOH溶液,充分反应后溶液中c(CH3COO-)=c(Na+),下列说法正确的是
A. b<0.01
B. 混合后溶液呈中性
C. CH3COOH的电离常数Ka=![]()
D. 向CH3COOH溶液中滴加NaOH溶液的过程中,水的电离程度逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学兴趣小组为探究铁与浓硫酸反应,设计了如图所示装置进行实验。
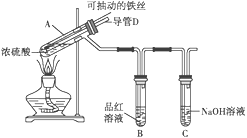
(1)已知C中盛有足量的氢氧化钠溶液,实验过程中,观察到B中的品红溶液褪色,C中发生反应的离子方程式为______________________________。一段时间后,观察到C中有少量气泡冒出,此气泡的成分是________________。
(2)用“可抽动的铁丝”代替“直接投入铁片”的优点是_____________________________;
(3)导管D作用是___________________________________________________。
(4)反应结束后,不需要打开胶塞,就可使装置中残留气体完全被吸收,应当采取的操作是_____。
(5)设计实验检验反应后试管A中所得溶液里是否含有亚铁离子,可选用的试剂为(_____)
A. NaOH溶液 B. 铁氰化钾溶液
C. KSCN溶液和双氧水 D.酸性高锰酸钾溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com