
【题目】下列实验装置,其中按要求设计正确的是
A. 电解饱和食盐水并验证产物 | B. 铜锌原电池电流方向如图所示 |
C. 在钥匙上电镀银 | D. 电解精炼铜 |
A. A B. B C. C D. D
【答案】B
【解析】
A.电解饱和的氯化钠溶液时,活泼电极作阳极,则阳极上放电的是阳极材料而不是溶液中阴离子;
B.含有盐桥的原电池中,电极材料和相应的电解质溶液有相同的金属元素;
C.电镀时,电解质溶液中的金属元素要和镀层相同;
D.电解精炼铜时,粗铜作阳极,纯铜作阴极,且电解质溶液中必须含有铜离子。
A.该电解池中,阳极上铁失电子而不是氯离子失电子,所以阳极上得不到氯气,则淀粉碘化钾溶液不会变蓝,所以实验设计不合适,故A错误;
B.含有盐桥的铜锌原电池中,铜电极对应的电解质是铜盐,锌电极对应的电解质是锌盐,符合原电池设计要求,所以B选项是正确的;
C.该电镀池中电解质应该是硝酸银而不是硝酸钠,故C错误;
D.电解精炼铜时,粗铜作阳极,纯铜作阴极,故D错误。
所以B选项是正确的。


 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:
【题目】钛矿工业中的硫酸酸性废水富含Ti、Fe等元素,其综合利用如下:
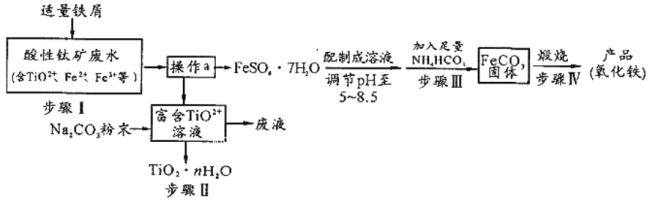
已知:TiO2+易水解,只能存在于强酸性溶液中。
(1)TiO2+钛的化合价为________________________。
(2)步骤Ⅰ中检验钛矿废水中加入铁屑是否足量的试剂是________________________。
(3)操作a是蒸发浓缩、冷却结晶、______________________________________________。
(4)步骤Ⅲ中发生反应的化学方程式为________________________;反应温度一般需控制在35℃以下,其目的是____________________________________。
(5)已知Ksp=[Fe(OH)2] = 8×10-16。步骤Ⅲ中,FeCO3达到溶解平衡时,若室温下测得溶液的pH为8.5, c(Fe2+) = 1×10-6mol/L。试判断所得的FeCO3中________(填“有”或“没有”)Fe(OH)2;步骤Ⅳ中,为了得到较为纯净的Fe2O3,除了适当的温度外,还需要采取的措施是_________________。
(6)向“富含TiO2+溶液”中加入Na2CO3粉末易得到固体TiO2 nH2O。请结合原理和化学用语解释其原因_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。
(1)E元素在周期表中的位置为___________________。
(2)由AW两种元素组成的18电子微粒的电子式为______________。
(3)经测定A2W2为二元弱酸,其酸性比碳酸的还要弱。常用硫酸处理BaO2来制备A2W2,写出该反应的化学方程式_____________________________。
(4)废印刷电路反上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2W2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出反应的离子方程式____________________。
(5)D的某化合物呈淡黄色,可与氯化亚铁溶液反应。若淡黄色固体与氯化亚铁反应的物质的量之比为1:2,且无气体生成,则该反应的离子方程式为_____________________________。
(6)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA,DA能与水反应放出氢气,若将1molDA和0.5molE单质混合加入足量的水,充分反应后生成气体的体积是___________(标准状况下)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示水解的离子方程式正确的是
A. CH3COO-+H2O![]() CH3COOH+OH-
CH3COOH+OH-
B. NH4++H2O![]() NH4OH+H+
NH4OH+H+
C. S2-+2H2O![]() H2S+2OH-
H2S+2OH-
D. HCO3-+H2O![]() H3O++CO32-
H3O++CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有短周期元素R、X、Y、Z、T。R与T原子最外层电子数均是电子层数的2倍;Y元素能与大多数金属和非金属元素形成化合物;Z+与Y2-电子层结构相同。五种元素的原子半径与原子序数的关系如图所示,下列推断正确的是

A. Y、Z组成的化合物只含离子键
B. 氢化物的沸点:Y < X
C. T、R的最高价氧化物对应的水化物的酸性T比R的强
D. Y分别与T、X组成的二元化合物的水溶液一定是强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究氮及其化合物的性质在人类进步过程中具有极为重要的意义。
(1)肼(N2H4)与N2O4分别是火箭发射中最常用的燃料与氧化剂。已知2N2H4(l)+N2O4(l)===3N2(g)+4H2O(l) ΔH=-1 225 kJ·mol-1。几种化学键的键能数据如下:
化学键 | N—H | N—N | N≡N | O—H |
键能/(kJ·mol-1) | 390 | 190 | 946 | 460 |
则1 mol N2O4(l)完全分解成相应的原子时需要吸收的能量是________。
(2)N2O4与NO2转化的热化学方程式为N2O4(g)![]() 2NO2(g) ΔH=+24.4 kJ·mol-1。
2NO2(g) ΔH=+24.4 kJ·mol-1。
①将一定量的N2O4投入固定容积的真空容器中,下述现象能说明反应达到平衡的是________(填字母)。
a.v正(N2O4)=2v逆(NO2) b.体系颜色不变
c.气体平均相对分子质量不变 d.气体密度不变
②在一密闭容器中发生该反应,达到平衡后,保持体积不变升高温度,再次达到平衡时,则混合气体的颜色________(填“变深”“变浅”或“不变”),判断理由______________________________________。
③平衡常数K可用反应体系中气体物质平衡分压表示,即K表达式中平衡浓度可用平衡分压代替,分压=总压×物质的量分数[例如:p(NO2)=p总×x(NO2)]。写出上述反应平衡常数K的表达式________(用p总、各气体物质的量分数x表示);影响K的因素为________。
(3)氨是一种重要的化工原料,在工农业生产中有广泛的应用。在773 K时,分别将2.00 mol N2和6.00 mol H2充入一个固定容积为1 L的密闭容器中,限着反应的进行,气体混合物中n(H2)、n(NH3)与反应时间(t)的关系如表所示:
t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
n(H2/span>)/mol | 6.00 | 4.50 | 3.60 | 3.30 | 3.03 | 3.00 | 3.00 |
n(NH3)/mol | 0 | 1.00 | 1.60 | 1.80 | 1.98 | 2.00 | 2.00 |
①该温度下,若向同容积的另一容器中投入N2、H2、NH3,其浓度均为3 mol·L-1,则此时v正________________(填“大于”“小于”或“等于”)。
②由表中的实验数据可得到“c—t”的关系,如图1所示,表示c(N2)—t的曲线是________。在此温度下,若起始充入4 mol N2和12 mol H2,则反应刚达到平衡时,表示c(H2)—t的曲线上相应的点为________。
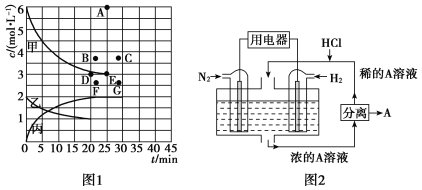
(4)有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图2所示。电池正极的电极反应式是____________________,A是_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一容积可变的恒压密闭容器里,反应3A(g)![]() B(g)+3C(g) 达到平衡时,A、B和C的物质的量分别为6 mol、2 mol、6 mol。在保持温度和压强不变的情况下,下列说法正确的是
B(g)+3C(g) 达到平衡时,A、B和C的物质的量分别为6 mol、2 mol、6 mol。在保持温度和压强不变的情况下,下列说法正确的是
A.将A、B、C各减少1 mol,C的百分含量减少
B.充入A、B、C各2 mol,平衡将向正反应方向移动
C.充入1mol A,C的体积分数增加
D.充入1 mol氦(He与容器中气体不反应),平衡将向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,已知AgCl的Ksp=1.8×10-10,Ag2CO3在水中的沉淀溶解平衡曲线如图所示,下列说法错误的是
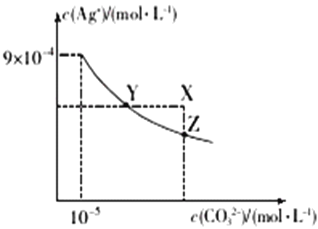
A. Ag2CO3的Ksp为8.1×10-12
B. Ag2CO3(s)+2Cl-(aq)2AgCl(s)+CO32-(aq)的平衡常数K=2.5×108
C. 在Ag2CO3的饱和溶液中加入K2CO3(s)可使c(CO32-)增大(由Y点到Z点)
D. 在0.001molL-1AgNO3溶液中滴入同浓度的KCl和K2CO3的混合溶液,CO32-先沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com