
【题目】某温度下,在一容积可变的恒压密闭容器里,反应3A(g)![]() B(g)+3C(g) 达到平衡时,A、B和C的物质的量分别为6 mol、2 mol、6 mol。在保持温度和压强不变的情况下,下列说法正确的是
B(g)+3C(g) 达到平衡时,A、B和C的物质的量分别为6 mol、2 mol、6 mol。在保持温度和压强不变的情况下,下列说法正确的是
A.将A、B、C各减少1 mol,C的百分含量减少
B.充入A、B、C各2 mol,平衡将向正反应方向移动
C.充入1mol A,C的体积分数增加
D.充入1 mol氦(He与容器中气体不反应),平衡将向正反应方向移动
科目:高中化学 来源: 题型:
【题目】已知:单质A为目前人类使用最广泛的金属,氧化物B为具有磁性的黑色晶体,根据下列转化关系填空。

(1)试判断:A的化学式为_____________,B的名称为_______________。
(2)实验室检验C溶液中的阳离子时,可加入氢氧化钠溶液,若先产生___________色沉淀,该沉淀在空气中迅速变为灰绿色,最终变为_________色,则含该离子。
(3)实验室检验D溶液中的阳离子时,通常可滴加_________,若溶液变为_______色,则含该离子。
(4)若E是一种黄绿色气体单质,该气体是________________,在C→D过程中,此气体做_________剂。
(5)写出固体B与过量盐酸反应的离子方程式__________________________。
(6)写出D + A→C的离子方程式__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组为了探究一种无机矿物质X(仅含四种元素)的组成和性质,设计并完成如下实验:
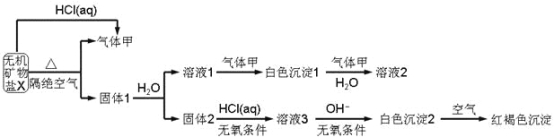
另取10.80gX在惰性气流中加热至完全分解,得到6.40g固体1.请回答如下问题:
(1)画出白色沉淀1中金属元素的原子结构示意图_______,写出气体甲的电子式_______。
(2)X的化学式是______,在惰性气流中加热X至完全分解的化学反应方程式为_______。
(3)白色沉淀2在空气中变成红褐色沉淀的原因是_______(用化学反应方程式表示)。
(4)一定条件下,气体甲鱼固体1中的某种成分可能发生氧化还原反应,写出一个可能的化学反应方程式_______,并设计实验方案验证该反应的产物_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置,其中按要求设计正确的是
A. 电解饱和食盐水并验证产物 | B. 铜锌原电池电流方向如图所示 |
C. 在钥匙上电镀银 | D. 电解精炼铜 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,溶液M中存在的离子有A2- HA- H+ OH-等,存在的分子有H2O 、H2A 。根据题意回答下列问题:
(1)写出酸H2A的电离方程式:__________________________________________
(2)若溶液M由10mL 2mol.L-1NaHA溶液与10mL 2mol.L-1NaOH溶液混合而得,则溶液M中离子浓度由大到小的顺序为_____________________。已知常温下,Ksp(BaA)=1.8×10-10,向该混合溶液中加入10mL 1mol.L-1BaCl2溶液,混合后溶液中的C(Ba2+)为__________mol.L-1。
(3)若NaHA溶液呈碱性,则溶液M有下列三种情况:①0.01 mol.L-1的H2A溶液;②0.01 mol.L-1的NaHA溶液;③0.02 mol.L-1的HCl溶液与0.04 mol.L-1的NaHA溶液等体积混合而成。则三种情况的溶液中C(H2A)最大的为__________(填序号,下同);pH由大到小的顺序为_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课题组以纳米Fe2O3作为电极材料制备锂离子电池(另一极为金属锂和石墨的复合材料),通过在室温条件下对锂离子电池进行循环充放电,成功地实现了对磁性的可逆调控(如图)。下列说法错误的是
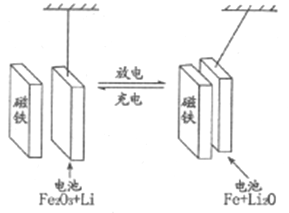
A. 放电时,负极的电极反应式为Li-e-=Li+
B. 放电时,电子通过电解质从Li流向Fe2O3
C. 充电时,Fe做阳极,电池逐渐摆脱磁铁吸引
D. 充电时,阳极的电极反应式为2Fe+3Li2O-6e-= Fe2O3+6Li+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烷烃的1个分子中含有9个碳原子,其一氯代物只有两种,该烷烃的名称是( )
A.正壬烷B.2,6-二甲基庚烷
C.2,2,4,4-四甲基戊烷D.2,3,4-三甲基己烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员研制出一种室温“可呼吸”Na—CO2电池。放电时该电池“吸入”CO2,充电时“呼出”CO2。“吸入”CO2时,其工作原理如下图所示。吸收的全部CO2中,有2/3转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面。下列说法中错误的是
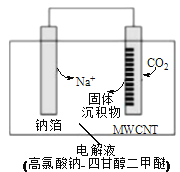
A. “吸入”CO2时,电流流向为:MWCNT→导线→钠箔
B. “呼出”CO2时,Na+向多壁碳纳米管电极移动
C. 放电时,正极的电极反应式为:3CO2+4Na++4e-=2Na2CO3+C
D. 电解液选用高氯酸钠-四甘醇二甲醚的优点是导电性好,与金属钠不反应,难挥发
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com