
【题目】高温下,反应CO+H2O![]() CO2+H2 达平衡。恒容时,温度升高,H2浓度减小。下列说法正确的是
CO2+H2 达平衡。恒容时,温度升高,H2浓度减小。下列说法正确的是
A. 该反应的焓变为负值
B. 恒温恒容下,增大压强,平衡一定不动
C. 升高温度,正反应速率减小
D. 平衡常数 ![]()
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】如图所示,把试管放入盛有25℃饱和石灰水的烧杯中,试管中开始放入几小块镁片,再滴入5mL稀盐酸。

回答下列问题:
(1)实验中观察到的现象是________________。
(2)产生上述现象的原因是________________。
(3)写出有关反应的离子方程式____________。
(4)由实验推知,MgCl2溶液和H2的总能量________(填“大于”、“小于”或“等于”)镁片和盐酸的总能量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的恒容容器中,当下列物理量不再发生变化时,不能表明反应A(s)+3B(g)![]() 2C(g)+D(g)已达平衡状态的是
2C(g)+D(g)已达平衡状态的是
A. B的物质的量浓度 B. 混合气体的密度
C. 混合气体的压强 D. v(B消耗)=3v(D消耗)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值,下列说法正确的是
A. 2gD2O和H2l8O混合物中所含中子数为NA
B. 1L0.1mol·L-1 NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA
C. 常温常压下,0.5 mol Fe和足量浓硝酸混合,转移电子数为1.5NA
D. 0.1 mol H2和0.1 mol I2 (g)于密闭容器中充分反应,其原子总数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题。
(1)现有下列物质:①CO2 ②液态氯化氢 ③CH4 ④熔融NaOH ⑤NH4Cl固体 ⑥氨水
请用序号回答下列问题:能导电的是___。属于电解质的是___。属于非电解质的是___。
(2)K2SO4和Fe2(SO4)3的混合溶液,已知其中Fe3+的浓度为0.5mol/L,SO42-浓度为0.9mol/L,则K+的物质的量浓度为___mol/L。
(3)1.204×1024个H2SO4分子的物质的量为___mol,共含___个氢原子。将上述H2SO4溶于水配成600mL溶液,再加水稀释到1000mL,稀释后溶液的物质的量浓度为___mol/L。
(4)15.6gNa2R2中含0.4mol的Na+,则R的相对原子质量是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
称取粗盐![]()
![]()
![]()
![]()
![]() 滤液
滤液![]()
![]() 精盐
精盐
(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,作用是___。
(2)在第③步操作中,选择的除杂剂NaOH不能用KOH代替,理由是___。
(3)第④步中加入过量的Na2CO3的目的是___。
(4)在第⑤步“过滤”操作中得到沉淀的成分有:泥沙、BaSO4、Mg(OH)2、___(填化学式)。
(5)写出第⑥步操作反应的离子方程式:___、___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将 CO2 在一定条件下与 H2 反应转化为甲醇(CH3OH)是变废为宝的好办法,一定条件下,每转化 44 kg CO2 放出的热量为 49000 kJ,CO2 转化为甲醇过程中浓度随时间的变化曲线如图所示(已知反应物和生成物在此条件下均为气体),下列叙述中正确的是

A. 0~3 min 内,用 CO2 和 H2 来表达的平均反应速率相等,均为 0.5 mol/(L·min)
B. 此反应的热化学方程式为 CO2(g) + 3H2(g) CH3OH(g) + H2O(g) △H = - 49 kJ/mol
C. 此条件下反应的平衡常数K=0.753×1.25/(0.75×0.75)
D. 降低温度,此反应的平衡常数可能为 0.8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在 20 L 的密闭容器中按物质的量之比 1∶2 充入 CO 和 H2,发生:CO(g)+2H2(g)CH3OH(g) ΔH。测得 CO 的转化率随温度的变化及不同压强下的变化,p2 和 195 ℃时 n(H2)随时间的变化结果如图表所示。下列说法正确的是( )

A. 0~3 min,平均速率 v(CH3OH)=0.8 mol·L-1·min-1
B. p1<p2,ΔH>0
C. 在 B 点时,v 正>v 逆
D. 在 p2 及 195 ℃时,该反应的平衡常数为 25
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带、海藻中含有大量的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如图:
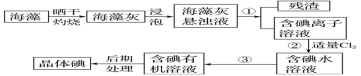
(1)实验室灼烧海带,需要下列仪器中的___(填字母)。
a.试管 b.烧杯 c.坩埚 d.泥三角 e.铁三脚架 f. 酒精灯
(2)指出提取碘的过程中有关的实验操作名称:
①____,③____。
(3)提取碘的过程中,可选择的有机试剂是___。
A.苯、酒精 B.四氯化碳、苯
C.汽油、乙酸 D.汽油、酒精
(4)为使海藻灰中碘离子转化为碘的有机溶液,实验室有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品,尚缺少的玻璃仪器有___、__。
(5)从含碘的有机溶液中提取碘和回收有机溶剂,还须经过蒸馏,指出下面实验装置图中的错误之处:
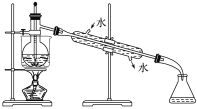
①_____;
②_____;
③_____。
(6)进行上述蒸馏操作时,使用水浴加热的原因是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com