
21.Cl元素位于元素周期表的第三周期 族, Cl原子的结构示意图为 。
22.不能比较硫、氯的非金属性强弱的是 (选填编号)。
a.S2-、Cl-的还原性 b.高氯酸和硫酸的酸性
c.H-Cl键和H-S键的稳定性 d.氯化钠和硫化钠溶液的pH
23.漂粉精可由Cl2通入消石灰中制备,漂粉精的有效成分是 ;将硝酸银溶液滴入下列物质的溶液中,无明显现象的是 (选填编号)。
a.碘化钾 b.氯酸钾 c.氯水 d.盐酸
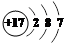
21.Ⅶ; (各1分)。22.d(2分)。23.Ca(ClO)2(1分);b(1分)。
解析试题分析:21.Cl元素是17号元素,原子核外电子为2,8,7,故位于元素周期表的第三周期VIIA族。
22.a.S2-、Cl-的还原性:S2-+Cl2→2Cl-+S,可以比较单质非金属性;b.高氯酸和硫酸的酸性,酸性越强,非金属性越强;c.稳定性H-Cl键强于H-S键,Cl的非金属性强于S;d.氯化钠和硫化钠溶液的pH,说明HCl水溶液的酸性强于H2S,但不是最高价氧化物的水化物,不能判断。
23.漂粉精可由Cl2通入消石灰中制备,2Ca(OH)2+2Cl2→Ca(ClO)2+CaCl2+2H2O,漂粉精的有效成分是Ca(ClO)2;硝酸银溶液不与氯酸钾溶液反应,无明显现象。
考点:氯的结构、元素及其化合物的性质。


科目:高中化学 来源: 题型:单选题
标准状况下2.24LH2和Cl2组成的混合气体,经光照后缓缓通入100ml 1mol/LNaOH溶液中充分反应,测得最终溶液中NaClO的浓度为0.1mol/L(假设溶液体积不变,且不考虑水解),则原混合气体中Cl2的体积分数为( )
| A.55% | B.60% | C.65% | D.70% |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
化合物A由N、H两种元素组成,0.01mol A与足量CuO充分反应生成红色Cu的同时,生成了0.36g水和标准状况下的体积为0.224L的N2。B是由Na和H两元素组成的离子化合物,能与水反应生成H2,称为产氢剂。化合物C的焰色反应为黄色,根据质谱分析它的相对分子质量为39且与水反应能生成氨气。
(1)A的化学式为 ;A与CuO反应的化学方程式为 。
(2)B的电子式为 。
(3)C中存在的化学键 ;C与过量稀盐酸反应的化学方程式为 。
(4)有一种理想的化合物NH4H,经查阅资料,该物质至今未能制得,请说明可能的原因
。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
在KBr和KI的混合液中通入过量的Cl2,除了水分子外,溶液中主要有 ______分子,若把溶液蒸干得到固体灼烧后还剩下 ____________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(4分)(1)写出下列物质的化学式:①漂白粉的有效成分: ;②钡餐: 。
(2)写出用Na2SO3与浓H2SO4反应制备SO2的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
NH3经一系列反应可以得到HNO3,如下图所示。
(1)I中,NH3和O2在催化剂作用下反应,其化学方程式是_____________________。
(2)II中,2NO(g)+O2 2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线(如右图)。
2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线(如右图)。
①比较P1、P2的大小关系:________________。
②随温度升高,该反应平衡常数变化的趋势是________________。
(3)III中,降低温度,将NO2(g)转化为N2O4(l),再制备浓硝酸。
①已知:2NO2(g) N2O4(g)△H1
N2O4(g)△H1
2NO2(g) N2O4(l)△H2
N2O4(l)△H2
下列能量变化示意图中,正确的是(选填字母)_______________。
②N2O4与O2、H2O化合的化学方程式是_________________。
(4)IV中,电解NO制备 NH4NO3,其工作原理如右图所示,为使电解产物全部转化为NH4NO3,需补充物质A,A是_____________,说明理由:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某含氯化合物A由两种短周期元素组成,常温下该物质为气态,测得该气体对空气的相对密度为3.0,A溶于水可得只含单一溶质B的弱酸性溶液,B溶液在放置过程中其酸性会增强。常温下,气体A与NH3反应生成离子晶体C、气体单质D和常见液体E,D为空气中含量最多的物质。气体A可用某一气体单质与潮湿的Na2CO3反应制得,同时生成两种钠盐。请回答下列问题:
(1)气体A的化学式为 ,气体单质D对应元素在周期表中的位置为 。
(2)用化学方程式表示B溶液酸性增强的原因 。
(3)气体A与NH3反应的化学方程式为 ,该反应体现气体A具有 性。
(4)试写出制取气体A的化学方程式为 。
(5)设计实验探究离子晶体C的成分为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某同学对Cl2与KI溶液的反应进行了实验探究。反应装置如下:
通入氯气一段时间,KI溶液变为黄色。继续通入氯气一段时间后,溶液黄色褪去,变为无色。继续通入氯气,最后溶液变为浅黄绿色。
(1)已知I2+I- I3- ,I2、I3-在水中均呈黄色。为确定黄色溶液的成分,进行了以下实验。
I3- ,I2、I3-在水中均呈黄色。为确定黄色溶液的成分,进行了以下实验。
| | 操作 | 实验现象 |
| a | 取2~3 mL黄色溶液,加入足量CCl4, 振荡静置。 | CCl4层呈紫红色, 水层显浅黄色。 |
| b | 取2~3 mL饱和碘水,加入足量CCl4, 振荡静置。 | CCl4层呈紫红色,水层几近无色。 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com