
【题目】下列关于硅及其化合物的叙述错误的是
A.SiO2很稳定,与所有的酸都不反应B.水晶、玛瑙的主要成分都是SiO2
C.陶瓷、玻璃、水泥都是硅酸盐产品D.水玻璃是一种常用的矿物胶
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】常温常压下,在带有相同质量活塞的容积相等的甲、乙两容器里,分别充有二氧化氮和空气,现分别进行下列两上实验:(N2O4![]() 2NO2 △H > 0)
2NO2 △H > 0)
(a)将两容器置于沸水中加热
(b)在活塞上都加2 kg的砝码
在以上两情况下,甲和乙容器的体积大小的比较,正确的是( )
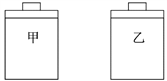
A. (a)甲>乙,(b)甲>乙 B. (a)甲>乙,(b)甲=乙
C. (a)甲<乙,(b)甲>乙 D. (a)甲>乙,(b)甲<乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于指定粒子构成的叙述中,不正确的是( )
A. 14C与16O具有相同的中子数
B. ![]() 与
与![]() 具有相同的最外层电子数
具有相同的最外层电子数
C. ![]() 与OH-具有相同的质子数和电子数
与OH-具有相同的质子数和电子数
D. Na2O2和Na2O具有相同的阴阳离子个数比
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某磁黄铁矿的主要成分是FexS(S为-2价),既含有Fe2+,又含有Fe3+,将一定量的该磁黄铁矿与100mL的盐酸恰好完全反应(注:矿石中其他成分不与盐酸反应),生成2.4g硫单质,0.425mol FeCl2 和一定量H2S气体,且溶液中无Fe3+。则下列说法正确的是
A. 该盐酸的物质的量浓度为4.25mol·L-1
B. 该磁黄铁矿FexS中,Fe2+与Fe3+的物质的量之比为3∶1
C. 成的H2S气体在标准状况下的体积为2.24L
D. 该磁黄铁矿中FexS的x=0.85
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ZrO2常用作陶瓷材料,可由锆英砂(主要成分为ZrSiO4,也可表示为ZrO2·SiO2,还含少量Fe2O3、Al2O3、SiO2等杂质)通过如下方法制取:
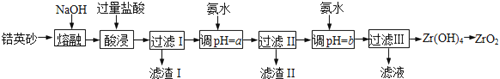
已知:①ZrO2能与烧碱反应生成可溶于水的Na2ZrO3,Na2ZrO3与酸反应生成ZrO2+。
②部分金属离子在实验条件下开始沉淀和完全沉淀的pH如下表。
金属离子 | Fe3+ | Al3+ | ZrO2+ |
开始沉淀时pH | 1.9 | 3.3 | 6.2 |
沉淀完全时pH | 3.2 | 5.2 | 8.0 |
(1)熔融时ZrSiO4发生反应的化学方程式为 ,滤渣I的化学式为 。
(2)为使滤液I的杂质离子沉淀完全,需用氨水调pH=a,则a的范围是 ;继续加氨水至pH=b时,所发生反应的离子方程式为 。
(3)向过滤III所得滤液中加入CaCO3粉末并加热,得到两种气体。该反应的离子方程式为 。
(4)为得到纯净的ZrO2,Zr(OH)4需要洗涤,检验Zr(OH)4是否洗涤干净的方法是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应mA(s)+nB(g)![]() pC(g) △H<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,下列叙述中一定正确的是
pC(g) △H<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,下列叙述中一定正确的是

①m+n>p ②x点表示的正反应速率大于逆反应速率
③n>p ④x点比y点时的反应速率慢
⑤若升高温度,该反应的平衡常数增大
A. ①②⑤ B. 只有②④ C. 只有①③ D. ①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫及其化合物在生产生活中应用广泛。回答下列问题:
(1)铁铵矾是一种化学物质,分子式是 NH4Fe(SO4)2·12H2O,其溶于水后,溶液中的离子浓度大小关系为__________________。
(2)已知某溶液中含有 CO32-、SO42-等离子,取一定量的该溶液,向其中滴加BaCl2溶液,当 CO32-开始沉 淀时,溶液中c(CO32-)/c(SO42-)为_______________。(已知 Ksp(BaSO4 )=1.0×10-10 ,Ksp(BaCO3)=2.5×10-9 )
(3)已知:S2Cl2(l)+Cl2(g)=2SCl2(l) ΔH=-50.2kJ·mol-1 。断裂 1molCl-Cl键、1molS-S键分别需要吸收 243kJ、268kJ 的能量,则断裂 1mol S-Cl键需要吸收的能量为____kJ。
(4)用 NaOH 溶液吸收烟气中的 SO2,将所得的 Na2SO3 溶液进行电解,可以制备H2SO4,其原理如下图所示(电极材料为石墨)。
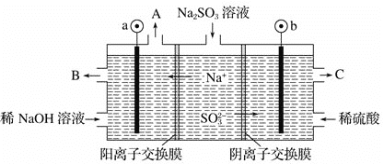
阳极的电极反应式为______________________;其中可循环使用的物质是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温条件下将气体A、B置于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g) ![]() 2C(g)+2D(g),反应进行到10s末,达到平衡,测得A的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为0.8mol,则:
2C(g)+2D(g),反应进行到10s末,达到平衡,测得A的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为0.8mol,则:
(1)用C表示10s内正反应的化学反应速率为___________;
(2)反应前A的物质的量浓度是___________;
(3)平衡时A的转化率为___________;
(4)能说明该反应达到平衡状态的是______________。
A.消耗3molA同时生成2molC B.反应体系中各物质的百分含量不变
C.混合气体平均相对分子质量不变 D.2V正(A)=3V逆(C)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列生产生活中所采取的措施不能用化学反应速率解释的是
A.有些食物的标签上注明须冷藏B.在糕点制作过程中添加防腐剂
C.在轮胎制品中加入适量的炭黑D.燃煤发电时常用煤粉代替煤块
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com