
【题目】下列变化中,一定需加还原剂才能实现的是( )
A. CO2 → CO32- B. FeCl3 → FeCl2 C. C → CO2 D. HCl → MgCl2
科目:高中化学 来源: 题型:
【题目】在元素周期表第三周期中,置换酸中氢能力最强的元素的元素符号为_____,最高价氧化物对应水化物的酸性最强的化合物的化学式是__________,碱性最强的化合物的化学式是__________,显两性的氢氧化物的化学式是__________,该两性氢氧化物与盐酸、氢氧化钠溶液分别反应的离子方程式为__________________、_________________,原子半径最大的金属元素的名称是________,离子半径最小的离子结构示意图是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用序号填写下列空格:
(1)下列各组物质
①O2和O3 ②H2、D2和T2 ③12C和14 C ④石墨和足球烯(C60)
⑤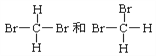 ⑥
⑥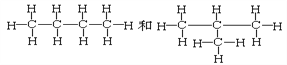
⑦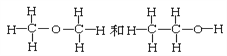 ⑧CH3CH3和CH3CH2CH2CH3
⑧CH3CH3和CH3CH2CH2CH3
互为同素异形体的是_____________;互为同位素的是______________,互为同分异构体的是______________,互为同系物的是_______________,同一种物质的是______________。
(2)现有① 金刚石 ② 干冰 ③ Na2SO4 ④ NH4Cl 四种物质,按下列要求回答:
晶体熔化时需要破坏共价键的是____________;熔点最低的是__________________;
晶体中只存在一种微粒间作用力是______________;属于离子晶体的是_____________。
请写出④ NH4Cl的电子式___________________
试判断 ①金刚石②干冰 ③Na2SO4晶体的熔点由高到低排列的顺序_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合氯化铝是一种新型净水剂,其中铝的总浓度(用c表示)包括三类:主要为A l3+的单体形态铝(用Ala表示)总浓度,主要为主要为[AlO4 Al12(OH)24(H2O)12 ]7+的中等聚合形态铝总浓度(用Alb 表示)和Al(OH)3胶体形态铝(用A1c表示)总浓度。
(1)真空碳热还原一氧化法可实现由铝土矿制备金属铝,相关反应的热化学方程式如下:
①Al2O3(s)+AlCl3(g)+3C(s)=3AlCl(g)+3CO(g)△H1=akJ·mol-1
②3AlCl(g)= 2Al(s)+AlCl3(g) △H2=bkJ·mol-1
则反应Al2O3(s)+33C(s)= 2Al(s)+ 3CO(g)△H=______kJ·mol-1(用含a、b的代数式表尔)。 反应①在常压、1900 ℃ 的高温下才能进行,说明△H______( 填“>”“=”或“<”)。
(1)用膜蒸馏(简称MD)浓缩技术将聚合氯化铝溶液进行浓缩,实验过程中不同浓度聚合氯化铝溶液中铝形态分布(百分数)如下表:
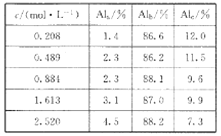
①在一定温度下,c越大,Al(OH)3胶体的百分含量______(填“越大”“越小”或“不变”)。
②若将c=2.520mol/L的聚合氯化铝溶液加水稀释,则稀释过程中发生的主要反应的离子方程式为_____________。
(3)一定条件下,向1.0mol/L的AlCl3溶液中加入0.6 mol/L的NaOH溶液,可制得Alb含量约为86 % 的聚合氯化铝溶液。写出生成[AlO4 Al12(OH)24(H2O)12 ]7+的离子方程式:_______。
(4)已知Al3++4X=2![]() ,X表示显色剂,
,X表示显色剂, ![]() 表示有色物质,通过比色分析得到25 ℃时Al3+浓度随时间的变化关系如图所示(初始时X的浓度为0.194mol·L-1)。
表示有色物质,通过比色分析得到25 ℃时Al3+浓度随时间的变化关系如图所示(初始时X的浓度为0.194mol·L-1)。

①1min时, ![]() 的浓度为___________。
的浓度为___________。
②0~3min内该反应的速率vx=________。
③第9min时,反应达到平衡,K=__________(用代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:
CO(g)+H2S(g)![]() COS(g)+H2(g) K=0.1
COS(g)+H2(g) K=0.1
反应前CO物质的量为10mol,平衡后CO物质的量为8mol。下列说法正确的是
A.升高温度,H2S浓度增加,表明该反应是吸热反应
B.通入CO后,正反应速率逐渐增大
C.反应前H2S物质的量为7mol
D.CO的平衡转化率为80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质]氢化铝钠(NaAlH4)是一种新型轻质储氢材料,掺入少量Ti的NaAlH4在150℃时释氢,在170℃、15.2MPa条件下又重复吸氢。NaAlH4可由AlCl3和NaH在适当条件下合成。NaAlH4的晶胞结构如右下图所示。

(1)基态Ti原子的价电子轨道表示式为 。
(2)NaH的熔点为800℃,不溶于有机溶剂。NaH属于 晶体,其电子式为 。
(3)AlCl3在178℃时升华,其蒸气的相对分子质量约为267,蒸气分子的结构式为 (标明配位键)。
(4)AlH4-中,Al的轨道杂化方式为 ;例举与AlH4-空间构型相同的两种离子 (填化学式)。
(5)NaAlH4晶体中,与Na+紧邻且等距的AlH4-有 个;NaAlH4晶体的密度为 g·cm-3(用含a的代数式表示)。若NaAlH4晶胞底心处的Na+被Li+取代,得到的晶体为 (填化学式)。
(6)NaAlH4的释氢机理为:每3个AlH4-中,有2个分别释放出3个H原子和1个Al原子,同时与该Al原子最近邻的Na原子转移到被释放的Al原子留下的空位,形成新的结构。这种结构变化由表面层扩展到整个晶体,从而释放出氢气。该释氢过程可用化学方程式表示为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烯烃在化工生产过程中有重要意义。下面是以烯烃A为原料合成粘合剂M的路线图。

回答下列问题:
(1)下列关于路线图中的有机物或转化关系的说法正确的是_______(填字母)。
A.A能发生加成、氧化、缩聚等反应
B.B的结构简式为CH2ClCHClCH3
C.C的分子式为C4H5O3
D.M的单体是CH2=CHCOOCH3和CH2=CHCONH2
(2)A中所含官能团的名称是_______,反应①的反应类型为_________。
(3)设计步骤③⑤的目的是_________, C的名称为________。
(4)C和D生成粘合剂M的化学方程式为____________。
(5)满足下列条件的C的同分异构体共有__种(不含立体异构),写出其中核磁共振氢谱有3组峰的同分异构体的结构简式:_____________。
①能发生银镜反应 ② 酸、碱性条件下都能水解 ③ 不含环状结构
(6)结合信息,以CH3CH=CHCH2OH为原料(无机试剂任选),设计制备CH3CH=CHCOOH的合成路线。合成路线流程图示例如下:_____________
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,a、b、c、d、e为元素周期表中前4周期的一部分元素,下列有关叙述正确的是( )
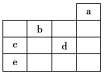
A. 元素b位于第ⅥA族,有+6、-2价两种常见化合价
B. 五种元素中,元素e的性质最稳定
C. 元素c和d的最高价氧化物对应的水化物的酸性:c>d
D. 元素c和e的气态氢化物的稳定性:c>e
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com