
ЎҫМвДҝЎҝФЪТ»¶ЁОВ¶ИПВЈ¬ФЪМе»эОӘ2LөДәгИЭГЬұХИЭЖчЦРЈ¬ДіТ»·ҙУҰЦРXЎўYЎўZИэЦЦЖшМеөДОпЦКөДБҝЛжКұјдұд»ҜөДЗъПЯИзНјЛщКҫЈ¬ПВБРұнКцЦРХэИ·өДКЗ

A. ·ҙУҰөД»ҜС§·ҪіМКҪОӘ2X = 3Y + Z
B. tКұЈ¬XөДЧӘ»ҜВКҙп66.7%
C. Ифt=4Ј¬Фт0Ў«tөДXөД»ҜС§·ҙУҰЛЩВКОӘ0.1 molLЈӯ1minЈӯ1
D. ОВ¶ИЎўМе»эІ»ұдЈ¬tКұҝМідИл1 mol HeК№С№ЗҝФцҙуЈ¬ХэЎўДж·ҙУҰЛЩВК¶јФцҙу
Ўҫҙр°ёЎҝC
ЎҫҪвОцЎҝ
A.УЙНјПуҝЙТФҝҙіцЈ¬·ҙУҰЦРXОпЦКөДБҝјхРЎЈ¬YЎўZөДОпЦКөДБҝФц¶аЈ¬ФтXОӘ·ҙУҰОпЈ¬YЎўZОӘЙъіЙОпЈ¬ЗТЎчn(X)ЈәЎчn(Y)ЈәЎчn(Z)=0.8molЈә1.2molЈә0.4mol=2Јә3Јә1Ј¬·ҙУҰЧоЦХҙпөҪЖҪәвЈ¬ёГ·ҙУҰОӘҝЙДж·ҙУҰЈ¬ФтёГ·ҙУҰөД»ҜС§·ҪіМКҪОӘЈә2X3Y+ZЈ¬№КAПоҙнОуЈ»
B. XөДЖрКјОпЦКөДБҝОӘ2.4molЈ¬tКұОпЦКөДБҝОӘ1.6 molЈ¬ЧӘ»ҜВК=![]() = 33.3%Ј¬№КBПоҙнОуЈ»
= 33.3%Ј¬№КBПоҙнОуЈ»
C.Ифt=4Ј¬Фт0Ў«tөДXөД»ҜС§·ҙУҰЛЩВКҰФ= ![]() molL-1min-1=0.1 molL-1min-1Ј¬№КCПоХэИ·Ј»
molL-1min-1=0.1 molL-1min-1Ј¬№КCПоХэИ·Ј»
D.ОВ¶ИЎўМе»эІ»ұдЈ¬tКұҝМідИл1 mol HeК№С№ЗҝФцҙуЈ¬ХэЎўДж·ҙУҰЛЩВКІ»ұдЈ¬№КDПоҙнОуЎЈ
ҙр°ёОӘCЎЈ



| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝТ»ЦЦРВРНДЖБтөзіШҪб№№КҫТвНјИзНјЈ¬ПВБРУР№ШёГөзіШөДЛө·ЁХэИ·өДКЗ

A.өзіШ·ЕөзКұЈ¬Na+Птөзј«Aј«ТЖ¶Ҝ
B.өзіШ·ЕөзКұЈ¬Aј«өзј«·ҙУҰОӘ2Na++xS+2e-= Na2Sx
C.өзіШідөзКұЈ¬BҪУёәј«
D.өзіШідөзКұЈ¬ГҝЧӘТЖ1molөзЧУҪ«УР1mol Na+ұ»»№Фӯ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВНјЛщКҫОӘ№ӨТөәПіЙ°ұөДБчіМНјЎЈУР№ШЛө·ЁҙнОуөДКЗ

A. ІҪЦиўЩЦРЎ°ҫ»»ҜЎұҝЙТФ·АЦ№ҙЯ»ҜјБЦР¶ҫ
B. ІҪЦиўЪЦРЎ°јУС№ЎұјИҝЙТФМбёЯФӯБПөДЧӘ»ҜВКЈ¬УЦҝЙТФјУҝм·ҙУҰЛЩВК
C. ІҪЦиўЫЎўўЬЎўўЭҫщУРАыУЪМбёЯФӯБПөДЧӘ»ҜВК
D. ІъЖ·Тә°ұіэҝЙЙъІъ»Ҝ·КНвЈ¬»№ҝЙУГЧчЦЖАдјБ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝіЈОВПВЈ¬№ШУЪpHПаөИөДСОЛбИЬТәәНҙЧЛбИЬТәЈ¬ПВБРЛө·ЁІ»ХэИ·өДКЗ
A. ҙЧЛбИЬТәөДөзАл·ҪіМКҪЈәCH3COOH![]() H+ + CH3COO-
H+ + CH3COO-
B. c(Cl-) = c(CH3COO-)
C. өИМе»эөДСОЛбИЬТәәНҙЧЛбИЬТә·ЦұрУлЧгБҝөДZnНкИ«·ҙУҰЈ¬·ҙУҰҝӘКјКұІъЙъH2өДЛЩВКТ»Сщҝм
D. УГПаН¬ЕЁ¶ИөДNaOHИЬТә·ЦұрУлСОЛбәНҙЧЛбИЬТәЗЎәГ·ҙУҰНкИ«Ј¬ПыәДөДNaOHИЬТәМе»эТ»Сщ¶а
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝөӘөД»ҜәПОпФЪ»Ҝ·КЎўТҪТ©ЎўХЁТ©ЎўІДБПөИБмУтЦРУРЧЕј«ЖдЦШТӘУГНҫЎЈ
ЈЁ1Ј©фЗ°ұДЬУлде»ҜТшРьЧЗТә·ҙУҰЈә2NH2OH+2AgBr=N2Ўь+2Ag+2HBr+2H2OЈ¬фЗ°ұөДөзЧУКҪОӘ________Ј»·ҙУҰЦРМю°ұұнПЦ________РФЈ®
ЈЁ2Ј©ТСЦӘЈәa.N2(g)+3H2(g)=2NH3(g) ЎчH=-92.2kJ/mol
b.H2(g)+Cl2(g)=2HCl(g) ЎчH=-184.6kJ/mol
c.2NH3(g)+3Cl2(g)=N2(g)+6HCl(g) ЎчH3
ўЩЎчH3________Ј®
ўЪ·ҙУҰcФЪіЈОВПВДЬҝмЛЩҪшРРөДФӯТтОӘ________Ј®
ЈЁ3Ј©ИЭ»эҫщОӘ1LөДјЧЎўТТБҪёцИЭЖчЈ¬ЖдЦРјЧОӘҫшИИИЭЖчЈ¬ТТОӘәгОВИЭЖчЈ®ПаН¬ОВ¶ИПВЈ¬·ЦұрідИл0.2molөДNO2Ј¬·ўЙъ·ҙУҰЈә2NO2(g)ЁPN2O4(g) ЎчH<0Ј¬јЧЦРNO2өДПа№ШБҝЛжКұјдұд»ҜИзПВНјЛщКҫЎЈ
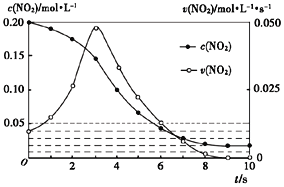
ўЩ0~3SДЪЈ¬јЧИЭЖчЦРNO2өД·ҙУҰЛЩВКФцҙуөДФӯТтКЗ________Ј®
ўЪјЧҙпЖҪәвКұЈ¬ОВ¶ИИфОӘTЎжЈ¬ҙЛОВ¶ИПВөДЖҪәвіЈКэKc=________Ј®
ўЫЖҪәвКұЈ¬KјЧ________KТТ(МоЎ°>ЎұЎўЎ°<Ўұ»тЎ°=ЎұЈ¬ПВН¬)Ј¬PјЧ________PТТ
ЈЁ4Ј©»ҜС§№ӨЧчХЯ¶ФNOУлH2өД·ҙУҰҪшРРСРҫҝЈ¬МбіцПВБР3ІҪ»ъАнЈә(kОӘЛЩВКіЈКэ)
өЪТ»ІҪ2NO=N2O2 ҝм·ҙУҰЈ¬ЖҪәвКұЈәVХэ=KХэЎӨc2(NO)=VДж=KДжЎӨc(N2O2)
өЪ¶юІҪN2O2+H2==N2O+H2O Вэ·ҙУҰ өЪИэІҪN2O+H2=N2+H2O ҝм·ҙУҰ
ЖдЦРҝЙҪьЛЖИПОӘөЪ¶юІҪ·ҙУҰІ»У°ПмөЪТ»ІҪЖҪәвЈ¬ПВБРЛө·ЁХэИ·өДКЗ________Ј®(МоЧЦДёұкәЕ)
AЈ®V(өЪТ»ІҪДж·ҙУҰ)<V(өЪ¶юІҪ·ҙУҰ) BЈ®ЧЬ·ҙУҰҝмВэЦчТӘУЙөЪ¶юІҪ·ҙУҰҫц¶Ё
CЈ®ҙпЖҪәвКұЈ¬2c(NO)=c(N2O2) DЈ®өЪТ»ІҪ·ҙУҰөДЖҪәвіЈКэK= KХэ/ KДж
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝТАҫЭПВБРКөСйПЦПуЈ¬ЛщөГҪбВЫІ»ХэИ·өДКЗ
КөСй | КөСйПЦПу |
| ўЩЖ·әмИЬТәәмЙ«НКИҘЈ¬ҫӯјмСйИЬТәЦРә¬УРSO42- ўЪјУИИНКЙ«әуөДИЬТәЦБ·РМЪЈ¬ОҙјыСХЙ«»ЦёҙЈ¬УРЖшМеТзіцЈ¬ҝЙК№А¶Й«КҜИпКФЦҪұдәмЈ¬Уцөн·Ыөв»ҜјШКФЦҪЈ¬ОЮГчПФұд»ҜЎЈ |
A. Ж·әмИЬТәНКЙ«КЗВИЛ®ЖҜ°ЧЛщЦВ
B. јҜЖшЖҝЦР·ўЙъБЛ·ҙУҰЈәCl2 + SO2 + 2H2O H2SO4 + 2HCl
C. ТАҫЭПЦПуўЪҝЙИ·¶ЁІъЙъөДЖшМеОӘSO2
D. јмСйSO42-өДКФјБОӘЈәСОЛбЎўBaCl2ИЬТә
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝДіКөСйРЎЧйУГТФПВјёёцКөСйЧ°ЦГМҪҫҝөз»ҜС§№эіМ¶ФҪрКфУлПЎБтЛб·ҙУҰЛЩВКөДУ°ПмЈ¬ЙХұӯЦР¶јКўУРПЎH2SO4ЎЈКФ»ШҙрЈә
ЈЁ1Ј©BЧ°ЦГЦРFeөзј«ЧчОӘ________ЈЁМоЎ°ХэЎұ»тЎ°ёәЎұЈ©ј«Ј¬өзј«·ҙУҰКҪОӘ______________Ј»
ЈЁ2Ј©CЧ°ЦГЦРСфАлЧУТЖПт_________ЈЁМоЎ°ZnЎұ»тЎ°FeЎұЈ©ј«Ј»
ЈЁ3Ј©ұИҪПЛДёцЧ°ЦГЦРFeЖ¬ұ»ёҜКҙөДЛЩВКУЙҝмөҪВэөДЛіРтКЗ_______ЈЁУГAЎўBЎўCЎўDұнКҫЈ©ЎЈ

Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝәгОВМхјюПВЈ¬ҝЙДж·ҙУҰЈә2NOЈЁgЈ©+O2ЈЁgЈ©![]() 2NO2ЈЁgЈ©ФЪМе»э№М¶ЁөДГЬұХИЭЖчЦРҪшРРЈ¬ҙпөҪЖҪәвЧҙМ¬өДұкЦҫөДКЗЈЁЎЎЎЎЈ©
2NO2ЈЁgЈ©ФЪМе»э№М¶ЁөДГЬұХИЭЖчЦРҪшРРЈ¬ҙпөҪЖҪәвЧҙМ¬өДұкЦҫөДКЗЈЁЎЎЎЎЈ©
ўЩөҘО»КұјдДЪЙъіЙn mol O2өДН¬КұЙъіЙ2n mol NO2ўЪөҘО»КұјдДЪЙъіЙn mol O2өДН¬КұЙъіЙ2n mol NOўЫУГNO2ЎўNOЎўO2ұнКҫөД·ҙУҰЛЩВКөДұИОӘ2Јә2Јә1өДЧҙМ¬ўЬ»мәПЖшМеөДСХЙ«І»ФЩёДұдөДЧҙМ¬ўЭ»мәПЖшМеөДГЬ¶ИІ»ФЩёДұдөДЧҙМ¬ўЮ»мәПЖшМеөДС№ЗҝІ»ФЩёДұдөДЧҙМ¬ўЯ»мәПЖшМеөДЖҪҫщПа¶Ф·ЦЧУЦКБҝІ»ФЩёДұдөДЧҙМ¬Ј®
A. ўЩўЬўЮўЯ B. ўЪўЫўЭўЯ C. ўЩўЫўЬўЭ D. И«Іҝ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБРРрКцЦРЈ¬ХэИ·өДКЗ
A. H2SO4өДДҰ¶ыЦКБҝКЗ98
B. өИЦКБҝөДO2әНO3ЦРЛщә¬өДСхФӯЧУКэПаН¬
C. өИЦКБҝөДCOУлCO2ЦРЛщә¬МјФӯЧУКэЦ®ұИОӘ7©U11
D. 98g H2SO4ИЬҪвУЪ500mLЛ®ЦРЈ¬ЛщөГИЬТәЦРБтЛбөДОпЦКөДБҝЕЁ¶ИОӘ2 mol/L
Ійҝҙҙр°ёәНҪвОц>>
№ъјКѧУУЕСЎ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com