解:(1)根据Zn及化合物的性质与Al及化合物的性质相似,Zn也能和氢氧化钠溶液反应,氢氧化钠溶液起到溶解镀锌层和去除油污作用,
故答案为:AB;
(2)调节溶液A的pH可产生Zn(OH)2沉淀,抽滤就可以得到氢氧化锌沉淀,洗涤除去附着的离子,高温灼烧氢氧化锌分解得到ZnO,
故答案为:抽滤、洗涤、灼烧;
(3)持续通入N2,防止Fe2+被氧化;
故答案为:在N2气氛下,防止Fe2+被氧化;
(4)Fe3O4胶体粒子能透过滤纸,所以不能用过滤的方法实现固液分离,
故答案为:不能;胶体粒子太小,抽滤时容易透过滤纸;
(5)m(K2Cr2O7)=0.01000mol?L-1×0.250 L×294.0 g?mol-1=0.7350g;
根据溶液浓度的精度,应选择电子天平用于称量固体质量,烧杯用于溶解固体,玻璃棒用于搅拌和引流操作,容量瓶用于配置溶液,胶头滴管用于加水定容.故用不到的仪器为量筒和移液管,
故答案为:0.7350g;③⑦;
(6)如果滴定前装有K2Cr2O7标准溶液的滴定管尖嘴部分有气泡,这样就造成读数偏小;滴定结束后气泡消失,这样读数就正常,所以读出来的K2Cr2O7标准溶液体积偏大,测定结果将偏大,
故答案为:偏大.
分析:(1)根据Zn及化合物的性质与Al及化合物的性质相似,Zn也能和氢氧化钠溶液反应,氢氧化钠溶液起到溶解镀锌层和去除油污作用;
(2)调节溶液A的pH可产生Zn(OH)2沉淀,抽滤就可以得到氢氧化锌沉淀,高温灼烧氢氧化锌分解得到ZnO;
(3)持续通入N2,防止Fe2+被氧化;
(4)Fe3O4胶体粒子能透过滤纸;
(5)根据m=cVM计算m(K2Cr2O7);
根据溶液浓度的精度,应选择电子天平用于称量固体质量,烧杯用于溶解固体,玻璃棒用于搅拌和引流操作,容量瓶用于配置溶液,胶头滴管用于加水定容;
(6)根据对K2Cr2O7标准溶液体积的影响分析.
点评:本题以“废旧镀锌铁皮可制备磁性Fe3O4胶体粒子及副产物ZnO”为载体,考查实验基本操作和技能,涉及标准溶液的配制及滴定的误差分析、对信息的利用、实验条件的控制等,试题难度中等,是对学生综合能力的考查,需要学生基本知识的基础与分析问题、解决问题的能力.




 名校课堂系列答案
名校课堂系列答案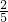 mol
mol mol
mol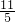 mol
mol mol
mol N2O4)
N2O4)