
【题目】下列有关说法正确的是( )
A.在轮船表面涂刷富锌油漆,能有效防止船体在海水中被腐蚀
B.0.1mol·L-1氨水加水稀释后,溶液中![]() 的值减小
的值减小
C.用pH均为2的盐酸和醋酸分别中和等物质的量的NaOH,消耗醋酸的体积更大
D.反应NH3(g)+HCl(g)=NH4Cl(s)在室温下可自发进行,则该反应的△H>0
【答案】A
【解析】
A.锌、铁和海水构成原电池,锌作负极被腐蚀,铁作正极被保护,A选项正确;
B.加水时电离平衡正向移动,n(NH4+)增大,n(NH3·H2O)减小,在同一溶液中体积相同,离子的浓度之比等于物质的量之比,则比值增大,B选项错误;
C.醋酸为弱酸,pH均为2的盐酸和醋酸溶液,两种溶液中H+浓度相等,则醋酸浓度大于盐酸,设盐酸的浓度为C1,醋酸的浓度为C2,则C1< C2 ,分别中和等体积、等物质的量浓度的氢氧化钠溶液,当氢氧化钠恰好被完全中和时,消耗的两种酸的物质的量相等,则有:n=C1V1=C2V2,因C1< C2,所以V1> V2,消耗盐酸的体积更大,C选项错误;
D.反应NH3(g)+ HCl(g)=== NH4Cl(s)在室温下可自发进行,△G=△H-T△S <0,△S< 0 ,则该反应的△H < 0,D选项错误;
答案选A。


科目:高中化学 来源: 题型:
【题目】对H2O2的分解速率影响因素进行研究。在相同温度下,实验测得不同条件下出O2浓度随时间变化如图所示。下列说法不正确的是( )
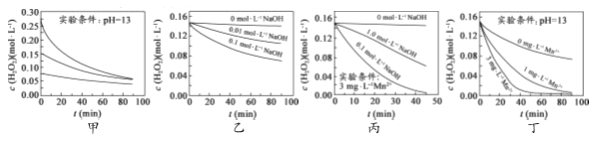
A. 图甲表明,可通过适当增大H2O2浓度,加快H2O2分解速率
B. 图乙表明,可通过调节溶液的酸碱性,控制H2O2分解速率快慢
C. 图丙表明,Mn2+少量存在时,碱性太强,不利于H2O2分解
D. 图乙、图丙和图丁表明,Mn2+是H2O2分解的催化剂,提高Mn2+的浓度就能增大H2O2 分解速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行。
已知:2CrO![]() +2H+===Cr2O
+2H+===Cr2O![]() +H2O Ba2++CrO
+H2O Ba2++CrO![]() ===BaCrO4↓
===BaCrO4↓
步骤Ⅰ移取x mL一定浓度的Na2CrO4溶液于锥形瓶中,加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸体积为V0 mL。
步骤Ⅱ:移取y mL BaCl2溶液于锥形瓶中,加入x mL与步骤Ⅰ相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1mL。滴加盐酸标准液时应用酸式滴定管,“0”刻度位于滴定管的________(填“上方”或“下方”)。BaCl2溶液的浓度为________mol·L-1,若步骤Ⅱ中滴加盐酸时有少量待测液溅出,Ba2+浓度测量值将________(填“偏大”或“偏小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或表示方法正确的是
A.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B.由C(石墨,s)=C(金刚石,s) △H=+1.9kJ/mol可知,金刚石比石墨稳定
C.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l) △H=﹣285.8kJ/mol
D.在稀溶液中,H+(aq)+OH﹣(aq)=H2O(l) △H=﹣57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含1molKOH的溶液混合,放出的热量大于57.3kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物中间体M的合成路线流程图

已知信息:
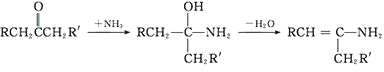
RCHO+ →
→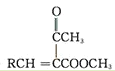 +H2O
+H2O
请回答下列问题:
![]() 下列说法中正确的是__________。
下列说法中正确的是__________。
A.化合物A只有1种结构可以证明苯环不是单双键交替的结构
B.可利用酸性![]() 溶液实现
溶液实现![]() 的转换
的转换
C.步骤![]() 、
、![]() 、
、![]() 所属的有机反应类型各不相同
所属的有机反应类型各不相同
D.化合物C具有弱碱性
![]() 化合物F的结构简式是__________。
化合物F的结构简式是__________。
![]() 步骤
步骤![]() 可得到一种与G分子式相同的有机副产物,其结构简式是__________。
可得到一种与G分子式相同的有机副产物,其结构简式是__________。
![]() 写出
写出![]() 的化学方程式__________。
的化学方程式__________。
![]() 写出
写出![]() 同时符合下列条件的同分异构体的结构简式__________。
同时符合下列条件的同分异构体的结构简式__________。
![]() 分子中具有联苯结构,能与
分子中具有联苯结构,能与![]() 溶液发生显色反应,能发生水解反应与银镜反应,且完全水解后只有两种物质的量之比为
溶液发生显色反应,能发生水解反应与银镜反应,且完全水解后只有两种物质的量之比为![]() 的水解产物;
的水解产物;![]() 谱和IR谱检测表明分子中有7种化学环境不同的氢原子,没有
谱和IR谱检测表明分子中有7种化学环境不同的氢原子,没有![]() 键。
键。
![]() 已知:CH3CHO+HCHO
已知:CH3CHO+HCHO![]() H2C=CHCHO,设计以
H2C=CHCHO,设计以![]() 、
、![]() 和
和 为原料制备
为原料制备 的合成路线流程图________________(无机试剂任选)。
的合成路线流程图________________(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应2C+O2=2CO的能量变化如图所示。下列说法正确的是( )
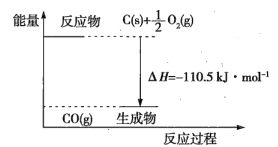
A.12gC(s)与一定量O2(g)反应生成14gCO(g)放出的热量为110.5kJ
B.2molC(s)与足量O2(g)反应生成CO2(g)放出的热量大于221kJ
C.该反应的热化学方程式是2C(s)+O2(g)=2CO(g) ΔH=-221kJ
D.该反应的反应热等于生成的CO(g)中所具有的能量与参加反应的O2(g)中所具有的能量的差
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:①H2(g)+![]() O2(g)=H2O(l)ΔH=-285.8kJ/mol②H2(g)+
O2(g)=H2O(l)ΔH=-285.8kJ/mol②H2(g)+![]() O2(g)=H2O(g)ΔH=-241.8kJ/mol③C(s)+
O2(g)=H2O(g)ΔH=-241.8kJ/mol③C(s)+ ![]() O2(g)=CO(g)ΔH=―110.4 kJ/mol④C(s)+O2(g)=CO2(g)ΔH=-393.5kJ/mol。回答下列各问:
O2(g)=CO(g)ΔH=―110.4 kJ/mol④C(s)+O2(g)=CO2(g)ΔH=-393.5kJ/mol。回答下列各问:
(1)上述反应中属于放热反应的是_______。(填序号)
(2)H2的燃烧热为___;C的燃烧热为____。
(3)燃烧4g H2生成液态水,放出的热量为_______。
(4)根据盖斯定律可知CO的燃烧热为_____;其热化学方程式为_____。
(5)比较下列各组热化学方程式中△H的大小:
①C(s)+O2(g)=CO2(g)△H1 C(s)+![]() O2(g)=CO(g) △H2 △H1 ____△H2
O2(g)=CO(g) △H2 △H1 ____△H2
②S(s)+O2(g)=SO2(g)△H3 S(g)+O2(g)=SO2(g) △H4 △H3 __△H4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有室温下的四种溶液:①pH=2的醋酸;②pH=a的Na2CO3溶液,体积为VL;③pH=2的硫酸;④pH=12的氢氧化钠溶液。下列有关说法正确的是( )
A.将②溶液用蒸馏水稀释,使体积扩大10倍,所得溶液pH变为(a-1)
B.V1L③溶液和V2L④溶液混合,若混合后溶液pH=3,则V1:V2=11:9
C.①与④两溶液等体积混合,混合液pH=7
D.①与③两溶液的物质的量浓度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、下列可用于分离和提纯物质的方法是
(1)分离NaCl溶液中的NaCl和水_________;
(2)分离乙醇和水的混合物___________;
(3)分离溴水中的溴和水_________;
(4)除去澄清石灰水中悬浮的CaCO3颗粒________;
II、掌握仪器的名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置。
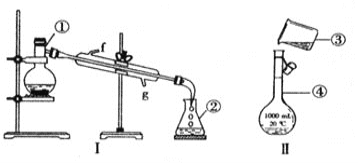
(1)写出下列仪器的名称:①_____________④______________
(2)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器__________;该分离操作的名称为__________;进行I分离操作时进水口为______(填f或g)。
(3)现需配制1000mL某溶液,其中装置II是该同学转移溶液的示意图,该同学操作的错误是_______;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com