
【题目】(1)在标准状况下①6.72L CH4②3.01×1023个HCl分子③13.6g H2S④0.2mol NH3,体积最大的是____,密最大的是度___,质量最小的是___,氢原子个数最多的是____。(填写序号)
(2)等温等压下,质子数相等的CO、N2两种气体,质量之比为____,体积之比为____,摩尔质量之比____。
(3)某物质在一定条件下加热分解,产物都是气体。分解方程式为:3A=B+3C+2D。测得生成的混合气体的平均相对分子质量为2a,则A的摩尔质量为____。
【答案】② ② ④ ① 1:1 1:1 1:1 4a g/mol
【解析】
(1)①6.72L CH4中:n(CH4)=![]() =0.3mol,m(CH4)=0.3mol×16g/mol=4.8g,ρ(CH4)=
=0.3mol,m(CH4)=0.3mol×16g/mol=4.8g,ρ(CH4)= ![]() ,N(H)=4N(CH4)=1.2NA;
,N(H)=4N(CH4)=1.2NA;
②3.01×1023个HCl分子中:n(HCl)=![]() =0.5mol,V(HCl)=0.5mol×22.4L/mol=11.2L,ρ(HCl)=
=0.5mol,V(HCl)=0.5mol×22.4L/mol=11.2L,ρ(HCl)=![]() ,m(HCl)=0.5mol×36.5g/mol=18.25g,N(H)=N(HCl)=0.5NA;
,m(HCl)=0.5mol×36.5g/mol=18.25g,N(H)=N(HCl)=0.5NA;
③13.6g H2S中:n(H2S)=![]() =0.4mol,V(H2S)=0.4mol×22.4L/mol=8.96L,ρ(H2S)=
=0.4mol,V(H2S)=0.4mol×22.4L/mol=8.96L,ρ(H2S)= ![]() ,N(H)=2N(H2S)=0.8NA;
,N(H)=2N(H2S)=0.8NA;
④0.2mol NH3中:m(NH3)=0.2mol×17g/mol=3.4g,V(NH3)=0.2mol×22.4L/mol=4.48L,ρ(NH3)= ![]() ,N(H)=3N(NH3)=0.6NA.
,N(H)=3N(NH3)=0.6NA.
所以:体积最大的是②,密度最大的是②,质量最小的是④,含氢原子数最多的是①;
(2)CO、N2两种气体涉及的元素有C、O、N质子数分别为6、8、7,所以两种气体的分子的质子数分别为:14、14,质子数相等的CO、N2,物质的量相等;CO、N2摩尔质量分别为28g/mol、28g/mol,故摩尔质量之比1:1;根据m=nM知:质量之比与摩尔质量成正比为28:28=1:1;根据阿伏伽德罗定律,相同条件下物质的量相等的气体具有相同的体积,故体积之比为1:1;
(3)化学方程式系数的意义:表示物质的量。设A的物质的量为3mol,则三种混合气体的总物质的量为6mol,由于平均相对分子质量为2a,即平均摩尔质量为2a g/mol,三种气体质量总和为12a g,根据质量守恒定律,A的质量也是12a g,故A的摩尔质量为4a g/mol。


科目:高中化学 来源: 题型:
【题目】如图所示,A处通入干燥的氯气,打开B阀后,C处的红布条逐渐退色,关闭B阀时,C处的红布条看不到明显现象,则D瓶中装的是( )

A. 浓硫酸B. 浓NaOH溶液
C. 浓盐酸D. 饱和NaCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示的一些物质或概念间的从属关系中正确的是

X | Y | Z | |
A | 过氧化钠 | 碱性氧化物 | 氧化物 |
B | 硫酸 | 化合物 | 电解质 |
C | 淀粉溶液 | 胶体 | 分散系 |
D | 置换反应 | 氧化还原反应 | 离子反应 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮气是制备含氮化合物的一种重要物质。两个常见的固氮反应[①N2(g)+3H2(g)![]() 2NH3(g)和②N2(g)+O2(g)
2NH3(g)和②N2(g)+O2(g)![]() 2NO(g)],其平衡常数对数值(lg K)与温度的关系如下图。根据图中的数据判断下列说法正确的是
2NO(g)],其平衡常数对数值(lg K)与温度的关系如下图。根据图中的数据判断下列说法正确的是

A. 反应①和②均为放热反应
B. 升高温度,反应①的反应速率减小
C. 在常温下,利用反应①固氮和利用反应②固氮,反应程度相差很大
D. 在1 000 ℃时,反应①和反应②体系中N2的浓度一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国化学家侯德榜根据NaHCO3溶解度比NaCl、Na2CO3、NH4HCO3、NH4Cl都小的性质,运用CO2+NH3+H2O+NaCl=NaHCO3↓+NH4Cl的反应原理制备纯碱.下面是在实验室进行模拟实验的生产流程示意图:
则下列叙述错误的是( )
A. A气体是NH3,B气体是CO2
B. 把纯碱及第Ⅲ步得到的晶体与某些固体酸性物质(如酒石酸)混合可制得发酵粉
C. 纯碱可广泛地用于玻璃、制皂、造纸、纺织等工业中
D. 第Ⅳ步操作是将晶体溶于水后加热、蒸发、结晶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下图是金属镁和卤素单质(X2)反应的能量变化示意图。
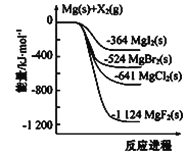
写出MgBr2(s)与Cl2(g)生成MgCl(s)和Br2(l)的热化学方程式______________________________。
(2)甲醇燃料电池(结构如图),质子交换膜左右两侧的溶液均为1L2mol·L-1H2SO4溶液。当电池中有2mol e-发生转移时,左右两侧溶液的质量之差为______g(假设反应物耗尽,忽略气体的溶解)。

(3)250mLK2SO4和CuSO4的混合溶液中c(SO42-)=0. 5mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到1.12L气体(标准状况下)。假定电解后溶液体积仍为250mL,写出阴极电极反应式______________原混合溶液中c(K+)=__________________
(4)NaHSO3溶液在不同温度下均可被过量![]() KIO3氧化。将浓度均为0.020mol/L
KIO3氧化。将浓度均为0.020mol/L![]() NaHSO3溶液(含少量淀粉)10ml
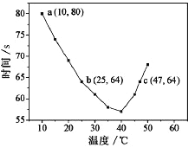
NaHSO3溶液(含少量淀粉)10ml![]() 、KIO3(过量)酸性溶液90.0ml混合,记录10—55℃间溶液变蓝时间,实验结果如图。据图分析,图中a点对应的
、KIO3(过量)酸性溶液90.0ml混合,记录10—55℃间溶液变蓝时间,实验结果如图。据图分析,图中a点对应的![]() NaHSO3反应速率为________________
NaHSO3反应速率为________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一混合物的水溶液,只可能含以下离子中的若干种:K+、Al3+、Fe3+、Mg2+、Ba2+、 NH4+、Cl-、CO32-、SO42-,现取三份100 mL溶液进行如下实验:① 第一份加入AgNO3溶液有沉淀产生,② 第二份加过量NaOH溶液加热后收集到气体0.02 mol,无沉淀生成,同时得到溶液甲,③ 在甲溶液中通过量CO2,生成白色沉淀,沉淀经过滤、洗涤、灼烧,质量为1.02 g,④ 第三份加足量BaCl2溶液后得白色沉淀,沉淀经足量盐酸洗涤干燥后质量为11.65 g。根据上述实验回答:
(1)一定不存在的离子是____________________,不能确定是否存在的离子是________________
(2)试确定溶液中肯定存在的阴离子及其浓度(可不填满):离子符号____________,浓度____________________
(3)试确定K+ 是否存在________ (填“是”或“否”),判断的理由是:____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对反应Al2O3+N2+3C ![]() 2AlN+3CO的叙述正确的是
2AlN+3CO的叙述正确的是
A. Al2O3是氧化剂,C是还原剂 B. 每生成1 mol CO需转移2 mol电子
C. AlN中氮元素的化合价为+3 D. N2发生了氧化反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com