
【题目】乙酰紫草素具有抗菌、抗炎、抗病毒、抗肿瘤等作用,它的结构简式如图所示,下列有关乙酰紫草素的说法正确的是
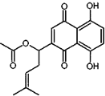
A. 该分子中含有1个手性碳原子
B. 1mol乙酰紫草素最多可与2mol NaOH反应
C. 1mol 乙酰紫草素最多可与2mol Br2反应
D. 能与FeCl3溶液发生显色反应
【答案】AD
【解析】本题主要是考查有机物结构和性质,A.该分子中只有连接酯基中-COO-的碳原子是手性碳原子,所以只有1个手性碳原子;B.能和氢氧化钠反应的有酚羟基、酯基水解生成的羧基,所以1mol乙酰紫草素最多可与3molNaOH反应;C.能和溴发生加成反应的有碳碳双键,苯环上酚羟基邻位氢原子能被溴取代,所以1mol 乙酰紫草素最多可与4molBr2反应;D.含有酚羟基,能发生显色反应。
A.该分子中只有连接酯基中-COO-的碳原子是手性碳原子,所以只有1个手性碳原子,A正确;
B.能和氢氧化钠反应的有酚羟基、酯基水解生成的羧基,所以1mol乙酰紫草素最多可与3molNaOH反应,B错误;
C.能和溴发生加成反应的有碳碳双键,苯环上酚羟基邻位氢原子能被溴取代,所以1mol 乙酰紫草素最多可与4molBr2反应,C错误;
D.含有酚羟基,能发生显色反应, D正确。
答案选AD。
点晴:该类试题的关键是明确有机物分子中含有的官能团,然后联系相应代表物质的结构和性质分析解答即可。本题侧重于考查酚、酯的性质,注意酯基水解生成的羧基能和NaOH反应,是答题的易错点。


科目:高中化学 来源: 题型:
【题目】室温下,将稀盐酸滴加到某0.01mol/L一元弱碱(BOH)溶液中,测得混合溶液的pOH与离子浓度的变化关系如图所示。下列叙述错误的是( )
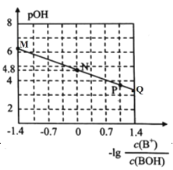
A.BOH的电离常数Kb的数量级为10-5
B.M点所示的溶液中:![]()
C.P点表示未加入稀盐酸的溶液
D.N点所示的溶液中:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以甲烷燃料电池为例来分析在不同的环境中电极反应的书写方法:
(1)碱性条件下燃料电池的负极反应:______________。
(2)碱性条件下燃料电池的正极反应:______________。
(3)固体电解质(高温下能传导O2-)环境中电池的负极反应:______________。
(4)固体电解质(高温下能传导O2-)环境中电池的正极反应:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
I.乳酸(![]() )、酒精、醋酸、淀粉等都是生活中常见的物质。
)、酒精、醋酸、淀粉等都是生活中常见的物质。
(1)在生活中,常选择上述物质中_______________(填结构简式)清洗水壶里的水垢。
(2)生活中常选择_______________酒精![]() 选择“75%”“95%”或“无水”
选择“75%”“95%”或“无水”![]() 皮肤消毒。
皮肤消毒。
(3)上述物质中,属于天然高分子化合物的是_________________![]() 填名称
填名称![]() 。
。
(4)乳酸中发生如下变化:![]() ,则所用的试剂a为________(写化学式)。
,则所用的试剂a为________(写化学式)。
II.X、Y、Z、W是元素周期表前四周期中的常见元素,其相关信息如下表:
元素 | 相关信息 |
X | X的最外层电子数是次外层的2倍 |
Y | M层上的电子数是K层的3倍 |
Z | Z的一种核素的质量数为53,中子数为34 |
W | W2+与氖原子具有相同核外电子排布 |
(5)X在元素周期表中的位置为___________;Y元素的名称为________________。
(6)元素W的离子结构示意图是_______________;Z、Y形成的化合物为____________(用化学式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硒(Se)和铜(Cu)在生产生活中有广泛的应用。硒可以用作光敏材料、电解锰行业的催化剂,也是动物体必需的营养元素和对植物有益的营养元素等。氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下所示:
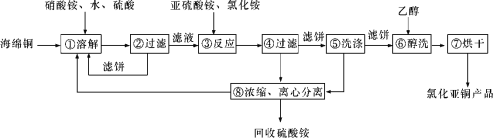
请回答下列问题:
(1)若步骤①中得到的氧化产物只有一种,则它的化学式是____________。
(2)写出步骤③中主要反应的离子方程式:____________________________________。
(3)步骤⑤包括用pH=2的溶液酸洗、水洗两步操作,酸洗采用的酸是__________(写酸的名称)。
(4)上述工艺中,步骤⑥和⑦的作用是_____________。
(5)Se为ⅥA族元素,用乙二胺四乙酸铜阴离子水溶液和硒代硫酸钠(Na2SeSO3)溶液反应可获得纳米硒化铜,硒代硫酸钠还可用于Se的精制,写出硒代硫酸钠(Na2SeSO3)与H2SO4溶液反应得到精硒的化学方程式:_____。
(6)氯化亚铜产率与温度、溶液pH关系如下图所示。据图分析,流程化生产氯化亚铜的过程中,温度过低影响CuCl产率的原因是____________________________________;温度过高、pH过大也会影响CuCl产率的原因是_______________________________。
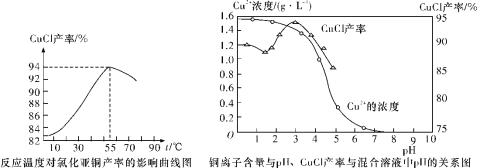
(7)用NaHS作污水处理的沉淀剂,可以处理工业废水中的Cu2+。已知:25℃时,H2S的电离平衡常数Ka1=1.0×10-7,Ka2=7.0×10-15,CuS的溶度积为Ksp(CuS)=6.3×10-36。反应Cu2+(aq)+HS-(aq) ![]() CuS(s)+H+(aq)的平衡常数K=__________(结果保留1位小数)。
CuS(s)+H+(aq)的平衡常数K=__________(结果保留1位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
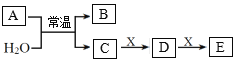
【题目】A、B是短周期元素m、n组成的常见二元化合物(原子序数m<n),常温下均为气体。X是一种能被磁铁吸引的金属单质,C、D、E为化合物。上述物质的转化关系如图所示。下列说法错误的是( )
A.元素的非金属性m<n
B.常温下,C的浓溶液能溶解X
C.B可通过化合反应生成A
D.D→E的离子方程式为: 2X3+ + X=3X2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等。下列判断不正确的是( )

A. 最简单气态氢化物的热稳定性:R>Q
B. 最高价氧化物对应水化物的酸性:Q<W
C. 原子半径:T>Q>R
D. T的最高价氧化物对应的水化物不能和强碱反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com