
【题目】室温下,将稀盐酸滴加到某0.01mol/L一元弱碱(BOH)溶液中,测得混合溶液的pOH与离子浓度的变化关系如图所示。下列叙述错误的是( )
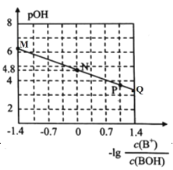
A.BOH的电离常数Kb的数量级为10-5
B.M点所示的溶液中:![]()
C.P点表示未加入稀盐酸的溶液
D.N点所示的溶液中:![]()
【答案】C
【解析】
A.一元弱碱(BOH)溶液中,BOHB++OH-,则电离常数Kb=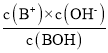 ,可得-lg
,可得-lg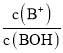 =-lg
=-lg![]() =- lgKb+ lgc(OH-)=-lgKb-pOH,代入N点数据,0=- lgKb-4.8,Kb=10-4.8,则Kb数量级为10-5,故A正确;
=- lgKb+ lgc(OH-)=-lgKb-pOH,代入N点数据,0=- lgKb-4.8,Kb=10-4.8,则Kb数量级为10-5,故A正确;
B.常温下,M点所示的溶液中存在电荷守恒:c(Cl-)+c(OH-)=c(H+)+c(B+),且pOH=6,则pH=14- pOH =8,溶液显碱性,c(OH-)>c(H+),则c(Cl-)<c(B+),故B正确;
C.根据图示,结合A项分析,P点,-lg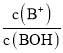 =-lgKb-pOH=1.05,则pOH=-lgKb+1.05=4.8-1.05=3.75,与图示不符,则P点不表示未加入稀盐酸的溶液,故C错误;
=-lgKb-pOH=1.05,则pOH=-lgKb+1.05=4.8-1.05=3.75,与图示不符,则P点不表示未加入稀盐酸的溶液,故C错误;
D.N点-lg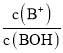 =0,则c(B+)= c(BOH),根据电荷守恒:c(Cl-)+c(OH-)=c(H+)+c(B+),则可变为:c(Cl-)+c(OH-)=c(H+)+ c(BOH),故D正确;
=0,则c(B+)= c(BOH),根据电荷守恒:c(Cl-)+c(OH-)=c(H+)+c(B+),则可变为:c(Cl-)+c(OH-)=c(H+)+ c(BOH),故D正确;
答案选C。


科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)某烷烃A,其蒸气密度是相同状况下氢气密度的64倍,经测定得知A分子中共含有6个甲基。
①若A不是烯烃与氢气加成的产物,则A的名称为:______;
②若A是炔烃与氢气加成的产物,则A的结构简式为:____。
(2)某烃B 0.1 mol 在氧气中充分燃烧后,可以生成7.2gH2O。试回答下列问题:
①若烃B不能使溴水褪色,但在一定条件下能与氯气发生取代反应,其一氯取代物有两种,则烃B的结构简式为_____。
②若烃B不能使溴水褪色,但能使酸性高锰酸钾溶液褪色,则烃B的可能的结构简式为_______
③若烃B能使溴水褪色,在催化剂作用下,与H2加成,其加成产物经测定分子中含有3个甲基,则烃B可能的结构简式_____。
(3)某烃C的相对分子质量为84。回答下列问题:
①下列物质与C以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不相等的是(填序号)___。
a.C7H12O2 b.C6H14 c.C6H14O d.C7H14O3
②若烃C为链烃,与HBr加成后只能得到一种产物,且该烃的一氯代物只有一种。C的结构简式为________;名称是_____;在一定条件下能发生加聚反应,写出该反应的化学方程式_____ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下事实不能用元素周期律解释的是( )
A.向![]() 溶液中通入氧气后生成浅黄色沉淀
溶液中通入氧气后生成浅黄色沉淀
B.氯与钠形成离子键,氯与硅形成共价键
C.工业生产硅单质原理: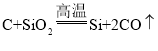
D.Na与冷水反应剧烈,Mg与冷水反应缓慢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向![]() 溶液中加入适量
溶液中加入适量![]() 溶液,不同时刻测得生成
溶液,不同时刻测得生成![]() 的体积(已折算为标准状况)如下表所示。资料显示,反应分两步进行:①
的体积(已折算为标准状况)如下表所示。资料显示,反应分两步进行:①![]() ,②
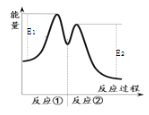
,②![]() ,反应过程中能量变化如下图所示。下列说法正确的是( )
,反应过程中能量变化如下图所示。下列说法正确的是( )
t/min | 0 | 3 | 6 | 10 |
V(O2)/mL | 0 | 9.9 | 17.2 | 22.4 |
A.![]() 是该反应过程的催化剂
是该反应过程的催化剂
B.0~10 min的平均反应速率:![]()
C.反应![]() 在无催化剂时的活化能为E1
在无催化剂时的活化能为E1
D.反应![]() 的
的![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学进行下列实验:
装置 | 操作 | 现象 |
| 将盛有浓硝酸的烧杯A放入盛有淀粉KI溶液的烧杯C中,然后将铜片放入烧杯A后,立即用烧杯B罩住。 | 烧杯A液体上方立即出现大量红棕色气体;一段时间后,红棕色气体消失,烧杯A和C中的液体都变成蓝色。 |
下列说法不合理的是
A.烧杯A中发生反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
B.红棕色气体消失可能与NO2和烧杯C中的KI发生反应有关
C.烧杯A中溶液变蓝是因为产生了Cu(NO3)2
D.若将铜片换成铁片,则C中的液体不会变蓝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种短周期元素,它们的原子序数依次增大。已知A和B原子具有相同的电子层数,且A元素的最高正价与最低负价和为零,C是同周期中原子半径最大的元素,D是同周期中离子半径最小的元素。C的单质在加热条件下与B的单质充分反应,可以得到与E单质颜色相同的淡黄色固态化合物F。试根据以上叙述回答:
(1)D元素在周期表中位置为_____________________;
(2)画出E的离子结构示意图_____________;写出ABE分子的结构式____________;
(3)工业上常用在微波条件下用A单质与EB2反应来解决其产生的环境问题,写出该化学方程式:___________________________________________;
(4)用电子式表示C2E的形成过程__________________________________________;
(5)1 mol F与A元素的最高价氧化物反应时转移的电子数为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Q是合成防晒霜的主要成分,某同学以石油化工的基本产品为主要原料,设计合成Q的流程如下(部分反应条件和试剂未注明):
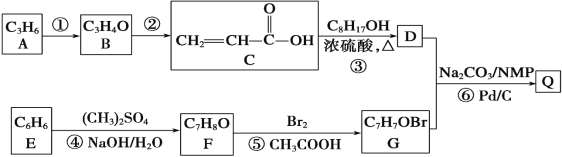
已知:Ⅰ.钯催化的交叉偶联反应原理(R、R1为烃基或其他基团,X为卤素原子):Pd/CR—X+R1—CH=CH2![]() R1—CH=CH—R+H—X
R1—CH=CH—R+H—X
II.C8H17OH 分子中只有一个支链,且为乙基,其连续氧化的产物能与碳酸氢钠反应生成CO2,其消去产物的分子只有一个碳原子上没有氢原子。
III.F不能与氢氧化钠溶液反应,G的核磁共振氢谱中有 3 个峰且为对位取代物。请回答下列问题:
(1)G的结构简式为__________。
(2)C8H17OH 的名称(用系统命名法命名)为____________。
(3)X是 F的同分异构体,X遇氯化铁溶液发生显色反应且环上的一溴取代物有两种,写出 X 的结构简式:___________。
(4)写出反应⑥的化学方程式:____________。
(5)下列有关 B、C的说法正确的是____________(填序号)。
a.二者都能使溴的四氯化碳溶液或酸性高锰酸钾溶液褪色
b.二者都能与碳酸氢钠溶液反应产生二氧化碳
c.1molB或C都能最多消耗44.8L(标准状况)氢气
d.二者都能与新制氢氧化铜悬浊液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于如图所示的原电池,下列说法正确的是
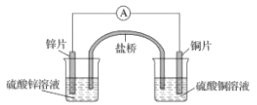
A.电子从锌电极通过电流表流向铜电极
B.盐桥中的阴离子向硫酸铜溶液中迁移
C.取出盐桥后,电流表仍会偏转,铜电极在反应前后质量不变
D.锌电极发生氧化反应;铜电极发生还原反应,其电极反应是2H++2e-=H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酰紫草素具有抗菌、抗炎、抗病毒、抗肿瘤等作用,它的结构简式如图所示,下列有关乙酰紫草素的说法正确的是
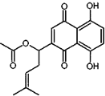
A. 该分子中含有1个手性碳原子
B. 1mol乙酰紫草素最多可与2mol NaOH反应
C. 1mol 乙酰紫草素最多可与2mol Br2反应
D. 能与FeCl3溶液发生显色反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com