
【题目】以下事实不能用元素周期律解释的是( )
A.向![]() 溶液中通入氧气后生成浅黄色沉淀
溶液中通入氧气后生成浅黄色沉淀
B.氯与钠形成离子键,氯与硅形成共价键
C.工业生产硅单质原理: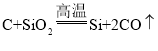
D.Na与冷水反应剧烈,Mg与冷水反应缓慢
【答案】C
【解析】
A.向![]() 溶液中通入氧气后生成浅黄色硫沉淀,反应中O2是氧化剂,S是氧化产物,氧化性:O2>S,O、S位于同主族,从上到下,非金属性减弱,非金属性越强,对应单质的氧化性越强,故A可以用元素周期律解释;
溶液中通入氧气后生成浅黄色硫沉淀,反应中O2是氧化剂,S是氧化产物,氧化性:O2>S,O、S位于同主族,从上到下,非金属性减弱,非金属性越强,对应单质的氧化性越强,故A可以用元素周期律解释;
B.Na、Si位于同周期,从左向右金属性减弱、非金属性增强,Na易失去电子,则氯与钠形成离子键,Si不易失去电子,氯与硅形成共价键,故B可用元素周期律解释;
C.C、Si位于同主族,从上到下,非金属性减弱,对应单质的氧化性逐渐减弱,工业生产硅单质原理: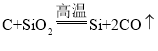 反应中C是还原剂,Si是还原产物,还原性C>Si,不能比较单质的氧化性强弱,故C不能用元素周期律解释;
反应中C是还原剂,Si是还原产物,还原性C>Si,不能比较单质的氧化性强弱,故C不能用元素周期律解释;
D.Na、Mg位于同周期,从左向右金属性减弱、非金属性增强,金属性:Na>Mg,元素金属性越强,对应单质与水反应越剧烈,故D能用元素周期律解释;
答案选C。


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】用如图所示的装置进行实验,仪器![]() 、
、![]() 、
、![]() 中分别盛有试剂1、2、3,其中能达到实验目的是( )
中分别盛有试剂1、2、3,其中能达到实验目的是( )
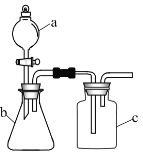
选项 | 试剂1 | 试剂2 | 试剂3 | 实验目的 |
A | 浓盐酸 |
| 饱和食盐水 | 制备 |
B | 浓硫酸 | 乙醇 | 溴水 | 验证乙烯能使溴水褪色 |
C | 盐酸 |
| 品红试液 | 证明 |
D | 稀硫酸 | 溶液 | 澄清石灰水 | 验证 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近期我国学者研制出低成本的电解“水制氢”催化剂——镍掺杂的磷化钴三元纳米片电催化剂(![]() )。回答下列问题:
)。回答下列问题:
(1)Co在元素周期表中的位置为_________,Co2+价层电子排布式为______________。
(2)Co、Ni可形成![]() 、
、![]() 、
、![]() 等多种配合物。
等多种配合物。
①![]() 的空间构型为__________,
的空间构型为__________,![]() 中N原子的杂化轨道类型为_________。
中N原子的杂化轨道类型为_________。
②C、N、O、S四种元素中,第一电离能最大的是_____________。
③![]() 中含有σ键的数目为__________;已知NF3比NH3的沸点小得多,试解释原因________________________________________。
中含有σ键的数目为__________;已知NF3比NH3的沸点小得多,试解释原因________________________________________。
(3)常用丁二酮肟来检验Ni2+,反应如下:
Ni2+(aq)+2 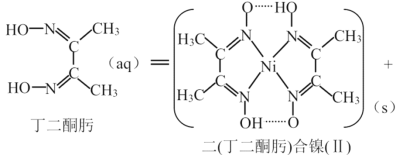 2H+(aq)
2H+(aq)
①1个二(丁二酮肟)合镍(Ⅱ)中含有_________________个配位键。
②上述反应的适宜![]() 为_________________(填字母序号)
为_________________(填字母序号)
A.12 B.5~10 C.1
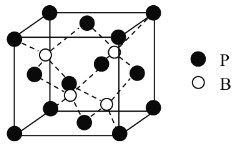
(4)磷化硼是一种备受关注的耐磨涂料,其晶体中磷原子作面心立方最密堆积,硼原子填入四面体空隙中(如图)。已知磷化硼晶体密度为![]() ,计算晶体中硼原子和磷原子的最近核间距为___________
,计算晶体中硼原子和磷原子的最近核间距为___________![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯氧磷(POCl3)是一种工业化工原料,可用于制取有机磷农药、长效磺胺药物等,还可用作染料中间体、有机合成的氯化剂和催化剂、阻燃剂等。利用O2和PCl3为原料可制备三氯氧磷,其制备装置如图所示(夹持装置略去):
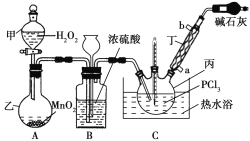
已知PCl3和三氯氧磷的性质如表:
熔点/℃ | 沸点/℃ | 其他物理或化学性质 | |
PCl3 | -112.0 | 76.0 | PCl3和POCl3互溶,均为无色液体,遇水均剧烈水解,发生复分解反应生成磷的含氧酸和HCl |
POCl3 | 1.25 | 106.0 |
(1)装置A中的分液漏斗能否用长颈漏斗代替?做出判断并分析原因:_______
(2)装置B的作用是______________(填标号)。
a.气体除杂 b.加注浓硫酸 c.观察气体流出速度 d.调节气压
(3)仪器丙的名称是___________,实验过程中仪器丁的进水口为__________(填“a”或“b”)口。
(4)写出装置C中发生反应的化学方程式_______,该装置中用温度计控制温度为60~65 ℃,原因是________。
(5)称取16.73 g POCl3样品,配制成100 mL溶液;取10.00 mL溶液于锥形瓶中,加入3.2 mol·L-1的AgNO3溶液10.00 mL,并往锥形瓶中滴入5滴Fe2(SO4)3溶液;用0.20 mol·L-1的KSCN溶液滴定,达到滴定终点时消耗KSCN溶液10.00 mL(已知:Ag++SCN-=AgSCN↓)。则加入Fe2(SO4)3溶液的作用是________,样品中POCl3的纯度为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为检验一种氮肥的成分,某学习小组的同学进行了以下实验:①加热氮肥样品生成两种气体,其中一种气体能使湿润的红色石蕊试纸变蓝,另一种气体能使澄清石灰水变浑浊。②取少量该氮肥样品溶于水,并加入少量BaCl2溶液,没有明显变化。由此可知该氮肥的主要成分是( )
A.NH4NO3B.(NH4)2CO3C.NH4ClD.NH4HCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为检验淀粉水解的情况,进行如下图所示的实验,试管甲和丙均用60~80℃的水浴加热5~6 min,试管乙不加热。待试管甲中的溶液冷却后再进行后续实验。

实验1:取少量甲中溶液,加入新制氢氧化铜,加热,没有砖红色沉淀出现。
实验2:取少量乙中溶液,滴加几滴碘水,溶液变为蓝色,但取少量甲中溶液做此实验时,溶液不变蓝色。
实验3:取少量丙中溶液加入NaOH溶液调节至碱性,再滴加碘水,溶液颜色无明显变化。
(1)写出淀粉水解的化学方程式: 。
(2)设计甲和乙是为了探究 对淀粉水解的影响,设计甲和丙是为了探究 对淀粉水解的影响。
(3)实验1失败的原因是 。
(4)实验3中溶液的颜色无明显变化的原因是 。
(5)下列结论合理的是 (填字母)。
a.淀粉水解需要在催化剂和一定温度下进行
b.欲检验淀粉是否完全水解,最好在冷却后的水解液中直接加碘
c.欲检验淀粉的水解产物具有还原性,应先在水解液中加入氢氧化钠中和稀硫酸至溶液呈碱性,再加入新制氢氧化铜并加热
d.若用唾液代替稀硫酸,则实验1可能出现预期的现象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期金属元素甲~戊在元素周期表中的相对位置如右表所示,下面判断正确的是
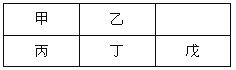
A. 原子半径:丙<丁<戊B. 金属性:甲>丙
C. 氢氧化物碱性:丙>丁>戊D. 最外层电子数:甲>乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将稀盐酸滴加到某0.01mol/L一元弱碱(BOH)溶液中,测得混合溶液的pOH与离子浓度的变化关系如图所示。下列叙述错误的是( )
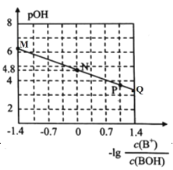
A.BOH的电离常数Kb的数量级为10-5
B.M点所示的溶液中:![]()
C.P点表示未加入稀盐酸的溶液
D.N点所示的溶液中:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以甲烷燃料电池为例来分析在不同的环境中电极反应的书写方法:
(1)碱性条件下燃料电池的负极反应:______________。
(2)碱性条件下燃料电池的正极反应:______________。
(3)固体电解质(高温下能传导O2-)环境中电池的负极反应:______________。
(4)固体电解质(高温下能传导O2-)环境中电池的正极反应:______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com