
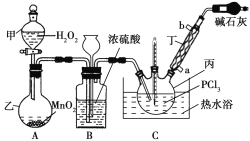
【题目】三氯氧磷(POCl3)是一种工业化工原料,可用于制取有机磷农药、长效磺胺药物等,还可用作染料中间体、有机合成的氯化剂和催化剂、阻燃剂等。利用O2和PCl3为原料可制备三氯氧磷,其制备装置如图所示(夹持装置略去):
已知PCl3和三氯氧磷的性质如表:
熔点/℃ | 沸点/℃ | 其他物理或化学性质 | |
PCl3 | -112.0 | 76.0 | PCl3和POCl3互溶,均为无色液体,遇水均剧烈水解,发生复分解反应生成磷的含氧酸和HCl |
POCl3 | 1.25 | 106.0 |
(1)装置A中的分液漏斗能否用长颈漏斗代替?做出判断并分析原因:_______
(2)装置B的作用是______________(填标号)。
a.气体除杂 b.加注浓硫酸 c.观察气体流出速度 d.调节气压
(3)仪器丙的名称是___________,实验过程中仪器丁的进水口为__________(填“a”或“b”)口。
(4)写出装置C中发生反应的化学方程式_______,该装置中用温度计控制温度为60~65 ℃,原因是________。
(5)称取16.73 g POCl3样品,配制成100 mL溶液;取10.00 mL溶液于锥形瓶中,加入3.2 mol·L-1的AgNO3溶液10.00 mL,并往锥形瓶中滴入5滴Fe2(SO4)3溶液;用0.20 mol·L-1的KSCN溶液滴定,达到滴定终点时消耗KSCN溶液10.00 mL(已知:Ag++SCN-=AgSCN↓)。则加入Fe2(SO4)3溶液的作用是________,样品中POCl3的纯度为_____________。
【答案】否,长颈漏斗不能调节滴液速度 acd 三颈烧瓶 a 2PCl3+O2=2POCl3 温度过低反应速度过慢;温度过高,PCl3易挥发,利用率低 指示剂 91.8%
【解析】
A装置中用双氧水与二氧化锰反应制备氧气,通过加入双氧水的量,可以控制产生氧气的速率,氧气中含有的水蒸气用浓硫酸除去,装置B中有长颈漏斗,可以平衡装置内外的压强,起到安全瓶的作用,纯净的氧气与三氯化磷在装置C中反应生成POCl3,为了控制反应速率,同时防止三氯化磷挥发,反应的温度控制在60~65℃,所以装置C中用水浴加热,POCl3遇水剧烈水解为含氧酸和氯化氢,为防止空气中水蒸汽进入装置,同时吸收尾气,所以在装置的最后连有碱石灰的干燥管,据此分析解答(1)~(4);
(5)测定POCl3产品含量,用POCl3与水反应生成氯化氢,然后用硝酸银标准溶液沉淀溶液中的氯离子,KSCN溶液滴定过量的AgNO3溶液,根据KSCN的物质的量可计算出溶液中剩余的AgNO3,结合AgNO3的总物质的量得知与氯离子反应的硝酸银,进而计算出溶液中氯离子的物质的量,根据元素守恒可计算出样品中POCl3的质量,进而确定POCl3的质量分数。
(1)装置A中的分液漏斗不能用长颈漏斗代替,因为长颈漏斗不能调节滴液速度,故答案为:否,长颈漏斗不能调节滴液速度;
(2)装置B中装有浓硫酸,可作干燥剂,另外气体通过液体时可观察到气泡出现,长颈漏斗,可以平衡装置内外的压强,起到安全瓶的作用,则装置B的作用是观察O2的流速、平衡气压、干燥氧气,故答案为:acd;
(3)根据装置图,仪器丙为三颈烧瓶,为了提高冷却效果,应该从冷凝管的下口进水,即进水口为a,故答案为:三颈烧瓶;a;
(4)氧气氧化PCl3生成POCl3,根据原子守恒,反应的化学方程式2PCl3+O2=2POCl3,根据上面的分析可知,反应温度应控制在60~65℃,原因是温度过低,反应速率小,温度过高,三氯化磷会挥发,利用率低,故答案为:2PCl3+O2=2POCl3;温度过低,反应速率小,温度过高,三氯化磷会挥发,利用率低;
(5)Fe3+的溶液中滴加KSCN溶液,溶液显红色,则用KSCN溶液滴定过量的AgNO3溶液时,可选择硫酸铁溶液为指示剂,达到终点时的现象是溶液会变红色;KSCN的物质的量为0.20molL-1×0.010L=0.002mol,根据反应Ag++SCN-=AgSCN↓,可知溶液中剩余的银离子的物质的量为0.002mol,POCl3与水反应生成氯化氢的物质的量为3.2molL-1×0.01L-0.002mol=0.03mol,即16.73 g POCl3产品中POCl3的物质的量为![]() ×
×![]() =0.1mol,则所得产品中POCl3的纯度为
=0.1mol,则所得产品中POCl3的纯度为![]() ×100%=91.8%,故答案为:指示剂;91.8%。
×100%=91.8%,故答案为:指示剂;91.8%。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】碳族元素的单质和化合物在化工、医药、材料等领域有着广泛的应用。
(1)锗是重要半导体材料,基态Ge原子中,核外电子占据最高能级的符号是______,该能级的电子云轮廓图为________。Ge的晶胞结构与金刚石类似,质地硬而脆,沸点2830℃,锗晶体属于_______晶体。
(2)(CH3)3C+是有机合成重要中间体,该中间体中碳原子杂化方式为_______,(CH3)3C+中碳骨架的几何构型为________。
(3)治疗铅中毒可滴注依地酸钠钙,使Pb2+转化为依地酸铅盐。下列说法正确的是_______。
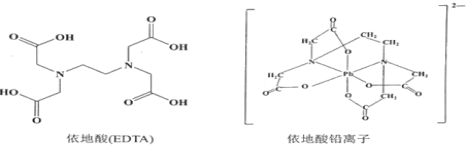
A.形成依地酸铅离子所需n(Pb2+)∶n(EDTA)=1∶4
B.依地酸中各元素的电负性从大到小的顺序为O>N>C>H
C.依地酸铅盐中含有离子键和配位键
D.依地酸具有良好的水溶性是由于其分子间能形成氢键
(4)下表列出了碱土金属碳酸盐的热分解温度和阳离子半径:
碳酸盐 | MgCO3 | CaCO3 | SrCO3 | BaCO3 |
热分解温度/℃ | 402 | 900 | 1172 | 1360 |
阳离子半径/pm | 66 | 99 | 112 | 135 |
碱土金属碳酸盐同主族由上到下的热分解温度逐渐升高,原因是:__________。
(5)有机卤化铅晶体具有独特的光电性能,下图为其晶胞结构示意图:
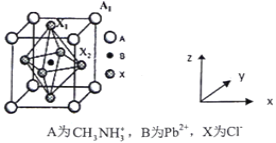
①若该晶胞的边长为anm,则Cl-间的最短距离是________。
②在该晶胞的另一种表达方式中,若图中Pb2+处于顶点位置,则Cl-处于____位置。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化工生产与人类进步紧密相联。下列有关说法不正确的是
A. 空气吹出法提取海水中溴通常使用SO2作还原剂
B. 侯氏制碱法工艺流程中利用了物质溶解度的差异
C. 合成氨采用高温、高压和催化剂主要是提高氢气平衡转化率
D. 工业用乙烯直接氧化法制环氧乙烷体现绿色化学和原子经济
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由甲酸甲酯、葡萄糖、乙醛、丙酸四种物质组成的混合物,已知其中氧元素的质量分数为44%,则氢元素的质量分数为( )
A. 48%B. 8%C. 56%D. 10%
查看答案和解析>>
科目:高中化学 来源: 题型:
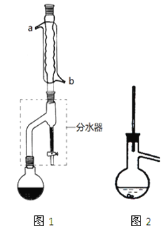
【题目】有机物的反应往往伴随副反应发生,因此需要分离提纯。有一种水果香精的合成步骤如下:
Ⅰ合成:
在干燥的圆底烧瓶中加11.5mL(9.3g,0.125mol)正丁醇、7.2mL(7.5g,0.125mol)冰醋酸(乙酸)和3~4滴浓H2SO4,摇匀后,加几粒沸石,再按图1所示装置安装好。在分水器中预先加入5.00mL水,其水面低于分水器回流支管下沿3~5mm,然后用小火加热,反应大约40min。
Ⅱ分离提纯:
①当分水器中的液面不再升高时,冷却,放出分水器中的水,把反应后的溶液与分水器中的酯层合并,转入分液漏斗中,用10mL10%碳酸钠溶液洗至酯层无酸性(pH=7),充分振荡后静置,分去水层。
②将酯层倒入小锥形瓶中,加少量无水硫酸镁干燥(生成MgSO47H2O晶体)
③将乙酸正丁酯粗产品转入50mL蒸馏烧瓶中,加几粒沸石进行常压蒸馏,收集产品,主要试剂及产物的物理常数如下:
化合物 | 正丁醇 | 冰醋酸 | 乙酸正丁酯 | 正丁醚 |
密度/(g/mL) | 0.810 | 1.049 | 0.882 | 0.7689 |
沸点/℃ | 117.8 | 118.1 | 126.1 | 143 |
在水中的溶解性 | 易溶 | 易溶 | 难溶 | 难溶 |
制备过程中还可能与的副反应有2CH3CH2CH2CH2OH![]() CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
根据以上信息回答下列问题:
(1)写出合成乙酸正丁酯的化学方程式____________。
(2)如图1整个装置可看作由分水器、圆底烧瓶和冷凝管组成,其中冷水应从______(填a或b)管口通入。
(3)步骤①中碳酸钠溶液的作用主要是除去硫酸、_________、___________。
(4)在操作步骤②后(即酯层用无水硫酸镁干燥后),应先___________(填实验操作名称),然后将乙酸正丁酯粗产品转入蒸馏烧瓶中,如果蒸馏装置如图2所示,则收集到的产品中可能混有___________________杂质。
(5)步骤③的常压蒸馏,需控制一定的温度,你认为在_______中加热比较合适(请从下列选项中选择)。
A.水 B.甘油(沸点290℃) C.石蜡油(沸点200~300℃) D.沙子
(6)反应结束后,若放出的水为6.98mL(水的密度为1g/mL),则正丁醇的转化率约为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把图b的碎纸片补充到图a中,可得到一个完整的离子方程式。下列有关该离子方程式的说法正确的是( )

A.配平后的化学计量数依次为3、1、2、6、3
B.若有1molS被氧化,则生成2molS2-
C.氧化剂与还原剂的物质的量之比为1:2
D.3molS参加反应有8mol电子发生转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.1molO2与金属Na反应,O2一定得到4NA个电子
B.18gNH4+中所含的电子数为11NA
C.1molFe与足量的Cl2反应,转移的电子数为2NA
D.1molCl2与足量的Fe反应,转移的电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按要求完成下列各题。
(1)将2molL-1Al2(SO4)3和0.2molL-1H2SO4溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中c(SO42-)=___molL-1.若用容量瓶以质量分数为98%、密度为1.84g/cm3的浓硫酸,配制480mL浓度成0.2molL-1稀硫酸,计算需要量取___mL的浓硫酸。(读到小数点后一位)
(2)在标准状况下,由CO和CO2组成的混合气体6.72L,质量为12g。此混合物中CO和CO2分子数目之比是___,混合气体的平均摩尔质量是___。
(3)还原铁粉与高温水蒸气反应的化学方程式:___。
(4)除去Mg粉中的Al粉的试剂是___,反应的离子方程式为:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】保水剂是一种强吸水树脂,能在短时间内吸收自身重量几百倍至上千倍的水分。聚丙烯酸钠就是一种高吸水性树脂。下面是丙烯合成聚丙烯酸钠的化工流程:

(1)上述反应中属于加成反应的有____________,反应⑧的反应类型为____________;
(2)若(1)的反应条件为通过溴的四氯化碳溶液,请写出A的结构简式____________;D中官能团名称是____________。
(3)请写出C→D的化学反应方程式__________________。
(4)![]() 是
是![]() 的同系物,式量比
的同系物,式量比![]() 大14,写出2种符合下列要求的
大14,写出2种符合下列要求的![]() 的同分异构体:①链状分子;②与新制氢氧化铜在加热条件下反应生成砖红色沉淀;③与
的同分异构体:①链状分子;②与新制氢氧化铜在加热条件下反应生成砖红色沉淀;③与![]() 溶液混合后滴入酚酞,加热,溶液颜色变浅。__________、___________
溶液混合后滴入酚酞,加热,溶液颜色变浅。__________、___________
(5)检验反应(4)是否全部转化的实验方案__________________。
(6)丙酮(![]() )是一种常用的化工试剂,请设计一条由丙烯制备丙酮的合成路线。(合成路线常用的表示方式为:
)是一种常用的化工试剂,请设计一条由丙烯制备丙酮的合成路线。(合成路线常用的表示方式为:![]() )
)
____________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com