
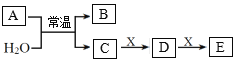
【题目】A、B是短周期元素m、n组成的常见二元化合物(原子序数m<n),常温下均为气体。X是一种能被磁铁吸引的金属单质,C、D、E为化合物。上述物质的转化关系如图所示。下列说法错误的是( )
A.元素的非金属性m<n
B.常温下,C的浓溶液能溶解X
C.B可通过化合反应生成A
D.D→E的离子方程式为: 2X3+ + X=3X2+
【答案】B
【解析】
X是一种能被磁铁吸引的金属单质,则X为Fe;A、B是短周期元素m、n组成的常见二元化合物(原子序数m<n),常温下均为气体,根据转化关系可知,A与水在常温下反应生成B和C,C能够与Fe反应生成D,D与Fe反应生成E,则A为NO2,B为NO,C为HNO3,D为硝酸铁,E为硝酸亚铁,结合原子序数大小可知,m为N,n为O元素,据此解答。
根据分析可知:A为NO2,B为NO,C为HNO3,D为硝酸铁,E为硝酸亚铁,m为N,n为O元素。
A. 同一周期从左向右非金属性逐渐增强,则非金属性m<n,故A正确;
B. 常温下浓硝酸与铁发生钝化现象,阻止了反应的继续进行,则无法溶解铁,故B错误;
C. NO与氧气发生化合反应生成二氧化氮,故C正确;
D. D→E为硝酸铁与Fe生成硝酸亚铁的反应,该反应的离子方程式为:2Fe3++Fe=3Fe2+,故D正确;
故答案选:B。


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源: 题型:
【题目】Q是合成防晒霜的主要成分,某同学以石油化工的基本产品为主要原料,设计合成Q的流程如下(部分反应条件和试剂未注明):
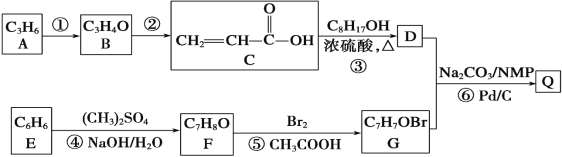
已知:Ⅰ.钯催化的交叉偶联反应原理(R、R1为烃基或其他基团,X为卤素原子):Pd/CR—X+R1—CH=CH2![]() R1—CH=CH—R+H—X
R1—CH=CH—R+H—X
II.C8H17OH 分子中只有一个支链,且为乙基,其连续氧化的产物能与碳酸氢钠反应生成CO2,其消去产物的分子只有一个碳原子上没有氢原子。
III.F不能与氢氧化钠溶液反应,G的核磁共振氢谱中有 3 个峰且为对位取代物。请回答下列问题:
(1)G的结构简式为__________。
(2)C8H17OH 的名称(用系统命名法命名)为____________。
(3)X是 F的同分异构体,X遇氯化铁溶液发生显色反应且环上的一溴取代物有两种,写出 X 的结构简式:___________。
(4)写出反应⑥的化学方程式:____________。
(5)下列有关 B、C的说法正确的是____________(填序号)。
a.二者都能使溴的四氯化碳溶液或酸性高锰酸钾溶液褪色
b.二者都能与碳酸氢钠溶液反应产生二氧化碳
c.1molB或C都能最多消耗44.8L(标准状况)氢气
d.二者都能与新制氢氧化铜悬浊液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是模拟“侯氏制碱法”制取NaHCO3的部分装置。下列操作正确的是( )
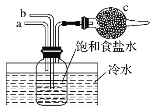
A.a通入NH3,然后b通入CO2,c中放碱石灰
B.b通入NH3,然后a通入CO2,c中放蘸稀硫酸的脱脂棉
C.a通入CO2,然后b通入NH3,c中放碱石灰
D.a通入NH3,然后b通入CO2,c中放蘸稀硫酸的脱脂棉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酰紫草素具有抗菌、抗炎、抗病毒、抗肿瘤等作用,它的结构简式如图所示,下列有关乙酰紫草素的说法正确的是
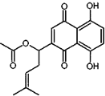
A. 该分子中含有1个手性碳原子
B. 1mol乙酰紫草素最多可与2mol NaOH反应
C. 1mol 乙酰紫草素最多可与2mol Br2反应
D. 能与FeCl3溶液发生显色反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两烧杯中各盛有100 mL 3 mol·L-1的盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后生成的气体的体积比为甲∶乙=1∶2,则加入铝粉的质量为( )
A.5.4 gB.3.6 gC.2.7 gD.1.8 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1mol·L-1MgSO4和0.05mol·L-1Al2(SO4)3溶液进行实验:①各取25mL,分别滴加0.5mol·L-1NaOH溶液,测得溶液pH与V(NaOH)的关系如图1;②将两种溶液等体积混合后,取出25mL,逐滴加入上述NaOH溶液,观察现象。下述正确的是 ( )
图1 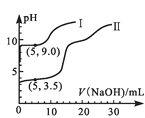 图2
图2
A.图1中的曲线II表示MgSO4与NaOH反应的关系
B.根据图1可得Ksp[Al(OH)3]的值大于1.0×10-32
C.实验②中Al(OH)3完全溶解前,溶液中c(Mg2+)/c(Al3+)逐渐变大
D.图2可以表示实验②中n(沉淀)与V(NaOH)的关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸盐与钻形成的一种配合物1Co(NH3)5N02]C12的制备流程如下:
CoC12·6H20![]() [Co(NH3)5C1]C12
[Co(NH3)5C1]C12![]() [Co(NH3)5NO2]C12
[Co(NH3)5NO2]C12
(1)Co2+基态核外电子排布式为_______________。
(2)配合物[Co(NH3)5C1]C12中与Co3+形成配位键的原子为___________(填元素符号);配离子[Co(NH3)5N02]2+的配体中氮原子的杂化轨道类型为___________。
(3)与NO2-互为等电子体的单质分子为___________(写化学式)。
(4)H202与H20可以任意比例互溶,除因为它们都是极性分子外,还因为 _______________。
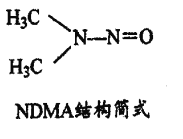
(5)亚硝酸盐在水体中可转化为强致癌物亚硝胺,亚硝胺NDMA的结构、简式如图所示,lmolNDMA分子中含有![]() 键的数目为______________mol.
键的数目为______________mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学要以“研究苯分子的结构”为题目做一次探究活动,下面是其活动记录,请你补全所缺内容。
(1)理论推测:他根据苯的凯库勒式________,推测苯分子中有两种不同的碳碳键,即________和________,因此它能使紫色的________溶液褪色。
(2)实验验证:他取少量的上述溶液加入试管中,然后加入苯,充分振荡,发现_____________________。
(3)实验结论:上述的理论推测是________(填“正确”或“错误”)的。
(4)查询资料:经查阅有关资料,发现苯分子中六个碳原子之间的键________(填“相同”或“不同”),是一种特殊的键,苯分子中的六个碳原子和六个氢原子________(填“在”或“不在”)同一个平面上,应该用________表示苯分子的结构更合理。
(5)发现问题:当他将苯加入溴水中时,充分振荡,发现能使溴水褪色,于是该同学认为所查资料有误。你同意他的结论吗?____。为什么?______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是用0.1000mol·L-1的NaOH溶液滴定20.00mL未知浓度盐酸(酚酞作指示剂)的滴定曲线,下列说法正确的是( )
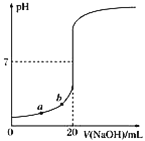
A.水电离出的氢离子浓度:a>b
B.盐酸的物质的量浓度为0.0100mol·L-1
C.指示剂变色时,说明盐酸与NaOH一定恰好完全反应
D.当滴加NaOH溶液10.00mL时,该混合液的pH=1+lg3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com