
【题目】ZrO2常用作陶瓷材料,可由锆英砂(主要成分为ZrSiO4,也可表示为ZrO2·SiO2,还含少量Fe2O3、Al2O3、SiO2等杂质)通过如下方法制取:

已知:①ZrO2能与烧碱反应生成可溶于水的Na2ZrO3,Na2ZrO3与酸反应生成ZrO2+。
②部分金属离子在实验条件下开始沉淀和完全沉淀的pH如下表。
金属离子 | Fe3+ | Al3+ | ZrO2+ |
开始沉淀时pH | 1.9 | 3.3 | 6.2 |
沉淀完全时pH | 3.2 | 5.2 | 8.0 |
(1)熔融时ZrSiO4发生反应的化学方程式为 ,滤渣I的化学式为 。
(2)为使滤液I的杂质离子沉淀完全,需用氨水调pH=a,则a的范围是 ;继续加氨水至pH=b时,所发生反应的离子方程式为 。
(3)向过滤III所得滤液中加入CaCO3粉末并加热,得到两种气体。该反应的离子方程式为 。
(4)为得到纯净的ZrO2,Zr(OH)4需要洗涤,检验Zr(OH)4是否洗涤干净的方法是 。
【答案】
(1)ZrSiO4+4NaOH![]() Na2SiO3+Na2ZrO3+2H2O;H2SiO3(或H4SiO4);
Na2SiO3+Na2ZrO3+2H2O;H2SiO3(或H4SiO4);
(2)5.2~6.2;ZrO2++2NH3·H2O+H2O= Zr(OH)4↓+2NH4+ ;
(3)2NH4++CaCO3![]() Ca2++2NH3↑+CO2↑+H2O;
Ca2++2NH3↑+CO2↑+H2O;
(4)取最后一次洗涤液,向其中滴加稀硝酸,再滴加硝酸银溶液,若无沉淀生成,则Zr(OH)4洗涤干净。
【解析】
试题分析:锆英砂(主要成分为ZrSiO4,也可表示为ZrO2SiO2,还含少量Fe2O3、Al2O3、SiO2等杂质)加NaOH熔融,ZrSiO4转化为Na2SiO3和Na2ZrO3,加过量盐酸酸浸,Na2SiO3与HCl生成硅酸沉淀,滤液中含有ZrO2+、Fe3+、Al3+,加氨水调节pH为5.2~6.2,使Fe3+、Al3+转化为氢氧化物沉淀,过滤,滤液中主要含有ZrO2+,再加氨水调节pH使ZrO2+转化为Zr(OH)4沉淀,过滤、洗涤,得到Zr(OH)4,加热分解,即可得到ZrO2;
(1)高温下,ZrSiO4与NaOH反应生成Na2SiO3和Na2ZrO3,其反应的方程式为:ZrSiO4+4NaOH ![]() Na2SiO3+Na2ZrO3+2H2O;加过量盐酸酸浸,Na2SiO3与HCl生成硅酸沉淀,过滤,滤渣为H2SiO3;故答案为:ZrSiO4+4NaOH
Na2SiO3+Na2ZrO3+2H2O;加过量盐酸酸浸,Na2SiO3与HCl生成硅酸沉淀,过滤,滤渣为H2SiO3;故答案为:ZrSiO4+4NaOH ![]() Na2SiO3+Na2ZrO3+2H2O;H2SiO3;
Na2SiO3+Na2ZrO3+2H2O;H2SiO3;
(2)需用氨水调pH=a,使Fe3+、Al3+转化为氢氧化物沉淀,而ZrO2+不能沉淀,根据表中数据可知:pH在5.2~6.2时Fe3+、Al3+完全沉淀,而ZrO2+不沉淀;加氨水至pH=b时,ZrO2+与NH3H2O反应生成Zr(OH)4沉淀,其反应的离子方程式为:ZrO2++2NH3H2O+H2O=Zr(OH)4↓+2NH4+;故答案为:5.2~6.2;ZrO2++2NH3H2O+H2O=Zr(OH)4↓+2NH4+;
(3)过滤Ⅲ所得滤液中主要含有铵根离子,溶液显酸性,加入CaCO3粉末并加热得到氨气和二氧化碳,其反应的离子方程式为:2NH4++CaCO3![]() Ca2++2NH3↑+CO2↑+H2O;故答案为:2NH4++CaCO3
Ca2++2NH3↑+CO2↑+H2O;故答案为:2NH4++CaCO3![]() Ca2++2NH3↑+CO2↑+H2O;
Ca2++2NH3↑+CO2↑+H2O;
(4)沉淀上附着的杂质为氯离子,用稀硝酸和硝酸银来检验洗液中是否含有氯离子即可,其操作为:取最后一次洗涤液,向其中滴加稀硝酸,再滴加硝酸银溶液,若无沉淀生成,则Zr(OH)4洗涤干净;故答案为:取最后一次洗涤液,向其中滴加稀硝酸,再滴加硝酸银溶液,若无沉淀生成,则Zr(OH)4洗涤干净。


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
【题目】有关组成生物体细胞元素的叙述,正确的是( )
A. 在不同生物体的细胞内,化学元素的种类完全相同
B. 组成细胞最基本元素是O
C. 在同一生物体的不同细胞内,各种化学元素的含量相同
D. 组成生物体细胞的化学元素,在无机自然界中都能找到
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将面团包在纱布中并放在清水中搓洗,检测黏留在纱布上的黏稠物质和洗出的白浆物质所用的试剂分别是
A. 碘液、苏丹Ⅲ染液 B. 碘液、斐林试剂
C. 双缩脲试剂、捵液 D. 双缩脲试剂、斐林试剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据以下三个热化学方程式:
2H2S(g)+3O2(g)==2SO2(g)+2H2O(l) ΔH=-Q1 kJ/mol
2H2S(g)+O2(g)==2S(s)+2H2O(l) ΔH=-Q2 kJ/mol;
2H2S(g)+O2(g)==2S(s)+2H2O(g) ΔH=-Q3 kJ/mol。
判断Q1、Q2、Q3三者关系正确的是:( )
A. Q1>Q2>Q3 B. Q1>Q3>Q2 C. Q3>Q2>Q1 D. Q2>Q1>Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(g)+3B(g)2C(g)+D(g),达到平衡时,下列说法正确的是( )
A.A、B全部变成了C和D
B.B的正反应速率和逆反应速率相等
C.反应已经停止
D.A、B、C、D四种物质的浓度一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用含碳化合物合成新燃料是发展低碳经济的重要方法,已知CO(g)+2H2(g) ![]() CH3OH(g)过程能量情况如下图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是
CH3OH(g)过程能量情况如下图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是

A.该反应的ΔH=+91 kJ·mol-1
B.加入催化剂,该反应的ΔH变小
C.反应物的总能量大于生成物的总能量
D.如果该反应生成液态CH3OH,则ΔH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验的叙述正确的是( )
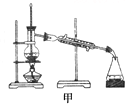

A.闻未知液体气味时,应该将试剂瓶口距离口鼻远一些,用手轻轻扇动
B.将碘单质从碘的CCl4溶液中分离出来可用如图甲所示实验装置
C.用容量瓶配制好一定浓度的某溶液后,塞紧瓶塞并在容量瓶上贴上标签
D.配制500 mL 0.4 mol·L-1NaCl溶液,必要的仪器如图乙所示
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
A.无色透明的溶液中:K+、Cu2+、NO![]() 、Cl-
、Cl-
B.0.1 mol·L-1CaCl2溶液中:Mg2+、NH![]() 、CO
、CO![]() 、SO
、SO![]()
C.pH=12的溶液:Na+、K+、SiO![]() 、Cl-
、Cl-
D.使甲基橙变红的溶液中:Na+、Fe2+、NO![]() 、Cl-
、Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com