
【题目】如图为向25 mL 0.1 mol·L-1NaOH溶液中逐滴滴加0.2 mol·L-1CH3COOH溶液过程中溶液pH的变化曲线。请回答:
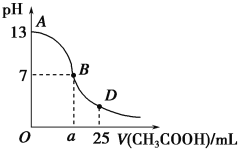
(1)B点溶液呈中性,有人据此认为,在B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确?______(填“是”或“否”)。若不正确,则二者恰好完全反应的点是在AB区间还是BD区间内?______区间(若正确,此问不答)。
(2)关于该滴定实验,从下列选项中选出最恰当的一项________(填字母)。
锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 | 选用滴定管 | |
A | 碱 | 酸 | 酚酞 | (乙) |
B | 酸 | 碱 | 甲基橙 | (甲) |
C | 碱 | 酸 | 酚酞 | (甲) |
D | 酸 | 碱 | 酚酞 | (乙) |

(3)AB区间,c(OH-)>c(H+),则c(OH-)与c(CH3COO-)大小关系是________。
A.c(OH-)大于c(CH3COO-)
B.c(OH-)小于c(CH3COO-)
C.c(OH-)等于c(CH3COO-)
D.上述三种情况都可以
(4)在D点时,溶液中c(CH3COO-)+c(CH3COOH)________span>(填“>”“<”或“=”)2c(Na+)。Ⅱ.t ℃时,某稀硫酸溶液中c(H+)=10-a mol·L-1,c(OH-)=10-b mol·L-1,已知a+b=13。
(5)该温度下水的离子积常数Kw的数值为________。
(6)该温度下(t ℃),将100 mL 0.1 mol·L-1的稀H2SO4与100 mL 0.4 mol·L-1的NaOH溶液混合(溶液体积变化忽略不计),溶液的pH=________。
【答案】(1)否 AB (2)C (3)D (4)= (5)1×10-13 (6)12
【解析】(1)NaOH与CH3COOH溶液的反应中若二者恰好完全反应,所得CH3COONa为强碱弱酸盐,溶液的pH大于7。当溶液的pH=7时。还有部分酸未反应,故二者恰好完全反应的点应在AB区间。(2)该滴定实验中锥形瓶中液体为NaOH溶液,随着CH3COOH溶液的不断滴入,溶液的pH逐渐减小,CH3COOH溶液应该盛放在酸式滴定管甲中,为了便于确定滴定终点。可以向锥形瓶中加入酚酞做酸碱指示剂。符合条件的为C项。(3)在AB区间溶液显碱性。当CH3COOH加入比较少时,c(OH-)大于c(CH3COO-);当CH3COOH加入比较多时,c(OH-)小于c(CH3COO-);还可能出现c(OH-)等于c(CH3COO-),即上述三种情况均可能出现。(4)在D点时,溶液中n(CH3COO-)+n(CH3COOH)=0.2 mol/L×25×10-3 L=5×10-3 mol,恰好是溶液中n(Na+)的2倍,即溶液中c(CH3COO-)+c(CH3COOH)=2c(Na+)。(5)Kw=c(H+)·c(OH-)=10-a×10-b=10-(a+b)即Kw=1×1013;
(6)该混合溶液中n(H+)<n(OH-),即混合液显碱性,c(OH-)=![]() =
=
0.1 mol/L,溶液中c(H+)=![]() =1×10-12mol/L,即混合液的pH=12。
=1×10-12mol/L,即混合液的pH=12。


 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
【题目】工业上制备纯硅的热化学方程式如下:SiCl4(g)+2H2(g) ![]() Si(s)+4HCl(g)ΔH = +Q kJ·mol-1 (Q >0);某温度、压强下,将一定量反应物通入密闭容器进行反应,下列叙述正确的是 ( )
Si(s)+4HCl(g)ΔH = +Q kJ·mol-1 (Q >0);某温度、压强下,将一定量反应物通入密闭容器进行反应,下列叙述正确的是 ( )
A. 反应过程中,若增大压强能提高SiCl4的转化率
B. 若反应开始时SiCl4为1 mol,则在平衡时,吸收热量为Q kJ
C. 将反应的温度由T1升高至T2,则对应温度下的平衡常数K1>K2
D. 当反应吸收热量为0.25Q kJ时,生成的HCl恰好与1 mol NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。回答下列问题:
(1)Y在元素周期表中的位置为_____________________________.
(2)上述元素的最高价氧化物对应的水化物酸性最强的是_____________________(写化学式),非金属气态氢化物还原性最强的是_______________(写化学式)。
(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有__________________(写出其中两种物质的化学式)。
(4)ZX的电子式为_________________;ZX与水反应放出气体的化学方程式为__________________。
(5)用X元素的单质与Y元素的单质及由X、Y、Z三种元素组成的化合物的溶液构成燃料电池,写出该电池的电极反应式:负极____________,正极__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下:
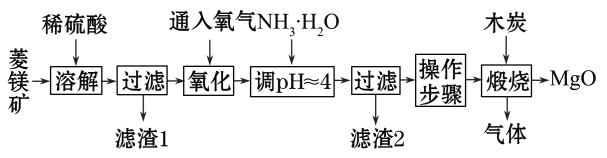
(1)通入O2氧化时,发生反应的离子方程式为________________________。
(2)滤渣2的成分是________(填化学式)。
(3)流程图中“操作步骤”为______________________、过滤等操作,得到MgSO4·7H2O晶体。对MgSO4·7H2O晶体直接加热________(填“能”或“不能”)得到无水MgSO4固体。
(4)长时间加热MgCO3悬浊液后生成Mg(OH)2,该反应的化学方程式为__________________________。
(5)已知酸碱指示剂百里酚蓝变色的pH范围如表所示:
pH | <8.0 | 8.9~9.6 | >9.6 |
颜色 | 黄色 | 绿色 | 蓝色 |
25 ℃时,向Mg(OH)2的饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为__________[25 ℃时,Ksp[Mg(OH)2]=5.6×10-12]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下在溶液里可发生如下两个离子反应:
Ce4++Fe2+===Fe3++Ce3+;Sn2++2Fe3+===2Fe2++Sn4+
由此可以确定Fe3+、Ce4+、Sn4+三种离子的氧化性由强到弱的顺序( )
A. Sn4+、Fe3+、Ce4+ B. Sn4+、Ce4+、Fe3+
C. Ce4+、Fe3+、Sn4+ D. Fe3+、Sn4+、Ce4+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在强碱的无色溶液中,下列各组离子能大量共存的是( )
A. K+、Na+、NO3-、Br- B. Na+、NH4+、NO3-、Cl-
C. K+、Na+、HCO3- 、NO3- D. K+、Cu2+、Cl-、SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com