
����Ŀ����ҵ���Ʊ�������Ȼ�ѧ����ʽ���£�SiCl4(g)��2H2(g) ![]() Si(s)��4HCl(g)��H �� ��Q kJ��mol��1 (Q >0)��ij�¶ȡ�ѹǿ�£���һ������Ӧ��ͨ���ܱ��������з�Ӧ������������ȷ���� (�� ��)
Si(s)��4HCl(g)��H �� ��Q kJ��mol��1 (Q >0)��ij�¶ȡ�ѹǿ�£���һ������Ӧ��ͨ���ܱ��������з�Ӧ������������ȷ���� (�� ��)
A. ��Ӧ�����У�������ѹǿ�����SiCl4��ת����
B. ����Ӧ��ʼʱSiCl4Ϊ1 mol������ƽ��ʱ����������ΪQ kJ
C. ����Ӧ���¶���T1������T2�����Ӧ�¶��µ�ƽ�ⳣ��K1>K2
D. ����Ӧ��������Ϊ0.25Q kJʱ�����ɵ�HClǡ����1 mol NaOH��Ӧ
���𰸡�D
��������A���÷�Ӧ����Ϊ�������������С�ķ�Ӧ��������ѹǿ��ƽ�������ƶ���SiCl4��ת���ʼ�С����A����B�����淴Ӧ���ص��Dz��ܽ��е��ף�����Ӧ��ʼʱSiCl4Ϊ1 mol������ƽ��ʱ����������С��QkJ����B����C���÷�ӦΪ���ȷ�Ӧ�������¶�ƽ�������ƶ���ƽ�ⳣ��������Ӧ���¶���T1������T2����Ӧ��ƽ�ⳣ��K1��K2����C����D����������Ȼ�ѧ����ʽ֪������Ӧ��������Ϊ0.25QkJʱ�����ɵ�HClΪ1mol��ǡ����1 molNaOH��Ӧ����D��ȷ����ѡD��


 �����Ծ�ϵ�д�
�����Ծ�ϵ�д� �ο�����������100��ϵ�д�
�ο�����������100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijʵ��С��������װ�ý����Ҵ���������ʵ�顣
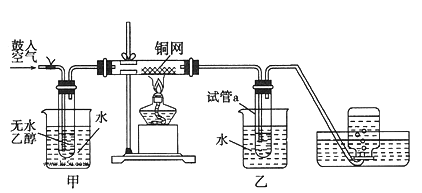
��1��ʵ�������ͭ�����ֺ�ɫ�ͺ�ɫ�����������д����Ӧ�Ļ�ѧ����ʽ��
________________________��_____________________________ ��
�ڲ��Ϲ������������£�Ϩ��ƾ��ƣ���Ӧ���ܼ������У�˵�����Ҵ�����Ӧ��_____��Ӧ��
��2����������ˮԡ���ò���ͬ����������___________���ҵ�������____________��
��3����Ӧ����һ��ʱ����Թ�a�����ռ�����ͬ�����ʣ�������____________��
��4�����Թ�a���ռ�����Һ������ɫʯ����ֽ���飬��ֽ�Ժ�ɫ��˵��Һ���л�����_____����д���ƣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������0.100 0 mol��L��1NaOH��Һ�ζ�20.00 mL 0.100 0mol��L��1CH3COOH��Һ���õζ���������ͼ������˵����ȷ����( )

A��������ʾ��Һ�У�c(CH3COO��)��c(OH��)��c(CH3COOH)��c(H��)
B��������ʾ��Һ�У�c(Na��)��c(CH3COOH)��c(CH3COO��)
C��������ʾ��Һ�У�c(Na��)>c(OH��)>c(CH3COO��)>c(H��)
D���ζ������п��ܳ��֣�c(CH3COOH)>c(CH3COO��)>c(H��)>c(Na��)>c(OH��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ʒ�Һ��Cr2O72-��ͨ�����з�Ӧת���ɸ���(PbCrO4)��Cr2O72-��aq��+2Pb2+��aq��+H2O��l��![]() 2 PbCrO4��s��+2H+��aq������H< 0�÷�Ӧ��ƽ��ı�������ʾ�ķ�Ӧ����������ʾ��ͼ��ȷ���ǣ� ��
2 PbCrO4��s��+2H+��aq������H< 0�÷�Ӧ��ƽ��ı�������ʾ�ķ�Ӧ����������ʾ��ͼ��ȷ���ǣ� ��
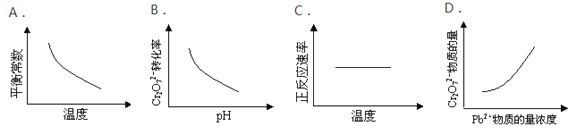
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������������߷��ļ��ڣ���������β����ȼúβ�������������ԭ��֮һ��
��1������β����������Ҫԭ��Ϊ��2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)
2CO2(g)+N2(g)
����һ�������£���һ���ݻ��̶�Ϊ2L���ܱ������г���0.8molNO��1.20molCO����ʼ��Ӧ��3minʱ���CO��ת����Ϊ20%������N2��ʾ��ƽ����Ӧ����ΪV(N2)=__________��
�ڶ������෴Ӧ����ij��֣�B����ƽ��ѹǿ��PB���������ʵ���Ũ�ȣ�CB��Ҳ���Ա�ʾƽ�ⳣ��������Kp������÷�Ӧƽ�ⳣ���ı���ʽKp=______________��
�۸÷�Ӧ�ڵ��������Է����У��÷�Ӧ�ġ�H_______0����ѡ�>������=����<����
����ijһ���ȣ����ݵ��ܱ������г���һ������NO��CO����������Ӧ���������Ӧ��������ʱ��仯��������ͼ��ʾ����֪t2��t1=t3��t2����������˵������ȷ����__________�������ţ�
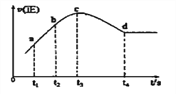
A����Ӧ��c��δ�ﵽƽ��״̬ B����Ӧ����a��С��b��
C����Ӧ��Ũ��a�����b�� D��NO��ת����t1��t2=t2��t3
��2��ʹ�ü״����Ϳ��ܼ�������β���Ի�������Ⱦ��ij��������ˮú��Ϊԭ�Ϻϳɼ״������������£�������ɱ���ܱ������з�����Ӧ��CO��g��+2H2��g��CH3OH��g��������ƽ��ʱ�����CO��H2��CH3OH�ֱ�Ϊ1mol��1mol��1mol�����������Ϊ3L�����������м���ͨ��3molCO����ʱv������____v���棩��ѡ�������������������=�������жϵ�����____________��
��3��������Ҳ�������Դ���úϳ����ڴ����������Ʊ������ѵķ�Ӧԭ��Ϊ��
2CO(g)+4H2(g)![]() CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
��֪һ�������£��÷�Ӧ��CO��ƽ��ת�������¶ȡ�Ͷ�ϱ�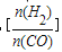 �ı仯������ͼ��
�ı仯������ͼ��
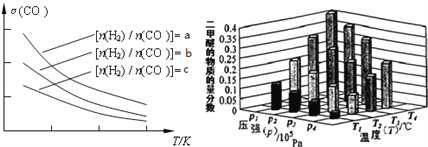
��a��b��c���Ӵ�С��˳������Ϊ___________��
��ij�¶��£���2.0mol CO��g����4.0mol H2��g�������ݻ�Ϊ2L���ܱ������У���Ӧ����ƽ��ʱ���ı�ѹǿ���¶ȣ�ƽ����ϵ��CH3OCH3��g�������ʵ��������仯�������ͼ��ʾ�������¶Ⱥ�ѹǿ�Ĺ�ϵ�ж���ȷ����___________��
A��P3��P2��T3��T2 B��P1��P3��T1��T3
C��P2��P4��T4��T2 D��P1��P4��T2��T3
���ں����ܱ������ﰴ�����Ϊ1��2����һ����̼��������һ�������·�Ӧ�ﵽƽ��״̬�����ı䷴Ӧ��ijһ�����������б仯��˵��ƽ��һ�����淴Ӧ�����ƶ�����___________��
A������Ӧ������������С
B���淴Ӧ������������С
C����ѧƽ�ⳣ��Kֵ����
D����Ӧ�������ٷֺ�������
E�����������ܶȼ�С
F��������ת���ʼ�С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȥCuSO4��5H2O�е�ɳ�ӣ���Ҫ��ʵ�����Ϊ(����)
A. �ܽ⡡���ˡ������ᾧ B. ���ȡ��ܽ⡡����
C. �ܽ⡡���ˡ����� D. �ܽ⡡���ˡ���Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ABn�ͷ��ӵ�����ԭ��A��û��δ�����γɹ��ۼ��ŶԵ��ӣ����ü۲���ӶԻ���ģ�ͣ�����˵����ȷ���ǣ� ��
A����n=2������ӵ����幹��ΪV�Ρ�����B����n=3������ӵ����幹��Ϊ������
C����n=4������ӵ����幹��Ϊ���������Ρ����� D������˵��������ȷ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪ��25 mL 0.1 mol��L��1NaOH��Һ����εμ�0.2 mol��L��1CH3COOH��Һ��������ҺpH�ı仯���ߡ���ش�
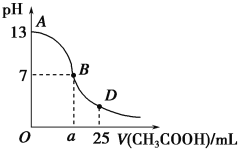
(1)B����Һ�����������˾ݴ���Ϊ����B��ʱNaOH��CH3COOHǡ����ȫ��Ӧ�����ֿ����Ƿ���ȷ��______(��ǡ���)��������ȷ�������ǡ����ȫ��Ӧ�ĵ�����AB���仹��BD�����ڣ�______����(����ȷ�����ʲ���)��
(2)���ڸõζ�ʵ����������ѡ����ѡ����ǡ����һ��________(����ĸ)��
��ƿ����Һ | �ζ�������Һ | ѡ��ָʾ�� | ѡ�õζ��� | |
A | �� | �� | ��̪ | (��) |
B | �� | �� | ���� | (��) |
C | �� | �� | ��̪ | (��) |
D | �� | �� | ��̪ | (��) |

(3)AB������c(OH��)>c(H��)����c(OH��)��c(CH3COO��)��С��ϵ��________��
A��c(OH��)����c(CH3COO��)
B��c(OH��)��c(CH3COO��)
C��c(OH��)����c(CH3COO��)
D�������������������
(4)��D��ʱ����Һ��c(CH3COO��)��c(CH3COOH)________span>(�>����<������)2c(Na��)����.t ��ʱ��ijϡ������Һ��c(H��)��10��a mol��L��1��c(OH��)��10��b mol��L��1����֪a��b��13��
(5)���¶���ˮ�����ӻ�����Kw����ֵΪ________��
(6)���¶���(t ��)����100 mL 0.1 mol��L��1��ϡH2SO4��100 mL 0.4 mol��L��1��NaOH��Һ���(��Һ�����仯���Բ���)����Һ��pH��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Һ�зֱ�ͨ����������Ӧ��������и������ӻ��ܴ������ڵ��ǣ� ��
A.������K+��Na+��SiO32����NO3��
B.��������Na+��NH4+��SO32����C1��
C.���⣺H+��K+��MnO4����SO42��
D.������K+��Na+��AlO2����CO32��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com