
【题目】X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。回答下列问题:
(1)Y在元素周期表中的位置为_____________________________.
(2)上述元素的最高价氧化物对应的水化物酸性最强的是_____________________(写化学式),非金属气态氢化物还原性最强的是_______________(写化学式)。
(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有__________________(写出其中两种物质的化学式)。
(4)ZX的电子式为_________________;ZX与水反应放出气体的化学方程式为__________________。
(5)用X元素的单质与Y元素的单质及由X、Y、Z三种元素组成的化合物的溶液构成燃料电池,写出该电池的电极反应式:负极____________,正极__________________。
【答案】 Y第2周期VIA HClO4 H2S O3、Cl2、ClO2(取其中任意二种都可) ![]()
![]() H2-2e-+2OH-=2H2O O2+4e-+2H2O =4OH-
H2-2e-+2OH-=2H2O O2+4e-+2H2O =4OH-
【解析】X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大,所以X是H元素;X、Z同主族,可形成离子化合物ZX,且Y原子序数大于Y原子序数,所以Z是Na元素;Y、M同主族,可形成MY2、MY3两种分子,所以Y是O元素,M是S元素,G是短周期主族元素,所以G是Cl元素(不考虑稀有气体),则
(1)Y是O元素,O原子有2个电子层,最外层电子数为6,处于第二周期第ⅥA族;(2)非金属元素的非金属性越强,其相应的最高价含氧酸的酸性越强,这几种元素非金属性最强的是Cl元素,所以其最高价含氧酸的酸性最强的是高氯酸HClO4;非金属性越弱,气态氢化物还原性越强,还原性最强的气态氢化物是硫化物 H2S;(3)Y的单质O3、G的单质Cl2、二者形成的ClO2均可作消毒剂;(4)ZX为NaH,属于离子化合物,由钠离子与氢负离子构成,电子式为![]() ,Na与水反应是氢氧化钠与氢气,反应化学方程式为为:NaH+H2O=NaOH+H2↑;(5)氢气在负极通入发生失去电子的氧化反应,电极反应式为H2-2e-+2OH-=2H2O。氧气在正极通入发生得到电子的还原反应,电极反应式为 O2+4e-+2H2O =4OH-。
,Na与水反应是氢氧化钠与氢气,反应化学方程式为为:NaH+H2O=NaOH+H2↑;(5)氢气在负极通入发生失去电子的氧化反应,电极反应式为H2-2e-+2OH-=2H2O。氧气在正极通入发生得到电子的还原反应,电极反应式为 O2+4e-+2H2O =4OH-。


科目:高中化学 来源: 题型:
【题目】2016年入夏以来,我国多地出现暴雨等灾害天气,抢险救灾需要大量物资,下列相关说法正确的是( )
A.救灾用的葡萄糖溶液能产生丁达尔效应
B.福尔马林可用于洪水后环境消毒和鱼肉等食益的防腐保鲜
C.医用酒精可用于灾后饮用水消毒
D.淀粉、油指、蛋白质可为灾民提供营养
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电镀废液中Cr2O72-可通过下列反应转化成铬黄(PbCrO4):Cr2O72-(aq)+2Pb2+(aq)+H2O(l)![]() 2 PbCrO4(s)+2H+(aq) ΔH< 0该反应达平衡后,改变横坐标表示的反应条件,下列示意图正确的是( )
2 PbCrO4(s)+2H+(aq) ΔH< 0该反应达平衡后,改变横坐标表示的反应条件,下列示意图正确的是( )
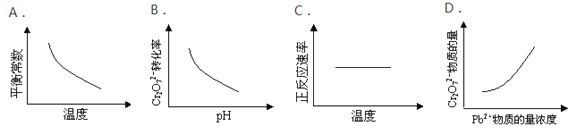
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲除去CuSO4·5H2O中的沙子,必要的实验操作为( )
A. 溶解 过滤 蒸发结晶 B. 加热 溶解 过滤
C. 溶解 过滤 蒸馏 D. 溶解 过滤 分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若ABn型分子的中心原子A上没有未用于形成共价键的孤对电子,运用价层电子对互斥模型,下列说法正确的是( )
A.若n=2,则分子的立体构型为V形 B.若n=3,则分子的立体构型为三角锥形
C.若n=4,则分子的立体构型为正四面体形 D.以上说法都不正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.“光化学烟雾”“硝酸型酸雨”的形成都与氮氧化合物有关
B.根据分散质微粒直径大小可以将分散系分为溶液、胶体和浊液
C.SiO2可用于制造光导纤维,其性质稳定,不溶于强酸、强碱
D.焰火的五彩缤纷是某些金属元素的性质的展现
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为向25 mL 0.1 mol·L-1NaOH溶液中逐滴滴加0.2 mol·L-1CH3COOH溶液过程中溶液pH的变化曲线。请回答:
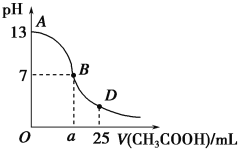
(1)B点溶液呈中性,有人据此认为,在B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确?______(填“是”或“否”)。若不正确,则二者恰好完全反应的点是在AB区间还是BD区间内?______区间(若正确,此问不答)。
(2)关于该滴定实验,从下列选项中选出最恰当的一项________(填字母)。
锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 | 选用滴定管 | |
A | 碱 | 酸 | 酚酞 | (乙) |
B | 酸 | 碱 | 甲基橙 | (甲) |
C | 碱 | 酸 | 酚酞 | (甲) |
D | 酸 | 碱 | 酚酞 | (乙) |

(3)AB区间,c(OH-)>c(H+),则c(OH-)与c(CH3COO-)大小关系是________。
A.c(OH-)大于c(CH3COO-)
B.c(OH-)小于c(CH3COO-)
C.c(OH-)等于c(CH3COO-)
D.上述三种情况都可以
(4)在D点时,溶液中c(CH3COO-)+c(CH3COOH)________span>(填“>”“<”或“=”)2c(Na+)。Ⅱ.t ℃时,某稀硫酸溶液中c(H+)=10-a mol·L-1,c(OH-)=10-b mol·L-1,已知a+b=13。
(5)该温度下水的离子积常数Kw的数值为________。
(6)该温度下(t ℃),将100 mL 0.1 mol·L-1的稀H2SO4与100 mL 0.4 mol·L-1的NaOH溶液混合(溶液体积变化忽略不计),溶液的pH=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用含有杂质(FeO、Fe2O3)的废CuO制备胆矾晶体经历下列过程(已知:Fe3+在pH=5时已完全沉淀):
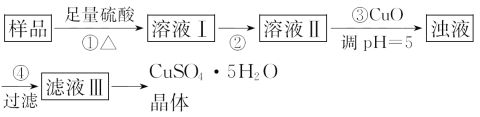
下列分析正确的是( )
A.用98%的浓硫酸配制溶解所用的4.5 mol·L-1的稀硫酸,需4种玻璃仪器
B.步骤②目的是将溶液Ⅰ中的Fe2+充分转化成Fe3+,实验操作是向溶液Ⅰ中通入足量的氯气
C.利用Cu(OH)2替代CuO也可调节溶液pH而不影响实验结果
D.步骤④之后的实验操作是蒸干溶剂结晶,所需仪器是蒸发皿、玻璃棒、酒精灯、泥三角、三脚架
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com