
【题目】下列有关氢氧化铁胶体说法正确的是
A. 将外加直流电源通过该胶体,阴极处颜色变深,则说明该胶体带正电荷
B. 鉴别FeCl3溶液和Fe(OH)3胶体,可用丁达尔效应或观察颜色两种方法
C. 采用过滤,可将Fe(OH)3胶体中的FeCl3杂质除去
D. 向Fe(OH)3胶体中加入大量盐酸溶液,则可引起胶体聚沉
科目:高中化学 来源: 题型:
【题目】在强酸性溶液中,能大量共存的离子组是
A. Al3+、Ag+、NO3-、Cl- B. Mg2+、NH4+、NO3-、Cl-
C. Ba2+、K+、S2-、Cl- D. Na+、NO3-、HCO3-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,一定浓度的某溶液,由水电离的出的c(OH-)=1×10-4 mol/L,则该溶液中的溶质可能是
A.H2SO4 B.NaOH C.KHSO4 D.CH3COONa
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完全沉淀等物质的量浓度的NaCl、MgCl2、A1C13溶液中的Cl-,消耗等物质的量浓度的AgNO3溶液的体积比为3: 2: 1,则上述溶液的体积比为
A.1: 1: 1 B.3: 2: 1 C.9: 3: 1 D.6: 3: 2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答氯碱工业的如下问题:
(1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k=__________
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO42-等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②盐酸 ③BaCl2,
这三种试剂添加的合理顺序是______________(填序号)
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
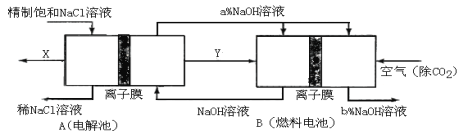
①图中X、Y分别是_____________、_____________(填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小 。
②分别写出燃料电池B中正极、负极上发生的电极反应: 、 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一条件下,把物质A,B按一定比例充入容积为2L的球开容器,发生如下反应:
2A(g)+B(g)![]() 2C(g);△H=-180KJ.mol-1
2C(g);△H=-180KJ.mol-1
(1) 写出该反应的化学平衡常数表达式 K=__________________
(2)降低温度,该反应K值_________,A转化率____________,化学反应速度________(以上均填“增大,减小或不变”)
(3) 若平均每分钟生成0.5mol的C,则此反应速率可表示为V(C)=__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学—物质结构与性质】如右图是元素周期表的一部分。已知R的核电荷数小于36,气态氢化物沸点:MHn>YHn。
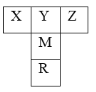
(1)表中五种元素第一电离能最大的是 (填元素符号),Y的最简单氢化物分子的空间构型为 ,基态R原子中有 个未成对电子。
(2)Y的最高价氧化物熔点比M的最高价氧化物熔点低,原因是 ,YZ-中σ键与π键的个数比为 。
(3)YO32-中Y原子的杂化方式是 ,写出一种与YO32-互为等电子体的粒子 (用化学符号表示)。
(4)Z的一种常见氢化物能与硫酸铜反应生成配合物。请用结构简式表示该配合物中的阳离子: 。
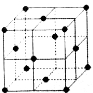
(5)如图为某金属单质的面心立方晶胞结构示意图,该晶体中配位数是 ;测得此晶体的密度为2.7g.cm-3,晶胞的边长为0.405nm,则此金属原子的相对原子质量为 (结果保留整数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知可逆反应aA+bB![]() cC中,物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是
cC中,物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是
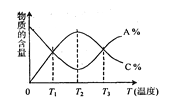
A.该反应在T1、T3温度时达到过化学平衡
B.该反应在T2温度时达到过化学平衡
C.该反应的逆反应是放热反应
D.升高温度,平衡会向正反应方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com