
下面是利用工业冶炼硫酸铜(含有Fe2+、AsO2-、Ca2+等杂质)提纯制备电镀硫酸铜的生产流程。

已知:①Fe3+ Cu2+ 开始沉淀的pH分别2.7、5.4,完全沉淀的pH分别为3.7、6.4;
②KSP[(Cu(OH)2]=2×10-20
(1)溶解操作中需要配制含铜64g/L的硫酸铜溶液100L,需要称量冶炼级硫酸铜的质量至少为 Kg。
(2)氧化步骤中发生的离子反应方程式为①
②AsO2— + H2O2+ H+=H3AsO4 ③ H3AsO4+ Fe3+=FeAsO4↓+ 3H+
(3)若要检验调节pH后溶液的Fe3+是否除尽,方法是 ;氧化后需要将溶液进行稀释,稀释后的溶液中铜离子浓度最大不能超过 mol·L-1。
(4)固体I的主要成分除 FeAsO4外还有 ,操作I为
(5)利用以上电镀级硫酸铜作为电解质溶液,电解粗铜(含铁、银杂质)制备纯铜,写出阳极发生的电极反应方程式
(16分)
(1)16 (2分)
(2)H2O2+2 H+ +2Fe2+ = 2Fe3+ +2H2O (2分)
(3)取少量溶液Ⅰ于试管, 加入几滴KSCN溶液,若溶液不出现红色,则说明Fe3+已经除尽;2×10-2
(各2分,共4分)
(4)Fe(OH)3、CaCO3(各1分,共2分);蒸发浓缩、冷却结晶、过滤干燥(2分,答对两个给即可)
(5)Fe—2e—= Fe2+ ;Cu —2e—= Cu2+ (各2分,共4分)
【解析】
试题分析:(1)m(CuSO4)=64g/L×100L÷(64/160)=16000g=16Kg。
(2)溶液中含具有还原性的Fe2+,H2O2与Fe2+发生氧化还原反应,离子方程式为:H2O2+2 H+ +2Fe2+ = 2Fe3+ +2H2O。
(3)Fe3+能与SCN反应,溶液变为红色,所以检验调节pH后溶液的Fe3+是否除尽,方法是:取少量溶液Ⅰ于试管, 加入几滴KSCN溶液,若溶液不出现红色,则说明Fe3+已经除尽;因为需要把溶液的pH调节至5,即c(OH)=10-9molL1,根据KSP[(Cu(OH)2]可得Cu2+恰好沉淀时的Cu2+浓度为:c(Cu2+)=2×10-20÷(10-9)2=2×10-2,稀释后的溶液中铜离子浓度最大不能超过2×10-2molL1。
(4)加入Na2CO3后,CO32与Ca2+反应生成CaCO3沉淀,Fe3+开始沉淀的pH分别2.7,完全沉淀的pH分别为3.7,所以pH调节至5时,Fe3+转化为Fe(OH)3沉淀,所以固体I的主要成分除 FeAsO4外还有Fe(OH)3、CaCO3;根据流程图可知经过操作I得到电镀硫酸铜和溶液II,则操作I为:蒸发浓缩、冷却结晶、过滤干燥。
(5)电解粗铜(含铁、银杂质)制备纯铜,阳极为粗铜,粗铜中Fe与Cu在阳极失去电子,所以阳极发生的电极反应方程式为:Fe—2e—= Fe2+ ;Cu —2e—= Cu2+。
考点:本题考查化学流程的分析、离子方程式的书写、化学计算、电解原理及应用。


科目:高中化学 来源:2014-2015学年广东省清远市高三上学期期末理综化学试卷(解析版) 题型:填空题
(16分)金属钛(Ti)性能优越,被称为继铁、铝之后的“第三金属”。工业上以钛铁矿(主要成分FeTiO3,含FeO、Al2O3、SiO2等杂质)为主要原料冶炼金属钛,其生产的工艺流程图如下:

已知:2H2SO4(浓)+ FeTiO3=TiOSO4 + FeSO4 + 2H2O
(1)步骤I中发生反应的离子方程式: 、 。
(2)已知:TiO2+易水解,只能存在于强酸性溶液中。
25 ℃时,难溶电解质溶解度(s)与pH关系如图,TiO(OH)2溶度积Ksp=1×10-29

①步骤Ⅲ加入铁屑原因是 。
②TiO2+水解的离子方程式为 。向溶液II中加入Na2CO3粉末的作用是 。
当溶液pH接近 时,TiO(OH)2已沉淀完全。
(3)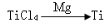 反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据下表信息,需加热的温度略高于 ℃即可。
反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据下表信息,需加热的温度略高于 ℃即可。
TiCl4 | Mg | MgCl2 | Ti | |
熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
(4)研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用下图所示装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛。写出阳极上所发生的反应式: 。

查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省清远市高三上学期期末理综化学试卷(解析版) 题型:选择题
常温下,下列有关物质的量浓度关系正确的是
A.等物质的量浓度的溶液中,水电离出的c(H+):HCl>CH3COOH
B.pH相同的溶液中:c(Na2CO3)<c(NaHCO3)
C.在Na2SO3溶液中:c(Na+) = 2c(SO32— ) + c(HSO3— ) + c(OH— )
D.0.1mol·L—1NaHS溶液中:c(Na+) = c(HS-)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省茂名市高三一模考试理综化学试卷(解析版) 题型:选择题
下列实验操作能达到预期实验目的的是
选项 | 目的 | 操作 |
A | 检验Fe2(SO4)3溶液中是否含有FeSO4 | 取少量溶液于试管, 加入几滴0.1 mol/L KMnO4溶液 |
B | 证明Al(OH)3是两性氢氧化物 | 取Al(OH)3于试管A、B,分别滴加氨水与盐酸 |
C | 比较S与P元素非金属性强弱 | 测定等浓度H2SO3、H3PO4的pH |
D | 除去Na2CO3中的NaCl | 溶解,加入AgNO3溶液至不再产生沉淀,静置,过滤 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省部分普高高三2月联考化学试卷(解析版) 题型:填空题
【选修3—物质结构与性质】(14分)
前四周期元素X、Y、Z、W、R的原子序数依次增大,已知:X原子的2p轨道为半充满状态;Y原子的L层有2个未成对电子;Z与Y位于同主族;W的+2价简单离子核外电子层排布与Ar原子相同;R原子的d轨道上有3个空轨道。请回答下列问题:
(1)R原子的基态电子排布式为 。
(2)X、Y原子的第一电离能大小顺序为 。(用元素符号表示)
(3)X的常见单质分子结构中σ键数目为 。
(4)Z的最高价氧化物对应水化物的酸根离子空间构型为 ,中心原子的杂化轨道类型为 。
(5)某矿物晶体由Y、W、R三种元素组成,其晶胞结构如图所示。

则该矿物的化学式为 ,若已知该晶胞的边长为a cm,则该晶胞的密度为 g/cm3。(用含a、NA的代数式表示)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省部分普高高三2月联考化学试卷(解析版) 题型:选择题
向含S2—、Fe2+、Br—、I—各0.1mol的溶液中通入Cl2,通入Cl2的体积(标准状况)和溶液中相关离子的物质的量关系图正确的是 :

查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高三上学期期末考试化学试卷(解析版) 题型:选择题
有关AgCl沉淀的溶解平衡说法正确的是
A.此时,AgCl沉淀溶解速率为零
B.AgCl难溶于水,溶液中没有Ag+ 和Cl—
C.升高温度,AgCl沉淀的溶解度增大
D.向AgCl沉淀中加入NaCl固体,AgCl沉淀的溶解度不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com