
【题目】俄罗斯科学家在利用回旋加速器进行的实验中,用含20个质子的钙元素的同位素反复轰击含95个质子的镅元素,结果4次成功制成4个第115号元素的原子。这4个原子在生成数微秒后衰变成第113号元素。前者的一种核素为![]() X。下列有关叙述正确的是
X。下列有关叙述正确的是
A. X元素的核外电子数为288
B. 113号元素属于IIIB族
C. 镅元素属于过渡元素
D. 核素![]() X的质量数与中子数之差为173
X的质量数与中子数之差为173
科目:高中化学 来源: 题型:
【题目】(1) 0.2 mol某烃A在氧气中完全燃烧后,生成CO2和H2O各0.6 mol。
① 烃A的分子式为____________。
② 若烃A能使溴水褪色,其结构简式为
③ 已知含碳碳双键的有机物与卤化氢发生加成反应时,氢原子总是加到含氢较多的双键
碳原子上。
依此规则,A与HBr发生加成反应生成的物质B的结构简式为
(2) 苹果酸是一种常见的有机酸,其结构简式为![]() 。
。
①苹果酸的分子式为_________;
②苹果酸中含有两种官能团的名称分别是 、 。
③1 mol 苹果酸与足量金属钠反应,能生成标准状况下的氢气的体积为__________
④苹果酸可能发生的反应是(选择填空)___________。
A.取代反应 B.加成反应 C.氧化反应 D.加聚反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应原理的发展在化学的发展史上有重要的推动作用。
(1)下图为N2和O2生成NO时的能量变化情况。

则NO分解为N2和O2的反应是 (填“吸热”或“放热”)反应。
(2)在某体积为2L的密闭容器中充入0.5molNO2和1molCO,一定条件下发生反应:
NO2(g)+ CO(g) ![]() CO2(g)+NO(g),2min时,测得容器中NO的物质的量为0.2mol。
CO2(g)+NO(g),2min时,测得容器中NO的物质的量为0.2mol。
①该段时间内,用CO2表示的平均反应率为 。
②下列事实能说明此反应在该条件下已经达到化学平衡的是 (填序号)。
A.容器内气体总质量保持不变 B.NO2的物质的量浓度不再改变
C.NO2的消耗速率与CO2的消耗速率相等 D.容器内气体总物质的量保持不变
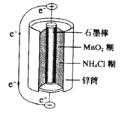
(3)锌锰干电池是最早使用的化学电池,其基本构造如下图所示。电路中每通过0.4mol电子,负极质量减少 g;工作时NH4+在正极放电产生两种气体,其中一种气体分子是含10电子的微粒,正极的电极反应式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组将下图所示装置按一定顺序连接,在实验室里制取一定量的FeCl3(所通气体过量并充分反应)。

请回答下列问题:
(1)各装置的正确连接顺序为(填写装置代号)A→______→_____→______→______。
(2)装置C的作用是_____________________;装置D的作用是_______________________;装置E的作用是_______________________。
(3)反应开始后,B中硬质玻璃管内的现象为______________________;可以检验生成物中含有Fe3+的试剂是____________(填写试剂名称)。
(4)A中发生反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是
A. 原电池是利用氧化还原反应将化学能转换为电能的装置
B. 由于生铁中含碳,所以比纯铁耐腐蚀
C. 在原电池中,电子从正极流向负极
D. 在原电池中,负极上发生还原反应,正极上发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化过程需要吸收能量的是( )
A. 2H2+O2=2H2O B. CaO+H2O=Ca(OH)2
C. Cl+Cl→Cl2 D. N2→N+N
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为提纯下列物质(括号内物质为杂质),所选用的除杂试剂和分离方法正确的是
被提纯的物质 | 除杂试剂 | 分离方法 | |
A | 乙酸乙酯(乙醇) | 乙酸 | 加热回流 |
B | 乙烷(乙烯) | 酸性KMnO4 | 洗气 |
C | 乙醇(乙酸) | 新制氧化钙 | 蒸馏 |
D | 苯(溴) | 碘化钾溶液 | 分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】课题式研究性学习是培养学生创造思维的良好方法.某研究性学习小组将下列装置如图连接,D、F、X、Y 都是铂电极、C、E是铁电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答下列问题:

(1)电源B 极的名称是___________。
(2)甲装置中电解反应的总化学方程式是:________________________。
(3)设电解质溶液过量,则同一时间内C、D电极上参加反应的单质或生成的单质的物质的量之比是__________。
(4)欲用丙装置将粗铜(含少量铁、锌等杂质)精炼,G极材料应该是__________(填“粗铜”或“精铜”),电解液中原电解质的物质的量浓度将__________(填“变大”、“变小”或“不变”)。
(5)设甲池中溶液的体积在电解前后都是500ml,当乙池所产生气体的体积为4.48L(标准状况)时,甲池中所生成物质的物质的量浓度为 mol/L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com