


 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
| A、①②③ | B、①③④ |
| C、②③④ | D、全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 现象或事实 | 解释 |
| A | 明矾用于净水 | 铝离子水解产生的胶体具有很强吸附杂质的作用 |
| B | SO2能使品红溶液褪色 | SO2具有漂白性 |
| C | “地沟油”禁止食用,但可以用来制肥皂 | “地沟油”主要成分为油脂属于酯类可以发生皂化反应 |
| D | 用氯水和淀粉溶液鉴别食盐是否加碘 | 目前加碘食盐中含碘元素物质为KI |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
 有如下化学反应:2A(g)+B(g)?2C(g),△H<0.
有如下化学反应:2A(g)+B(g)?2C(g),△H<0.查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、Cu2S只作还原剂 |
| B、该反应中的氧化剂只有O2 |
| C、Cu2S 中的Cu元素被S元素还原 |
| D、当1 mol O2参加反应时,共转移4 mol e- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol H2所占体积约为22.4 L |
| B、22 g CO2中含有的分子数约为6.02×1023 |
| C、100 mL 0.5 mol/L NaOH溶液中含溶质的质量为0.05 g |
| D、标准状况下,11.2 L O2和H2的混合气体所含分子数约为3.01×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:
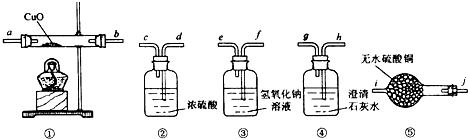
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、K+、C1O-、I- |
| B、C1-、NO3-、Fe2+、Na+ |
| C、K+、Ba2+、OH-、SO42- |
| D、Fe3+、NH4+、Cl-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com