
����A��E�������±��е�������ɵģ������½������ʵ���
Һ��1 mLϡ�͵�1 000 mL��pH�ı仯��ϵ��ͼ����ʾ������A��D��Ӧ�õ�E����ش��������⡣
| ������ | NH4+��H����Na�� |
| ������ | OH����CH3COO����Cl�� |


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��16�֣��Ƽ��仯������й㷺����;��
(1)��ҵ���Ʊ������Ƶij��÷����� (�����ӷ���ʽ��ʾ)��
(2)��Na2CO3������������ʣ�CO��O2��CO2Ϊԭ�Ͽ�������͵�ء��õ�صĽṹ��ͼ��ʾ��
�����ĵ缫��ӦʽΪ ����ع���ʱ����A��ѭ��ʹ�ã�A���ʵĻ�ѧʽΪ ��
(3)�����£�Ũ�Ⱦ�Ϊ0.1 mol��L��1����������������Һ��pH���±���
| ���� | CH3COONa | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 11.6 | 10.3 | 11.1 |
| ���� | Fe2�� | Cu2�� | Mg2�� |
| pH | 7.6 | 5.2 | 10.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
����Ũ�Ⱦ�Ϊ0.1 mol/L��������Һ�������ᡡ�ڴ��ᡡ���������ơ����Ȼ��
��ش��������⣺
(1)�٢ڢۢ�������Һ����ˮ�������H��Ũ���ɴ�С��˳����(�����)________��
(2)���ۺܵ͢������Ϻ��Һ�и�����Ũ���ɴ�С��˳����____________��
(3)��֪t��C��KW��1��10��13����t��C______(�����������������)25��C��
(4)25��Cʱ����pH��x�������pH��y������������Һ(x��6��y��8)��ȡa L��������b L������������Һ��Ӧ��ǡ����ȫ�к͡�����Һ��pH(x��y)�Ĺ�ϵʽΪ________________(�����ʽ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��һѧ����ʵ���Ҳ�ij��Һ��pH,ʵ��ʱ,����������ˮ��ʪpH��ֽ,Ȼ���ýྻ����IJ�����պȡ�������м��:
(1)��ѧ���IJ�������������(���ȷ�ġ�����ġ�),����������������������������������
(2)���ô˷����ֱ�ⶨc(H+)��ȵ�����ʹ�����Һ��pH,���ϴ������������,ԭ����
������������������������������
(3)��ѧ����������ʽ�ⶨ������Һ��pH,��������(����)
| A��NaOH | B��CH3COONa | C��NaCl | D��NaHSO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��pH��4�����ᡢ���ᡢ������ƿ��Һ��(�����ã�����������ʾ)
(1)��������Һ�����ʵ���Ũ������Ϊc1��c2��c3�������ϵ�� ��
(2)ȡ��ͬ�����������ֱ��������ˮϡ�͵�pH��6����ˮ���������ΪV1��V2��V3�������ϵ�� ��
(3)��ȫ�к���������ʵ���Ũ�Ⱦ���ͬ��Ba(OH)2��Һʱ��������������ʵ�������Ϊn1��n2��n3�������ϵ�� ��
(4)ȡͬ����������Һ�ֱ����������п�ۣ���Ӧ��ʼ�ų�H2����������Ϊv1��v2��v3�������ϵ�� ����Ӧ�����зų�H2����������Ϊva��vb��vc�������ϵ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��ͼ��ʾ��������Ϊ��Һ��pHֵ��������ΪZn2�����ӻ�Zn(OH)42���������ʵ���Ũ�ȵĶ������ش��������⡣
(1)��ZnCl2��Һ�м�������������������Һ����Ӧ�����ӷ���ʽ�ɱ�ʾΪ��________��
(2)��ͼ�����ݼ���ɵ�Zn(OH)2���ܶȻ�(Ksp)��________��
(3)ij��Һ�к�Zn2�����ӣ�Ϊ��ȡZn2�����ӿ��Կ�����Һ��pHֵ�ķ�Χ��________________________��
(4)��֪����ZnCl2��Һ�м�������Ǧ�����Ǧ��Һ�����Ƶ�PbCl2��ɫ���壻25��ʱ��PbCl2�����������е��ܽ�����£�
| c(HCl)/( mol��L��1) | 0.50 | 1.00 | 2.04 | 2.90 | 4.02 | 5.16 | 5.78 |
| c(PbCl2)/( mol��L��1)��10��3 | 5.10 | 4.91 | 5.21 | 5.90 | 7.48 | 10.81 | 14.01 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��Ҫ��ش��������⣺
��1��ʵ�����г���NaOH��Һ������ϴ�����ᴿ����100mL 3mol/L��NaOH��Һ���ձ�״����4��48L CO2ʱ��������Һ�и�����Ũ���ɴ�С��˳��Ϊ
��2����������һ�������0��1 mol/L������Һ�м�ˮϡ�ͺ�����˵����ȷ���� ��
A����Һ�е������ӵ���Ŀ����
B����ĵ���̶�����c(H+)������
C����Һ��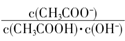 ����
����
D��Һ�� ��С
��С
��3���ٳ����½�0��15 mol/Lϡ����V1 mL��0��1 mol/L NaOH��ҺV2 mL��ϣ�������Һ��pHΪ1����V1��V2= ����Һ����仯���Բ��ƣ���
�ڳ���������Һ��pH=3��HA��ҺV1mL��pH=11��NaOH��ҺV2mL��϶��ã�������˵����ȷ����
A������Ӧ����Һ�����ԣ���
B����V1=V2,��Ӧ����ҺpHһ������7
C������Ӧ����Һ�����ԣ���V1һ������V2
D������Ӧ����Һ�ʼ��ԣ���V1һ��С��V2
��4�������£�Ũ�Ⱦ�Ϊ0��lmol/L������������Һ��PHֵ�����ʾ��
�ٸ��ݱ������ݣ���Ũ�Ⱦ�Ϊ0��01 mol/L���������������Һ�ֱ�ϡ��100����pH�仯��С����
A��HCN B��HClO C��H2CO3 D��CH3COOH
�ڸ����������ݣ��ж����з�Ӧ���Գ������� ��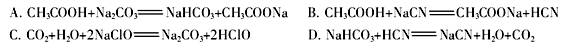
��5���������ӿ�ʼ����ʱ��pH���±���
������ͬŨ�� ���ӵ���Һ�еμ�NaOH��Һʱ�� �������ӷ��ţ��ȳ�����
���ӵ���Һ�еμ�NaOH��Һʱ�� �������ӷ��ţ��ȳ����� �����������������������
�����������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�±��Dz�ͬ�¶���ˮ�����ӻ������ݣ�
| �¶�/�� | 25 | t1 | t2 |
| ˮ�����ӻ� | 1��10��14 | a | 1��10��12 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
���С������г��漰�ơ����仯���
(1)ʵ���ҿ�����ˮ�Ҵ��������������Ľ����ƣ���ѧ��Ӧ����ʽΪ ��Ҫ��ϴ�������Թܱ��ϵ����õ��Լ��� ��
(2)��ͼΪ�Ƹ��ܵ�صĽṹʾ��ͼ���õ�صĹ����¶�Ϊ320 �����ң���ط�ӦΪ2Na+xS=Na2Sx,�����ĵ缫��ӦʽΪ ��M(��Na2O��Al2O3�Ƶ�)������������ ��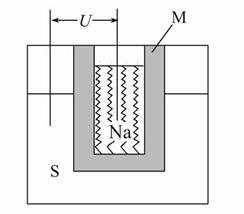
��Ǧ������ȣ���������ͬ�����ĸ�����������ʱ�������ص����۷ŵ�����Ǧ���ص� __ ����
(3)Na2S��Һ������Ũ���ɴ�С��˳��Ϊ �������Һ�м�����������CuSO4����ҺpH (���������С�����䡱)��Na2S��Һ���ڷ�������������ԭ��Ϊ (�����ӷ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com