
【题目】已知4NH3+5O2=4NO+6H2O ,若反应速率分别用V(NH3)、 V(O2)、V(NO)、V(H2O)表示,则正确的关系是
A. ![]() V(NH3)=V(O2) B.
V(NH3)=V(O2) B. ![]() V(O2)=V(H2O)
V(O2)=V(H2O)
C. ![]() V(NH3)=V(H2O) D.
V(NH3)=V(H2O) D. ![]() V(O2)=V(NO)
V(O2)=V(NO)
科目:高中化学 来源: 题型:
【题目】某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合溶液(已知氯气和NaOH在一定温度下能发生反应:Cl2+2NaOH=NaCl+NaClO+H2O ,3Cl2+6NaOH=5NaCl+NaClO3+3H2O),经测定ClO﹣与ClO3﹣的物质的量之比为1:2,则氯气与氢氧化钠反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为
A.21:5 B.11:3 C.3:1 D.4:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法不正确的是
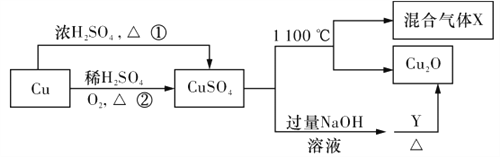
A. 相对于途径①,途径②更好地体现了绿色化学思想
B. Y可以是葡萄糖溶液
C. CuSO4在1100℃分解所得气体X是SO2和SO3的混合气体
D. 将CuSO4溶液蒸发浓缩、冷却结晶可制得胆矾晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯碱工业是以电解饱和食盐水为基础的基本化学工业。下图是某氯碱工业生产原理示意图:
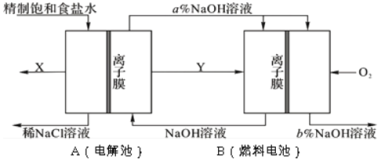
(1)写出装置A在通电条件下反应的化学方程式______________。
(2)A装置所用食盐水由粗盐水精制而成。精制时,为除去食盐水中的Mg2+和Ca2+,要加入的试剂分别为___________、___________。
(3)氯碱工业是高耗能产业,按上图将电解池与燃料电池相组合的新工艺可以节(电)能30%以上,且相关物料的传输与转化关系如图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
①图中Y是______________(填化学式);X与稀NaOH溶液反应的离子方程式是:______________。
②分析比较图示中氢氧化钠质量分数a%与b%的大小___________。
③若用B装置作为A装置的辅助电源,每当消耗标准状况下氧气的体积为11.2 L时,则B装置可向A装置提供的电量约为______________(一个e-的电量为1.60×10-19C;计算结果精确到0.01)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作与安全事故处理正确的是
A. 做H2还原CuO的实验时,为防止H2爆炸,实验完毕,应先停止通H2,再停止加热
B. 配制稀硫酸溶液时,先在量筒加入一定体积的水,再沿容器壁慢慢加入浓硫酸,并不断搅拌
C. 用试管夹从试管底由下往上夹住距离管口约2/3处,手持试管夹长柄末端进行加热
D. 分液漏斗在使用前要检漏,使用过程中要适当旋开活塞放气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与有机物的结构、性质的有关叙述中正确的是( )
A.乙烯、氯乙烯、聚乙烯均可使酸性高锰酸钾溶液褪色
B.乙酸与乙醇可以发生酯化反应,又均可与金属钠发生置换反应
C.分馏、干馏都是物理变化,裂化、裂解都是化学变化
D.石油经过分馏得到多种烃,煤经过分馏可制得焦炭、煤焦油等产品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图是金属牺牲阳极的阴极保护法的实验装置,有关说法正确的是( )

A. 该装置为电解池
B. 本实验牺牲了金属Fe来保护金属Zn
C. 若加入K3[Fe(CN)6]溶液后,Fe电极附近不会产生特征蓝色的沉淀
D. 远洋货轮上镶嵌的金属Zn长时间没有什么变化,不需要更换
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在下列物质中①![]() Li ②
Li ②![]() Na③
Na③![]() Mg④
Mg④![]() Li⑤
Li⑤![]() C⑥C60⑦异丁烷⑧正丁烷⑨石墨
C⑥C60⑦异丁烷⑧正丁烷⑨石墨
互为同位素的是 (填编号,下同);互为同素异形体的是 ;
互为同分异构体的是 。
(2)在下列事实中,是什么因素影响了化学反应的速率?
夏天的食品易发霉,冬天就不易发生该现象。影响因素是 ;
MnO2加入双氧水中反应更剧烈。影响因素是 ;
同浓度、同体积的盐酸中放入同样大小的锌粒和镁条,镁条产生气体更快。影响因素是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com