
【题目】下列所陈述的事实与解释均正确的是
选项 | 实验操作及现象 | 实验结论 |
A | 用pH试纸测定NaClO溶液的酸碱性,试纸显蓝色 | NaClO水解显碱性 |
B | 收集铜与浓硝酸反应生成的气体,用冰水混合物冷却降温,气体颜色变浅 | 生成的红棕色NO2气体部分转化为无色气体 |
C | 向某溶液中加入几滴新制的氯水,再加入2滴KSCN溶液,溶液变为红色 | 原溶液中一定含有Fe2+ |
D | 甲苯能使酸性高锰酸钾溶液褪色 | 发生了萃取 |
A.AB.BC.CD.D
【答案】B
【解析】
A.次氯酸钠是强碱弱酸盐,其溶液呈碱性,但次氯酸钠水解生成的次氯酸具有漂白性,所以不能用pH试纸测定次氯酸钠溶液的pH值,现象不正确,应该用pH计,故A错误;
B.铜和浓硝酸反应生成二氧化氮,二氧化氮能自身发生转化生成无色的四氧化二氮,2NO2 ![]() N2O4,降低温度,气体颜色变浅,说明平衡向生成N2O4的方向移动,说明红棕色NO2气体部分转化为无色气体,故B正确;
N2O4,降低温度,气体颜色变浅,说明平衡向生成N2O4的方向移动,说明红棕色NO2气体部分转化为无色气体,故B正确;
C.用KSCN溶液检验溶液中是否含有亚铁离子时需要排除铁离子的干扰,应该先加KSCN溶液,然后加氯水检验亚铁离子,故C错误;
D.甲苯能被酸性高锰酸钾溶液氧化,而使酸性高锰酸钾溶液褪色,该实验发生氧化还原反应,不是发生了萃取,故D错误;
故选B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列事实不能用化学平衡移动原理解释的是
A.新制氯水长时间放置颜色变浅
B.高压比常压更有利于 SO2 转化为 SO3
C.蒸干 AlCl3 溶液无法得到无水 AlCl3
D.滴加少量 CuSO4 溶液可以加快 Zn 与稀 H2SO4 反应的速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某密闭容器中发生如下反应:X(g)+3Y(g) ![]() 2Z(g) ΔH<0,下图表示该反应的速率(v)随时间(t)变化的关系,t1、t3、t4时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中不正确的是( )
2Z(g) ΔH<0,下图表示该反应的速率(v)随时间(t)变化的关系,t1、t3、t4时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中不正确的是( )
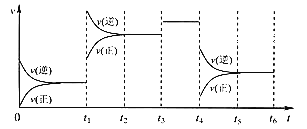
A. t1时升高了温度 B. t3时加入了催化剂
C. t4时降低了压强 D. 在t3~t4时间内,X的体积分数最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为10L的密闭容器中,进行如下反应:A(g)+2B(g)![]() C(g)+D(g),最初加入1.0mol A和2.2mol B,在不同温度下,D的物质的量n(D)和时间t的关系如图1.
C(g)+D(g),最初加入1.0mol A和2.2mol B,在不同温度下,D的物质的量n(D)和时间t的关系如图1.

试回答下列问题:
(1)800℃时,0~5min内,以B表示的平均反应速率为 .
(2)能判断反应达到化学平衡状态的依据是 (填字母).
A.容器中压强不变 B.混合气体中c(A)不变
C.2v正(B)=v逆(D) D.c(A)=c(C)
(3)若最初加入1.0mol A和2.2mol B,利用图中数据计算800℃时的平衡常数K=__________,该反应为__________反应(填“吸热”或“放热”).
(4)700℃时,某时刻测得体系中物质的量浓度如下:n(A)=1.1mol,n(B)=2.6mol,n(C)=0.9mol,n(D)=0.9mol,则此时该反应__________(填“向正方向进行”、“向逆方向进行”或“处于平衡状态”).
(5)在催化剂作用下,CO可用于合成甲醇:CO(g)+2H2(g)CH3OH(g)若在恒温恒压的条件下,向密闭容器中充入4mol CO和8mol H2,合成甲醇,平衡时CO的转化率与温度、压强的关系如图所示:

①该反应的正反应属于__________反应;(填“吸热”或“放热”).
②在0.1Mpa、100℃的条件下,该反应达到平衡时容器内气体的物质的量为 mol。
若在恒温恒容的条件下,向上述平衡体系中充入4mol CO,8mol H2,与原平衡状态相比,达到平衡时CO转化率 (填“增大”,“不变”或“减小”),平衡常数K (填“增大”,“不变”或“减小”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 常温下醋酸分子不可能存在于pH>7的碱性溶液中
B. 常温下pH=2的H2SO4与pH=13的NaOH溶液混和,所得混和液的pH=11,则H2SO4溶液与NaOH溶液的体积比是9:1
C. 0.1mol/L硫化钠溶液中,c(S2-)+c(HS-)+2c(H2S)=0.1mol/L
D. 常温下向氯化铵溶液中加入少量氨水使溶液的pH=7,则混合溶液中c(NH4+)>c(Cl-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4 + aNa2O2=2Na2FeO4 + bX + 2Na2SO4 +cO2↑该反应中物质X应是__________,b与c的关系是_______________。
(2)湿法制备高铁酸钾反应体系中有六种数粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①写出并配平湿法制高铁酸钾的离子反应方程式:__________________。
②每生成1mol FeO42-转移_____________mol电子,若反应过程中转移了0.3mol电子,则还原产[物的物质的量为_____________mol。
Ⅱ.已知:2Fe3++2I-=2Fe2++I2,2Fe2++Br2=2Fe3++2Br-。
(3)含有1 mol FeI2和2 mol FeBr2的溶液中通入2 mol Cl2,此时被氧化的离子及其物质的量是_______________________________。
(4)若向含a mol FeI2和b mol FeBr2的溶液中通入c mol Cl2,当I-、Fe2+、Br-完全被氧化时,c为________________________________(用含a、b的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍镉(Ni—Cd)可充电电池在现代生活中,有广泛应用,它的工作原理如下:Cd+2NiO(OH)+2H2O ![]() Cd(OH)2+2Ni(OH)2.下列叙述正确的是
Cd(OH)2+2Ni(OH)2.下列叙述正确的是
A. 该电池放电的时候,负极附近pH增大
B. 放电时每转移2mol电子,有2mol NiO(OH)被氧化
C. 充电时,阳极反应式是Ni(OH)2-e-+OH-=NiO(OH)+H2O
D. 充电时,Cd电极接电源正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2﹣羟基异丁酸乙酯能溶于水,是一种应用于有机合成和药物制造的化工原料。

(1)2﹣羟基异丁酸乙酯的分子式为_________,不同化学环境的氢在核磁共振氢谱图中有不同的吸收峰,则2﹣羟基异丁酸乙酯有_________个吸收峰;
(2)①②的反应类型分别为_________,_________;
(3)已知I为溴代烃,I→B的化学方程式为_________;
(4)缩聚产物F的结构简式为_________;
(5)下列关于![]() 和
和 的说法正确的有_________(双选,填字母);
的说法正确的有_________(双选,填字母);
A.后者遇到FeCl3溶液显紫色,而前者不可
B.两者都可以与NaHCO3溶液反应放出CO2
C.两者都可以与氢氧化钠溶液发生反应,当两者物质的量相等时,消耗氢氧化钠的量不相等
D.两者都可以与氢气发生加成反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com