
【题目】若以M表示水的摩尔质量(g/mol),V表示在标准状况下水蒸气的摩尔体积(L/mol),ρ为标准状况下水蒸气的密度(g/L),NA为阿伏加德罗常数,m和α分别表示每个水分子的质量(g)和体积(L),下面四个关系式的判断正确的是:
①NA=![]() ②ρ=
②ρ= ![]() ③m =
③m =![]() ④α=
④α=![]()
A.①和②都正确B.①和③都正确C.③和④都正确D.①和④都正确
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】铅氧化还原液流电池作为一种新型铅电池,具有一定的应用前景,正在逐渐成为电化学储能领域的一个研究热点。该电池以酸性甲基磺酸铅溶液为电解液,简化的工作原理如图所示,下列说法正确的是( )
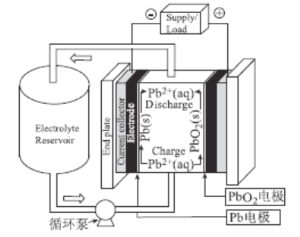
A.放电时,H+经过循环泵向Pb电极移动
B.放电时,正极反应式为PbO2+4H++2e-=Pb2++2H2O
C.充电时,阴极反应式为2H++2e-=H2↑
D.该电解液可用稀H2SO4替代,放电效果相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图像分别表示有关反应的反应过程与能量变化的关系。
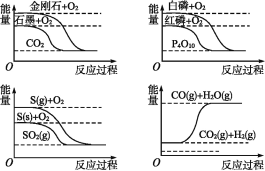
据此判断下列说法中正确的是( )
A.石墨转变为金刚石是吸热反应
B.S(g)+O2(g)![]() SO2(g) ΔH1,S(s)+O2(g)
SO2(g) ΔH1,S(s)+O2(g)![]() SO2(g) ΔH2,则ΔH1>ΔH2
SO2(g) ΔH2,则ΔH1>ΔH2
C.白磷比红磷稳定
D.CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH>0
CO2(g)+H2(g) ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温、恒容密闭容器中发生反应: A(s) +2B(g)![]() C(g)+D(g),当下列物理量不再发生变化时,表明该反应已达到平衡状态的是
C(g)+D(g),当下列物理量不再发生变化时,表明该反应已达到平衡状态的是
①混合气体的压强 ②混合气体的密度 ③各气态物质的物质的量浓度
④气体的总物质的量 ⑤混合气体的平均相对分子质量
A. ②③⑤ B. ①②③ C. ②③④⑤ D. ①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列图示所得出的结论一定错误的是
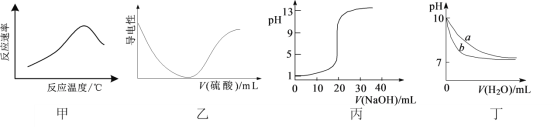
A.图甲表示酶催化反应的反应速率随反应温度的变化
B.图乙表示向BaCl2溶液中滴加稀硫酸至过量的过程中溶液导电性的变化
C.图丙表示用0.1000 mol·L-1 NaOH溶液滴定20.00 mL 0.1000 mol·L-1醋酸的滴定曲线
D.图丁表示相同温度下,向等体积pH=10的氢氧化钠溶液和氨水中分别加水稀释时pH的变化曲线,其中a表示氨水稀释时pH的变化曲线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LiFePO4电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车。电池反应为:FePO4+Li ![]() LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨,含U导电固体为电解质。下列有关LiFePO4电池说法正确的是 ( )
LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨,含U导电固体为电解质。下列有关LiFePO4电池说法正确的是 ( )
A.可加入硫酸以提高电解质的导电性
B.放电时电池内部Li+向负极移动.
C.充电过程中,电池负极材料的质量减少
D.充电时,电池阴极反应为:FePO4+Li++e-=LiFePO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向冰醋酸中加水稀释,溶液导电能力变化情况图所示,回答下列问题。
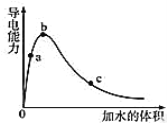
(1)a、b、c三点醋酸电离程度由大到小的顺序为________;a、b、c三点对应的溶液中c(H+)最大的是________。
(2)若实验测得c点处溶液中c(CH3COOH)=0.01 mol·L-1,c(CH3COO-)=0.0001 mol·L-1,则该条件下CH3COOH的电离常数Ka=________________。
(3)在稀释过程中,随着醋酸浓度的降低,下列始终保持增大趋势的量是(_______)。
A.c(H+) B.溶液pH C.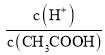 D.CH3COOH分子数
D.CH3COOH分子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是 ( )
A.明矾溶液中加入过量的氨水 Al3++4OH-=AlO2-+2H2O
B.次氯酸钙溶液中通入过量二氧化碳:ClO-+H2O+CO2=HClO+CO32-
C.用石墨作电极电解饱和食盐水: ![]()
D.澄清的石灰水中加入少量的NaHCO3溶液:Ca2++2OH-+2HCO3-=CaCO3↓+ 2H2O + CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2.0mol PCl3和1.0mol Cl2充入体积不变的密闭容器中,在一定条件下发生下述反应: PCl3(g)+Cl2(g)![]() PCl5(g)达平衡时,PCl5为0.40mol,如果此时再移走1.0mol PCl3和0.50mol Cl2,在相同温度下再达平衡时PCl5的物质的量是( )
PCl5(g)达平衡时,PCl5为0.40mol,如果此时再移走1.0mol PCl3和0.50mol Cl2,在相同温度下再达平衡时PCl5的物质的量是( )
A.0.40molB.0.20mol
C.小于0.20molD.大于0.20mol,小于0.40mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com