
【题目】2007年9月,美国科学家宣称发现了普通盐水在无线电波照射下可燃烧,这很可能是21世纪人类最伟大的发现之一,有望解决用水作人类能源的重大问题.无线电频率可以降低盐水中所含元素之间的“结合力”,释放出氢原子,若点火,氢原子就会在该种频率下持续燃烧.上述中“结合力”实质是( )
A.分子间作用力B.氢键C.非极性共价键D.极性共价键
科目:高中化学 来源: 题型:
【题目】化学上常用燃烧法确定有机物的组成。下图是用燃烧法确定有机物化学式常用的装置,该方法是在电炉加热时用纯氧氧化管内样品。根据产物的质量确定有机物的组成。

回答下列问题:
(1)A装置中发生反应的化学方程式为______________________________________,
(2)C装置(燃烧管)中CuO的作用是_______________________________________,
(3)写出E装置中所盛放试剂的名称_____________,
(4)将4.6 g有机物M进行实验,测得生成5.4 g H2O和8.8 g CO2,则该物质的实验式是________。
(5)经测定,有机物M的核磁共振氢谱示意图如图,则M的结构简式为_____________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 分子的结构是由键角决定的
B. H2O分子中的两个O—H键的键角为180°
C. CF4、CCl4、CBr4、CI4中C—X键的键长、键角均相等
D. 共价键的键能越大,共价键越牢固,由该键形成的分子越稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微型实验因操作简单、装置小巧、安全可靠、减少污染等特点而被广泛应用,而且其原理和工业原理相同,图中所示是实验室中进行NH3的催化氧化实验的装置(附着在玻璃纤维上的Cr2O3做催化剂),图中的铁架台、酒精灯等已经略去,若化学药品可随便取用(尽可能按照实验室制气方法配制),则:

(1)若A中产生的气体遇到HCl 气体冒出白烟,叉型管中的固体物质A是_______, B 是_______。
(固体物质A、B可以是一种物质也可以是多种物质的混合物)
(2)C处发生 反应的化学方程式为______________,该反应中还原剂是_______;在工业 上,该反应要求气体_______(气体名称) 过量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜及其化合物在工业生产及生活中用途非常广泛。回答下列问题:
(1)基态铜原子价电子排布式为____________;第一电离能I(Cu)________I (Zn)(填“>”或“<”)
(2)配合物[Cu (CH3CN) 4] BF4[四氟硼酸四(乙腈)合铜(Ⅰ)]是有机合成中常见催化剂。
①该配合物中阴离子的空间构型为__________,与其互为等电子体的分子或离子是________(各举1例)。
②配体分子中与Cu(I) 形成配位键的原子为____________;配体CH3CN 中:碳原子杂化方式是______。
(3)已知Cu2O 熔点为1235 ℃,K2O 熔点为770℃,Cu2O 属于____晶体,前者熔点较高,其原因是______________________________________________________________________________
(4)Cu3N 的晶胞(立方)结构如下图所示:
①距离最近的两个Cu+间的距离为________nm。(保留两位小数)
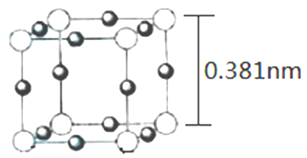
②Cu3N 晶体的密度为____________ g·cm-3。(列出计算式,不必计算出结果)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答下列问题:
(1)①Fe原子的核外电子排布式为[Ar]_________,Mg原子核外占据最高能层电子的电子云轮廓图形状为_________。
②As的卤化物的熔点如下:
AsCl3 | AsBr3 | AsI3 | |
熔点/K | 256.8 | 304 | 413 |
表中卤化物熔点差异的原因是_________,AsCl3分子的立体构型为_________。
(2)维生素B1可作为辅酶参与糖的代谢,并有保护神经系统的作用。该物质的结构式为

以下关于维生素B1的说法正确的是________。
A.只含σ键和π键
B.既有共价键又有离子键
C.该物质的熔点可能高于NaCl
D.该物质易溶于盐酸
(3)维生素B1晶体溶于水的过程中要克服的微粒间作用力有________。
A.离子键、共价键 B.离子键、氢键、共价键
C.氢键、范德华力 D.离子键、氢键、范德华力
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究铁和铁的化合物的一些化学性质,某学生实验小组设计了以下实验。
(1)往A、B溶液中分别滴入几滴KSCN溶液,溶液的颜色A________,B____________。
(2)写出上述过程中有关反应的化学方程式:
Fe2O3→A_______________________;A→B____________________________。
(3)B→C可看到的现象是___________________________________________。
(4)将A的饱和溶液滴入沸水中并不断加热,可制得_______________胶体;当光束通过该胶体时,可看到一条光亮的“通路”,这种现象称为___________效应。
【答案】血红色 不变(浅绿色) Fe2O3+6HCl=2FeCl3+3H2O Fe+2FeCl3=3FeCl2 白色沉淀转变为灰绿色又转变为红褐色 Fe(OH)3 丁达尔
【解析】
(1)氧化铁与盐酸反应生成氯化铁,氯化铁与铁反应生成氯化亚铁,因此往A、B溶液中分别滴入几滴KSCN溶液,溶液A中显血红色,B中不变色;(2)Fe2O3与盐酸反应的方程式为Fe2O3+6HCl=2FeCl3+3H2O,A→B的方程式为Fe+2FeCl3=3FeCl2。(3)氯化亚铁与氢氧化钠反应生成氢氧化亚铁,氢氧化亚铁不稳定,易被氧化,所以B→C可看到的现象是白色沉淀转变为灰绿色又转变为红褐色。(4)将氯化铁饱和溶液滴入沸水中并不断加热,可制得氢氧化铁胶体;当光束通过该胶体时,可看到一条光亮的“通路”,这种现象称为丁达尔效应。
【题型】实验题
【结束】
28
【题目】现有某铁碳合金,某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题(由实验装置引起的实验误差忽略不计)。

I、探究浓硫酸的某些性质
(1)按图示连接装置,检查装置___________,称量E的质量。
(2)将aɡ铁碳合金样品放入A中,再加入适量的浓硫酸,仪器A的名称为______,未点燃酒精灯前,A、B 均无明显现象,其原因是______________________。
(3)点燃酒精灯一段时间后,A、B中可观察到明显的现象,如A中![]() ,写出A中C和浓硫酸发生反应的化学方程式:__________________________,B中的现象是_________________,因此可得到浓硫酸具有_____________性。
,写出A中C和浓硫酸发生反应的化学方程式:__________________________,B中的现象是_________________,因此可得到浓硫酸具有_____________性。
(4)随着反应的进行,浓硫酸浓度逐渐减小变为稀硫酸,A中还可能发生某些离子反应,写出相应的离子方程式:_________________、____________________。
II、测定铁的质量分数
(5)待A中固体完全消失并不再逸出气体时,停止加热,拆下E并称重,E增重bg。铁碳合金中铁的质量分数为___________________(写表达式)。
(6)某同学认为上述方法较复杂,使用如图所示的装置和其他常用的实验仪器测定某些数据即可。为了快速和准确地计算出铁的质量分数,最简便的实验操作是___________(填写代号)。

①用排水法测定H2的体积
②反应结束后,过滤、洗涤、干燥、称量残渣的质量
③ 测定反应前后装置和药品的总质量ag
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 标准状况下,11.2 LCH2Cl2中含有分子的数目为0.5NA
B. 常温下a g某烷烃(CnH2n+2)中含有共用电子对数目为![]() (3n+1)NA
(3n+1)NA
C. 56 g 聚乙烯中含有碳碳双键的数目为2NA
D. 常温下,0.2 mol/L的FeCl3溶液中含Cl﹣数目为0.6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】诗句“春蚕到死丝方尽,蜡炬成灰泪始干”中的“丝”和“泪”分别属于
A. 纤维素、脂肪 B. 淀粉、油脂 C. 蛋白质、烃 D. 蛋白质、植物油
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com