
【题目】(1)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示。请认真观察图示,然后回答问题:
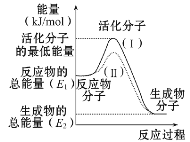
①图中所示反应是________(填“吸热”或“放热”)反应,,该反应的ΔH=________ (用含E1、E2的代数式表示)。
②已知热化学方程式:H2(g)+ ![]() O2(g)=H2O(g) ΔH=-241.8 kJ/mol。该反应的活化能为167.2 kJ/mol,则其逆反应的活化能为_____________。
O2(g)=H2O(g) ΔH=-241.8 kJ/mol。该反应的活化能为167.2 kJ/mol,则其逆反应的活化能为_____________。
(2)已知反应2HI(g)![]() H2(g)+I2(g)的ΔH=+11 kJ·mol-1,1 mol H2(g)、1 mol I2(g)分子中化学键断裂时分别需要吸收436 kJ、151 kJ的能量,则1 mol HI(g)分子中化学键断裂时需吸收的能量为________kJ。
H2(g)+I2(g)的ΔH=+11 kJ·mol-1,1 mol H2(g)、1 mol I2(g)分子中化学键断裂时分别需要吸收436 kJ、151 kJ的能量,则1 mol HI(g)分子中化学键断裂时需吸收的能量为________kJ。
【答案】放热 -(E1-E2) 409kJ/mol 299
【解析】
(1)依据图象分析反应物的能量大于生成物的能量,反应放热;在化学反应中,只有能量比平均能量高得多的反应物的活化分子发生碰撞时才能发生化学反应,反应需要能量;反应的焓变=生成物的能量-反应物的能量;
(3)反应的活化能是使普通分子变成活化分子所需提供的最低限度的能量,依据图象能量关系可知,逆反应的活化能=正反应的活化能+反应的焓变;
正反应为吸热反应,化学键断裂时需吸收的能量-化学键生成时需放出的能量=反应吸收的热量,以此解答该题.
(1) ①依据图象分析反应物的能量大于生成物的能量,反应放热;在化学反应中,只有能量比平均能量高得多的反应物的活化分子发生碰撞时才能发生化学反应,反应需要能量;反应的焓变=生成物的能量反应物的能量;△H=(E2E1)KJ/mol;
故答案为:放热;(E2E1)KJ/mol;
②反应的活化能是使普通分子变成活化分子所需提供的最低限度的能量,依据图象能量关系可知,逆反应的活化能=正反应的活化能-反应的焓变; H2(g)+ 1/2O2(g)=H2O(g) ΔH=-241.8 kJ/mol,该反应的活化能为167.2kJmol1,则其逆反应的活化能=167.2KJ/mol+241.8KJ/mol=409.0KJ/mol;
故答案为:409.0KJ/mol;
(2)设1molHI(g)分子中化学键断裂时需吸收的能量为xkJ,则:2xkJ436kJ151kJ=11kJ,解得x=299,
故答案为:299.


科目:高中化学 来源: 题型:
【题目】已知![]() 是中学化学的常见物质,且
是中学化学的常见物质,且![]() 均含有同一种元素。在一定条件下,它们之间的相互转化关系如图所示(反应中生成的v已略去)。请回答下列问题:
均含有同一种元素。在一定条件下,它们之间的相互转化关系如图所示(反应中生成的v已略去)。请回答下列问题:
(1)若A是一种可用于自来水消毒的黄绿色气体,D是目前产量最大的金属单质,则C的化学式为_______________;写出A与C的溶液反应的离子方程式:___________________________。
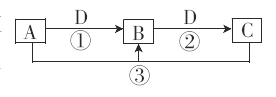
(2)若A是一种常见的强碱,D是一种气体,通常用来灭火,则反应②的离子方程式是__________________。
(3)若A是非金属固体单质,![]() 在常温下均为气体,D是空气中的主要成分,则C的化学式为________________。
在常温下均为气体,D是空气中的主要成分,则C的化学式为________________。
(4)若A是一种呈碱性的气体,![]() 为自然固氮过程,则在一定条件下反应③的化学方程式为__________________。
为自然固氮过程,则在一定条件下反应③的化学方程式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的镁和铜组成的混合物加入到足量的稀硝酸中,金属完全溶解(假设反应中还原产物只有NO)。向反应后的溶液中加3mol/LNaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g。下列叙述错误的是
A. 当金属全部溶解时,电子转移的数目为0.3NA
B. 参加反应的金属的总质量3.6g<w<9.6g
C. 当金属全部溶解时,产生的NO气体的体积在标准状况下为2.24L
D. 当生成的沉淀量达到最大时,消耗NaOH溶液的体积为l00mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列实验过程完成后,最终的白色沉淀不一定是BaSO4的是( )
A.Fe(NO3)3溶液![]()
![]()
![]() 白色沉淀
白色沉淀
B.Ba(NO3)2溶液![]()
![]() 白色沉淀
白色沉淀
C.无色溶液![]() 无沉淀
无沉淀![]() 白色沉淀
白色沉淀
D.无色溶液![]()
![]() 白色沉淀
白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨工业对国民经济和社会发展具有重要的意义,对密闭容器中的反应:N2(g)+3H2(g) ![]() 2NH3(g) △H<0。400℃、30MPa下n(NH3)和n(H2)随时间变化的关系如图,下列叙述错误的是( )
2NH3(g) △H<0。400℃、30MPa下n(NH3)和n(H2)随时间变化的关系如图,下列叙述错误的是( )
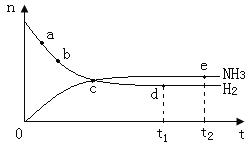
A.点a的正反应速率比b点的大
B.点c处反应还未达到平衡
C.点d(t1时刻)和点e(t2时刻)处n(N2)不一样
D.其他条件不变,500℃下反应至t1时刻,n(H2)比右图中d点的值大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)“电解”所用食盐水由粗盐水精制而成,精制时,为除去Mg2+和Ca2+,要加入的试剂分别为________、________。
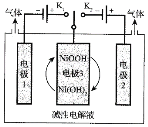
(2)氢能源是最具应用前景的能源之一,高纯氢制备是目前的研究热点。可利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接K1或K2,可交替得到H2和O2。
①制H2时,连接_______________(填K1或者K2)。产生H2的电极反应式是_____________。
②改变开关连接方式,可得O2,写出制备氧气时电极3对应的电极反应式是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W原子序数依次增大,Y的原子半径是短周期主族元素原子中最大的,X与Z属于同一主族,Z的最外层电子数为最内层电子数的3倍。下列说法正确的是
A.原子半径: r(Y)>r(W)>r(Z)>r(X)
B.由X、Y组成的化合物中均不含共价键
C.W的氧化物对应水化物的酸性比Z的强
D.X的简单气态氢化物的热稳定性比Z的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应4NH3+5O2![]() 4NO+6H2O(g),下列叙述正确的是( )
4NO+6H2O(g),下列叙述正确的是( )
A.达到平衡状态,2 v正(NH3)= 3v逆(H2O)
B.单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D.反应达到平衡时,反应物的转化率一定小于100%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由CH3CH2CH2Br制备CH3CH(OH)CH2OH,依次从左至右发生的反应类型和反应条件都正确的是 ( )
选项 | 反应类型 | 反应条件 |
A | 加成反应;取代反应;消去反应 | KOH醇溶液 |
B | 消去反应;加成反应;取代反应 | NaOH水溶液 |
C | 氧化反应;取代反应;消去反应 | 加热;KOH醇溶液 |
D | 消去反应;加成反应;水解反应 | NaOH醇溶液 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com