
【题目】在下列实验过程完成后,最终的白色沉淀不一定是BaSO4的是( )
A.Fe(NO3)3溶液![]()
![]()
![]() 白色沉淀
白色沉淀
B.Ba(NO3)2溶液![]()
![]() 白色沉淀
白色沉淀
C.无色溶液![]() 无沉淀
无沉淀![]() 白色沉淀
白色沉淀
D.无色溶液![]()
![]() 白色沉淀
白色沉淀
【答案】D
【解析】
A. 硝酸铁中有硝酸根离子存在,加入过量的稀盐酸,就相当于硝酸存在,与二氧化硫发生氧化还原反应生成硫酸根离子,加入氯化钡,最终生成BaSO4沉淀,A项不符合;
B. 硝酸钡溶液中有硝酸根离子存在,加入过量的稀盐酸,就相当于硝酸存在,加入亚硫酸钠,亚硫酸根离子被硝酸氧化成硫酸根离子,所以一定是BaSO4沉淀,B项不符合;
C. 无色溶液,加盐酸无沉淀,可以排除碳酸根、亚硫酸根、银离子的干扰,再加入氯化钡生成白色沉淀,一定是BaSO4沉淀,C项不符合;
D. 无色溶液加入稀硝酸,加入氯化钡,Ag+可能干扰,最终生成的白色沉淀可能是AgCl或BaSO4,D项符合;
答案选D。


 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:
【题目】ClO2是一种优良的消毒剂,浓度过高时易发生分解,常将其制备成NaClO2固体以便运输和贮存。过氧化氢法制备NaClO2固体的实验装置如图所示。

已知:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O
2ClO2+H2O2+2NaOH=2NaClO2+O2↑+2H2O
ClO2熔点-59 ℃、沸点11 ℃;H2O2沸点150 ℃。
请回答:
(1)仪器A的名称为________;仪器B的作用是________;冰水浴冷却的目的是____________(写出两种)。
(2)空气流速过快或过慢,均降低NaClO2产率,试解释其原因______________。
(3)Cl-存在时会催化ClO2的生成。反应开始时在三颈烧瓶中加入少量盐酸,ClO2的生成速率大大提高,并产生微量氯气。该过程可能经两步反应完成,将其补充完整:①_______________________________(用离子方程式表示),②H2O2+Cl2=2Cl-+O2+2H+。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向![]() 和NaOH混合溶液中缓慢通入
和NaOH混合溶液中缓慢通入![]() 至过量
至过量![]() 溶液温度变化忽略不计
溶液温度变化忽略不计![]() ,生成沉淀物质的量与通入
,生成沉淀物质的量与通入![]() 体积的关系如图所示。下列说法不正确的是
体积的关系如图所示。下列说法不正确的是![]()
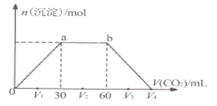
A.b点时溶质为![]()
B.横坐标轴上![]() 的值为90
的值为90
C.![]() 、
、![]() 、
、![]() 时,溶液
时,溶液![]() 中相等
中相等
D.原混合物中![]() :
:![]() ;2
;2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于平衡体系:aA(g)+bB(g)![]() cC(g)+dD(g);正反应放热,有下列判断,其中正确的是( )
cC(g)+dD(g);正反应放热,有下列判断,其中正确的是( )
A.若温度不变,容器体积扩大一倍,此时A的浓度是原来的0.6倍,则a+b<c+d
B.若从正反应开始,A、B的初始物质的量之比为1:1,则平衡时A、B的转化率一定相等
C.若平衡体系中共有气体M mol,再向其中充入b mol B,达到平衡时气体总物质的量为(M+b)mol,则a+b>c+d
D.若从正反应开始,平衡时A、B的转化率相等,则投入A、B物质的量之比为a:b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组以有机物A为原料,合成抗癌药——拉帕替尼的中间体H的具体路线如下:
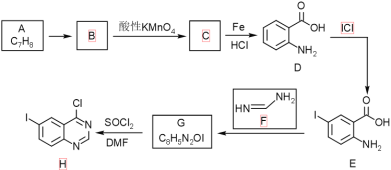
已知:①![]()
②![]()
回答下列问题:
(1)C的名称为________________。D中所含官能团的名称为________________。G的结构简式为________________。
(2)B→C的反应类型为________________。
(3)A分子中共面原子数最多为___________。
(4)A→B的化学方程式为____________________________________________。
(5)碳原子上连有4个不同原子或基团时,该碳原子为手性碳原子。写出D与足量H2反应后产物的结构简式,并用星号(*)标出其中的手性碳原子_________________。
(6)C有多种同分异构体,其中满足下列条件的同分异构体共有_______种。
①分子中含有苯环;②分子中含有-NO2(不考虑-O-NO2);③能发生银镜反应
其中核磁共振氢谱有3组峰,并且峰面积之比为1:2:2的有机物结构简式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年11月第四届国际碳材料大会在上海举行,碳材料产品丰富,应用广泛,让人感到“碳为观止”。下列有关说法正确的是
A.金刚石与石墨互为同位素
B.石墨烯是一种有发展前途的导电材料
C.碳纤维、合成纤维、光导纤维都属于高分子材料
D.富勒烯是由60个碳原子都以碳碳单键构成的分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示。请认真观察图示,然后回答问题:
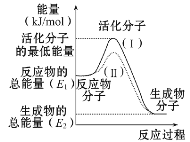
①图中所示反应是________(填“吸热”或“放热”)反应,,该反应的ΔH=________ (用含E1、E2的代数式表示)。
②已知热化学方程式:H2(g)+ ![]() O2(g)=H2O(g) ΔH=-241.8 kJ/mol。该反应的活化能为167.2 kJ/mol,则其逆反应的活化能为_____________。
O2(g)=H2O(g) ΔH=-241.8 kJ/mol。该反应的活化能为167.2 kJ/mol,则其逆反应的活化能为_____________。
(2)已知反应2HI(g)![]() H2(g)+I2(g)的ΔH=+11 kJ·mol-1,1 mol H2(g)、1 mol I2(g)分子中化学键断裂时分别需要吸收436 kJ、151 kJ的能量,则1 mol HI(g)分子中化学键断裂时需吸收的能量为________kJ。
H2(g)+I2(g)的ΔH=+11 kJ·mol-1,1 mol H2(g)、1 mol I2(g)分子中化学键断裂时分别需要吸收436 kJ、151 kJ的能量,则1 mol HI(g)分子中化学键断裂时需吸收的能量为________kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S是一种剧毒气体,如图为质子膜H2S燃料电池的示意图,可对H2S废气资源化利用。下列叙述不正确的是( )
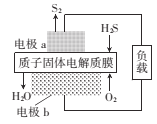
A.电池工作时,化学能转化为电能和热能
B.电极b上发生的电极反应式为O2+ 4e+4H+=2H2O
C.a是负极,电池工作时,电子的流动方向是:电极a→负载→电极b→质子膜→电极a
D.当电路中通过4mol电子时,有4molH+经质子膜进入正极区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机化合物的结构简式如图所示,下列说法不正确的是( )
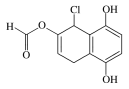
A.能发生银镜发应
B.能与FeCl3溶液发生显色反应
C.1 mol该物质最多可与4 mol NaOH反应
D.与NaHCO3、Na2CO3溶液均能发生反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com