
ij����ɱ���ܱ�������ʢ��������A��B�Ļ�����壬��һ�������·�����Ӧ��A + 3B  2C����ά���¶Ⱥ�ѹǿ���䣬���ﵽƽ��ʱ�����������ΪV L������C��������ռ10%�������ƶ���ȷ���ǣ� ��
2C����ά���¶Ⱥ�ѹǿ���䣬���ﵽƽ��ʱ�����������ΪV L������C��������ռ10%�������ƶ���ȷ���ǣ� ��
��ԭ�����������Ϊ1.2VL ��ԭ�����������Ϊ1.1VL
�۷�Ӧ��ƽ��ʱ,����A���ĵ�0.05VL �ܷ�Ӧ��ƽ��ʱ������B���ĵ�0.05V L
A���ڢ� B���ڢ� C���٢� D���٢�
A
��������
������������ݷ�Ӧ�� A + 3B 2C
2C
����������仯�� 0.05V 0.15V 0.1V
����������C��������ڷ�Ӧ�л��������ٵ����������Ϊ0.1V������A�����ĵ�������ڻ��������ٵ��������һ�룬����B�����ĵ�������ڻ��������ٵ��������1.5 ��������ƽ��ʱ���������10%V L����ԭ�����������ӦΪ1V L+10%V L��1.1V L������ƽ��ʱ������A������Ϊ����10%V L��0.05V L������B������Ϊ��5��10%V L��0.15V L����ѡA��
���㣺����ѧ��������������йؼ���


 �����Ƹ���ʦ����ϵ�д�
�����Ƹ���ʦ����ϵ�д� ��ͨ����ͬ����ϰ��ϵ�д�
��ͨ����ͬ����ϰ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ��һ��ѧ�����л�ѧ�Ծ��������棩 ���ͣ������
��9�֣���֪ͭ��Ũ��������ڼ��������·�����Ӧ����ѧ����ʽ���£�����ƽ����
Cu��2H2SO4(Ũ) 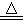 CuSO4��A����2H2O
CuSO4��A����2H2O
��ͨ����������������������⣺
��1���ڲμӷ�Ӧ�������У�����ԭ��������δ����ԭ����������ʵ���֮��Ϊ ��A���ʿ�����ǿ�Ӧ�����κ�ˮ����AӦ������ ������ĸ������д����
a���� b���� c���� d������������ e������������
��2��һ������ͭƬ�뺬1.8mol H2SO4��ŨH2SO4��ַ�Ӧ��ŨH2SO4������������÷�Ӧ������ת����0.2 mol���ӣ����ɵ�CuSO4������Ϊ g�����ɵ�A�����ڱ�״�������Ϊ
L����������ȫ���ݳ�����
��3������2���з�Ӧ�����õ�����Һϡ�ͺ�������Ba(OH)2��Һ��Ӧ�����ó���������Ϊ g��д���˹����з�����Ӧ�����ӷ���ʽ��
��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�߶���ѧ��10���¿���ѧ�Ծ��������棩 ���ͣ�ʵ����
ʵ������ȼ�շ��ⶨij�����л���A�ķ�����ɣ��ⶨװ����ͼ(����̨�����С��ƾ��Ƶ�δ����)��H:1 O:16 C:12

ȡ17.1 g A����װ���У�ͨ�����O2ȼ�գ�����CO2��H2O����ش������й����⣺
��1��ͨ�����O2��Ŀ���� ��
��2��Cװ�õ������� ��
Dװ�õ������� ��
��3��ͨ����ʵ�飬�ܷ�ȷ��A���Ƿ�����ԭ�ӣ�________��
��4����A��Ħ������Ϊ342 g/mol��Cװ������9.99 g��Dװ������26.4 g����A�ķ���ʽΪ________��
��5��д��Aȼ�յĻ�ѧ����ʽ ��
��6��A�ɷ���ˮ�ⷴӦ��1 mol A��ˮ������2 molͬ���칹�壬��A�ڴ���������ˮ��Ļ�ѧ���� ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�߶���ѧ��10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���������������
A����ϩ�ͱ�����ʹ��ˮ��ɫ����ɫ��ԭ����ͬ
B�����ۡ���֬�������ʶ���ˮ�⣬��ˮ����ﲻͬ
C��ú�Ϳ���ʯ�ͷ����ã�������ȼ�Ϻͱ�������������
D���Ҵ������ᡢ�����������ܷ���ȡ����Ӧ�����������е�����������ñ���Na2CO3��Һ��ȥ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������人�������и߶�10���¿���ѧ���������Ծ��������棩 ���ͣ������
(10��)����ȼ�տ���ͨ����������;����
;��I��C3H8(g) + 5O2(g) == 3CO2(g) +4H2O(l) ��H��-a kJ��mol-1
;��II��C3H8(g) == C3H6(g)+ H2(g) ��H��+b kJ��mol-1
2C3H6(g)+ 9O2(g) == 6CO2(g) +6H2O(l) ��H��-c kJ��mol-1
2H2(g)+O2 (g) == 2H2O(l) ��H��-d kJ��mol-1 (a��b��c��d��Ϊ��ֵ)
��ش��������⣺
��1���жϵ����ı���ͨ������;���ų���������;��I�ų������� (����ڡ��������ڡ���С�ڡ�);��II�ų���������
��2������C3H8(g) ==C3H6(g)+ H2(g) �ķ�Ӧ�У���Ӧ����е������� (����ڡ��������ڡ���С�ڡ�)��������е�����������ô�ڻ�ѧ��Ӧʱ,��Ӧ�����Ҫ (��ų����������ա�)��������ת��Ϊ���������䷴Ӧ������ ��
��3��b ��a��c��d����ѧ��ϵʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������人�������и߶�10���¿���ѧ���������Ծ��������棩 ���ͣ�ѡ����
��2molSO2 ��1molO2����һ�ݻ��̶����ܱ�������,��һ�������·�����Ӧ��2SO2(g)+O2(g) 2SO3(g)��������Щ�����ٱ仯ʱ������˵����ѧ��Ӧ�Ѵ�ƽ��״̬�� ��
2SO3(g)��������Щ�����ٱ仯ʱ������˵����ѧ��Ӧ�Ѵ�ƽ��״̬�� ��
A�����������ܶ� B����������ѹǿ
C���������������ʵ��� D����������ƽ����Է�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������人�������и߶�10���¿���ѧ���������Ծ��������棩 ���ͣ�ѡ����
1gH2��O2��ȼ������Һ̬ˮ�ų�142.9kJ���������������Ȼ�ѧ����ʽ��ȷ���ǣ� ��
A��2H2(g) + O2(g) = 2H2O(l) ��H=-142.9kJ��mol-1
B��2H2(g) + O2(g) = 2H2O(l) ����H=-571.6kJ��mol-1
C��H2(g) + 1/2O2(g) = H2O(g) ����H=-285.8kJ��mol-1
D��H2(g) + 1/2O2(g) = H2O(l) ����H=- 285.8kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���㽭ʡ�����и�һ��ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij�л���Ľṹ��ʽΪ

������������ȷ����
A��1mol���л����������������Ʒ�Ӧ�ų�1molH2
B�������Ҵ�����������Ӧ
C��1mol���л����ڴ����������������1molH2������ԭ��Ӧ
D��1mol���л�����������NaHCO3��Һ��Ӧ�ų�2 molCO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���㽭ʡ������ʮУ�������һ��ѧ������������ѧ�Ծ��������棩 ���ͣ������
��3�֣�2.3g������ˮ���γ���Һ��������Һ��Na����H2O�ĸ�����Ϊ1:100���������Ҫ���� ��ˮ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com